氨基酸转运体SLC7A5调节小鼠肠道细胞增殖
来源:生物谷原创 2024-05-02 16:53
本研究通过引入mTORC1信号通过敲除肠上皮细胞中的氨基酸转运体SLC7A5而减少的遗传模型,进一步证明了mTORC1信号在肠道内稳态中的作用。
肠道是负责消化和吸收营养物质和水分的器官,也是抵御环境有害物质/生物的屏障。它不断受到来自食物消化和肠道内数以万亿计的微生物的机械、化学和病原体驱动的攻击,因此,维持肠道的完整性和功能至关重要。肠道内稳态依赖于肠上皮、下层非上皮组织、微生物群和免疫系统内不同类型细胞之间相互作用的完美平衡。
肠上皮细胞对肠道稳态至关重要,在成体干细胞的驱动下,小鼠每3-5天就会不断更新一次。两种类型的上皮细胞,杯状细胞和潘氏细胞,维持肠道的完整性。杯状细胞分泌粘液,覆盖上皮,阻止微生物群进入粘膜,并允许高浓度抗微生物肽(amp)的积累。杯状细胞数量减少和粘液分泌减少是人类炎症性肠病(IBD)的标志。Paneth细胞分泌AMPs,包括溶菌酶和防御素,保护上皮免受病原体侵害。
SLC7A5,也称为LAT1,通过与糖蛋白CD98 (SLC3A2)相互作用形成异二聚体氨基酸转运体,涉及一个保守的二硫键。异二聚体运输大量中性氨基酸,对免疫系统、胎盘、血脑屏障和保护机体免受病原体侵害至关重要,通过破坏CD98的细胞外结构域破坏转运体功能导致小鼠胚胎致死。众所周知,slc7a5介导的mTORC1激活对免疫系统,尤其是T细胞激活具有重要作用。SLC7A5在包括肠在内的许多器官中广泛表达。然而,slc7a5介导的mTORC1激活是否以及如何在肠道稳态和功能中发挥作用仍然未知。虽然有关于肠道中mTORC1信号传导的研究,但主要集中在能量利用上,研究结果不太一致。因此,需要进一步分析mTORC1信号在肠道稳态中的作用和调控。

图片来源:https://pubmed.ncbi.nlm.nih.gov/38617535/
近日,来自美国马里兰州贝塞斯达国立卫生研究院的研究者们在Int J Biol Sci杂志上发表了题为“Amino acid transporter SLC7A5 regulates cell proliferation and secretary cell differentiation and distribution in the mouse intestine”的文章,该研究表明氨基酸转运体SLC7A5可能通过调节分泌细胞分化影响干细胞生态位,间接调节细胞增殖。
肠道不仅对营养物质的处理至关重要,而且还能保护机体免受环境的影响。这些功能主要由不断自我更新的上皮细胞完成。许多基因和途径可以影响肠上皮细胞的增殖。其中有mTORC1,其激活可促进细胞增殖。

肠上皮细胞特异性敲除SLC7A5可导致小肠隐窝延长
图片来源:https://pubmed.ncbi.nlm.nih.gov/38617535/
在这里,研究者报告了肠上皮细胞(IEC)特异性敲除(ΔIEC)能够激活mTORC1的氨基酸转运体。研究者发现,转运蛋白SLC7A5在小鼠肠隐窝中高度表达,Slc7a5ΔIEC可减少mTORC1信号传导。令人惊讶的是,成人Slc7a5ΔIEC肠隐窝增加了细胞增殖,但减少了成熟的Paneth细胞。杯状细胞是小肠中另一种主要的分泌细胞类型,在隐窝中增多,而在绒毛中减少。scRNA-seq和电镜分析显示Slc7a5ΔIEC小鼠Paneth细胞去分化,导致分泌颗粒明显减少,但对Paneth细胞数量影响不大。因此,SLC7A5可能通过调节分泌细胞分化影响干细胞生态位,间接调节细胞增殖。
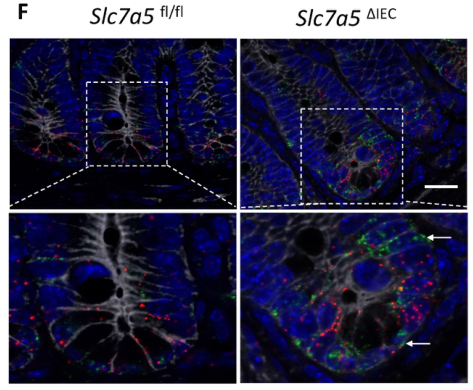
Slc7a5ΔIEC分泌颗粒在Paneth细胞和增加隐窝基干细胞有丝分裂活性
图片来源:https://pubmed.ncbi.nlm.nih.gov/38617535/
综上所述,本研究通过引入mTORC1信号通过敲除肠上皮细胞中的氨基酸转运体SLC7A5而减少的遗传模型,进一步证明了mTORC1信号在肠道内稳态中的作用。研究者发现SLC7A5的缺失导致Paneth细胞去分化,通过分泌颗粒的减少导致分泌功能的破坏。Slc7a5ΔIEC小鼠的整体表型与mTORC1肠上皮细胞特异性敲除小鼠相似。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


