Nature:大脑的“邻里效应”,细胞如何互相加速或延缓衰老?
来源:生物探索 2024-12-27 11:33
衰老是生物体不可避免的过程,而大脑作为神经系统的核心,不仅在维持认知功能中扮演着重要角色,同时也是衰老影响最深远的器官之一。随着年龄增长,大脑中的细胞和组织会经历显著的退化,表现为认知能力下降、记忆力
衰老是生物体不可避免的过程,而大脑作为神经系统的核心,不仅在维持认知功能中扮演着重要角色,同时也是衰老影响最深远的器官之一。随着年龄增长,大脑中的细胞和组织会经历显著的退化,表现为认知能力下降、记忆力衰退,以及神经退行性疾病(如阿尔茨海默病)的风险显著增加。然而,尽管我们对衰老过程中分子和细胞水平的变化已有一定了解,现有研究大多集中于单细胞转录组学,忽视了细胞之间的空间关联和相互作用。这种空间维度的缺失限制了我们对衰老如何在组织层面扩散和加剧的深入理解。
为了填补这一空白,12月18日Nature的研究报道“Spatial transcriptomic clocks reveal cell proximity effects in brain ageing”,利用一种先进的高通量空间转录组学技术——多重误差修复荧光原位杂交(MERFISH),首次构建了涵盖4.2百万细胞的单细胞分辨率小鼠大脑衰老全景图谱,横跨小鼠整个成年生命周期。研究人员不仅在时间维度上捕捉了细胞种类和基因表达的动态变化,还在空间维度上揭示了不同细胞之间的相互作用与影响,甚至包括罕见细胞类型(如T细胞和神经干细胞,NSC)。此外,该研究进一步开发了基于机器学习的“空间衰老时钟”(spatial ageing clocks),可以精准预测细胞的生物年龄,揭示不同细胞类型对周围细胞的“促衰老”或“促年轻化”效应。
研究结果表明,大脑中的T细胞随年龄增长显著增加,并通过邻近效应对周围细胞产生强烈的促衰老作用;而神经干细胞则表现出显著的促年轻化效应,为潜在的抗衰老干预提供了重要的靶点。更为引人注目的是,研究还探索了运动和基因重编程等干预手段对衰老的影响,为延缓甚至逆转大脑衰老提供了重要的科学依据。

大脑衰老:隐藏的危机
随着年龄增长,大脑衰老逐渐成为影响人类健康的重要因素。它不仅导致认知功能的退化,例如记忆力减弱、信息处理能力下降,还显著增加了神经退行性疾病(如阿尔茨海默病和帕金森病)的风险。衰老对大脑的影响深刻且多层次,它改变的不仅仅是单个细胞的生理状态,更体现在细胞之间复杂的相互作用和空间组织上。然而,现有研究多聚焦于单细胞的基因表达变化,忽视了细胞与邻近细胞之间的关联性及其在组织衰老中的作用,这使得我们对大脑衰老的理解仍然碎片化。
研究发现,大脑的衰老不仅表现为某些细胞类型的减少,还伴随着一些细胞类型的显著增多。例如,小胶质细胞(microglia)和T细胞(T cells)在衰老过程中数量明显增加,而神经干细胞(neural stem cells, NSCs)和神经母细胞(neuroblasts)则逐渐减少。这种细胞组成的变化直接影响了大脑的生理功能和修复能力。数据显示,T细胞的比例从年轻小鼠(3.4个月)的极低水平增加到老年小鼠(34.5个月)时的显著高峰(相关性r = 0.72)。与此同时,NSC的比例则从年轻时的较高水平下降到几乎不可检测的低值(相关性r = -0.93)。这些动态变化为我们揭示了细胞种类间的“此消彼长”,预示着大脑环境的逐渐恶化。
此外,衰老不仅是“单细胞”的孤立现象,它可能通过细胞之间的“邻里效应”加剧整个组织的老化。例如,T细胞被发现对周围细胞具有强烈的“促衰老”效应,而NSC则展现出“促年轻化”的潜力。这种跨细胞的相互影响或许是大脑衰老过程加速的关键所在。
技术突破:揭开脑衰老的时空之谜
理解大脑衰老的复杂过程,需要不仅在时间维度上捕捉细胞变化,还要解码细胞在组织空间中的相互作用。然而,传统的单细胞RNA测序技术虽然能够揭示细胞的基因表达,但却无法提供空间位置信息,限制了我们对组织层面衰老机制的全面理解。该研究通过采用一种先进的高通量空间转录组学技术——多重误差修复荧光原位杂交(MERFISH),成功实现了对小鼠大脑在单细胞水平的时空解析,为揭示大脑衰老的全貌打开了一扇全新的大门。
MERFISH技术的核心优势在于其能够在保持组织空间结构的同时,对单个细胞内的数百种基因进行高精度测量。在该研究中,研究团队利用MERFISH对20个不同年龄阶段的小鼠大脑进行系统分析,涵盖了从3.4个月到34.5个月的完整生命周期。这项技术帮助研究人员从冠状切片和矢状切片中收集了总计超过420万细胞的空间转录组数据,分析了300个关键基因,这些基因涵盖了细胞类型标记、衰老相关通路以及疾病相关过程。这种无损组织结构的技术,使得研究人员能够以细胞类型为单位,准确定位不同基因的表达,同时揭示细胞之间的空间关联。
研究的创新之处在于,它不仅捕捉了细胞在时间维度上的变化,还首次揭示了空间维度中细胞比例和分布的动态特征。例如,研究发现,兴奋性神经元和抑制性神经元主要分布于皮层区域,而小胶质细胞和少突胶质细胞则更多集中于白质区。更重要的是,MERFISH技术揭示了特定细胞(如T细胞和神经干细胞)对周围邻近细胞的影响,这为理解衰老过程中的“邻里效应”提供了新的视角。
通过MERFISH,研究团队得以绘制出世界首个大脑衰老的时空地图,这不仅填补了单细胞技术在空间信息上的空白,也为进一步研究大脑衰老及其干预策略提供了强大的技术工具。
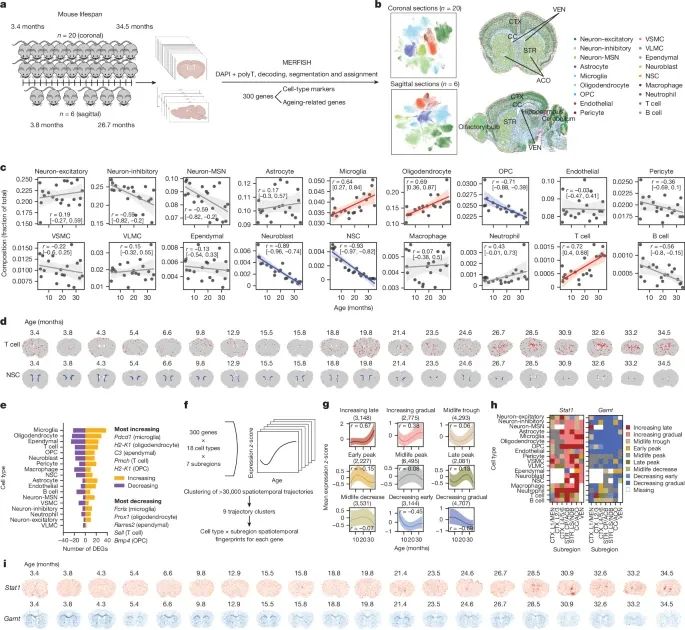
跨生命周期的大脑单细胞空间转录组学分析(Credit: Nature)
通过MERFISH技术进行的跨生命周期小鼠大脑单细胞空间转录组学研究,系统分析了不同年龄阶段的细胞类型和基因表达的动态变化。
a. 实验流程
实验的整体设计,研究通过从不同年龄段小鼠的大脑冠状切片和矢状切片中采样,并利用MERFISH技术测量300个基因的表达,这些基因涵盖了细胞类型标记、衰老相关通路和疾病相关基因。这项实验覆盖了整个成年生命周期,从年轻小鼠(3.4个月)到老年小鼠(34.5个月),提供了高分辨率的单细胞空间转录组数据。
b. 细胞类型的空间分布与UMAP投影
使用UMAP可视化所有冠状切片和矢状切片中的单细胞数据,并根据细胞类型进行着色:左侧UMAP图,展示了所有细胞的类型分布,如神经元、胶质细胞和免疫细胞等。右侧空间分布图,显示了一个典型冠状切片和一个典型矢状切片中细胞的空间分布,并标注了解剖学区域(如皮层、胼胝体等)。结果显示,不同细胞类型在空间上的分布高度一致,例如兴奋性神经元主要集中于皮层,而小胶质细胞和少突胶质细胞则更多分布于白质区域。
c. 细胞类型组成的年龄相关变化
研究分析了冠状切片数据集中不同细胞类型随年龄的比例变化,每个点代表一只小鼠。使用回归曲线拟合结果显示:随年龄增加,T细胞和小胶质细胞的比例显著上升(标记为红色,表明正相关),例如T细胞的相关性r = 0.72。神经干细胞(NSCs)和少突胶质祖细胞(OPCs)则显著下降(标记为蓝色,表明负相关),如NSCs的相关性r = -0.93。
d. 细胞在空间中的分布
以散点图显示了所有冠状切片中细胞的空间分布:不同类型的细胞用颜色标记,例如T细胞(红色)和NSCs(蓝色),其他细胞为灰色。结果揭示了不同细胞类型在空间分布上的显著差异,并且细胞间的空间邻近关系可能对衰老过程产生重要影响。
e. 基因表达的年龄相关变化
分析了每种细胞类型中随年龄表达显著变化的基因数量:小胶质细胞中表现出最多的基因表达变化,尤其是免疫相关基因的显著上调。统计了前五种细胞类型中基因变化幅度最大的基因,例如 Pdcd1(上调)和 Fcrls(下调)。
f. 时空基因表达轨迹聚类
构建了基因、细胞类型和空间亚区域的轨迹聚类,识别出九种不同的时空表达模式(如“逐步增加”、“早期下降”等)。这些轨迹揭示了基因表达在衰老过程中随时间和空间的动态变化规律,例如免疫相关基因的“晚期增加”轨迹与衰老炎症加剧一致。
g. 基因表达的分布趋势
绘制了基因表达随年龄的平滑中值曲线及其区间误差范围。不同基因轨迹显示了与年龄的Pearson相关性,例如某些基因在晚期表现出强烈的上调或下调趋势。
h. 两个关键基因的轨迹热图
以热图形式显示了两个代表性基因(Stat1 和 Gamt)的轨迹:Stat1(免疫响应基因)呈现“晚期增加”模式,尤其在免疫细胞中显著上调。Gamt(肌酸合成基因)在神经元中呈现“逐步减少”模式,反映了神经代谢功能的下降。
i. 空间基因表达的直接可视化
显示了细胞空间分布中的基因表达水平:例如,Stat1 的表达水平主要分布于免疫细胞区域(红色),而 Gamt 的表达则集中在代谢活跃的区域(蓝色)。
衰老的大脑地图:细胞组成的动态变化
大脑是一个由多种细胞类型构成的复杂网络,而衰老不仅改变了这些细胞的功能,还显著影响了它们的组成和分布。通过构建覆盖整个生命周期的小鼠大脑衰老时空图谱,研究人员揭示了不同细胞类型在衰老过程中比例的动态变化及其潜在的生物学意义。
在年轻阶段,大脑中神经元占据主导地位,这些兴奋性和抑制性神经元(neuron-excitatory, neuron-inhibitory)分布于皮层区域,维持着大脑的正常信息传递与处理功能。然而,随着年龄增长,这些神经元的比例逐渐减少,同时,支持性和免疫相关的细胞类型显著增加。例如,小胶质细胞(microglia)和少突胶质细胞(oligodendrocyte)在衰老过程中表现出持续上升的趋势。其中,小胶质细胞作为大脑的常驻免疫细胞,其比例从年轻小鼠的约0.03增加到老年小鼠的约0.06,增幅达一倍以上。这种增加表明大脑正在经历更强的炎症反应,而这种低度慢性炎症(也被称为“炎症衰老”)与神经退行性疾病的发生密切相关。
更值得注意的是,免疫细胞T细胞(T cell)的比例在衰老过程中显著提升,显示出其潜在的促衰老作用。研究发现,T细胞比例与年龄呈显著正相关(r = 0.72),而其分布并不局限于特定区域,几乎遍布整个大脑。这种现象暗示了T细胞可能通过释放促炎因子对周围细胞产生广泛影响,加速衰老进程。
相较之下,神经干细胞(NSC)和神经母细胞(neuroblast)的比例却大幅下降。研究显示,NSC在年轻阶段活跃于侧脑室区域(ventricular zone),但其比例从3.4个月的小鼠高峰下降到34.5个月时几乎不可检测(r = -0.93)。这一发现揭示了随着衰老,大脑的自我修复和再生能力显著减弱,进一步加剧了功能退化的风险。
这种细胞组成的动态变化反映了大脑在衰老过程中从“功能性”向“保护性”的转变——神经元减少,免疫细胞和胶质细胞增加。尽管这种变化可能是大脑自我保护的一种尝试,但同时也为疾病的发生和进展埋下了隐患。
邻里效应:细胞间的“善”与“恶”
衰老并非仅仅是个体细胞内的孤立事件,它更是一种由细胞间复杂互动所推动的“社会性”现象。在大脑中,某些细胞的“邻里效应”对周围环境的影响尤为显著,甚至可以在局部范围内加速或延缓衰老的进程。该研究通过“空间衰老时钟”(spatial ageing clocks)技术,首次揭示了T细胞和神经干细胞(NSC)在这一过程中截然不同的角色——前者扮演“加速衰老”的反派,而后者则以“促进年轻化”的方式对抗衰老。
研究发现,T细胞的促衰老效应尤为显著。随着年龄增长,T细胞在大脑中的比例持续上升,并且广泛分布于所有区域。利用空间衰老时钟分析发现,T细胞对周围细胞(尤其是少突胶质细胞和血管周细胞)的邻近效应表现为强烈的“促衰老”作用,这种效应在老年小鼠中更加明显。具体而言,当T细胞靠近其他细胞时,这些邻近细胞的生物年龄会显著加速。研究进一步指出,这种促衰老效应可能与T细胞释放的促炎因子(如干扰素-γ,IFN-γ)有关,这些因子会引发周围细胞的炎症反应,从而加速其功能衰退。
与之形成鲜明对比的是,NSC展现了强大的促年轻化效应。作为位于侧脑室区域的关键修复细胞,NSC的存在能够通过释放神经生长因子和其他调节因子显著减缓邻近细胞的衰老。研究显示,这种“促进年轻化”的影响主要作用于少突胶质祖细胞(OPC)和血管周细胞,帮助它们维持健康状态,并在年轻小鼠中尤为显著。然而,随着年龄增长,NSC的数量逐渐减少,其促年轻化效应也随之减弱。
有趣的是,这种细胞间的“善”与“恶”效应并非单向的。例如,T细胞的促衰老效应范围广泛,可以通过炎症信号传播到更远距离,而NSC的促年轻化效应则局限于近距离范围。这提示了T细胞和NSC在衰老过程中的不同作用机制:前者通过扩散性炎症信号驱动全局性老化,而后者则通过局部因子保护邻近环境。
这些发现揭示了细胞间互动在大脑衰老中的重要性,也为未来开发以T细胞和NSC为靶点的抗衰老疗法提供了新方向。
基因的时空轨迹:衰老如何改变大脑的分子图谱
衰老不仅改变了大脑中细胞的构成,也在分子层面上引发了基因表达的深刻变化。这种变化随着时间和空间的推移不断累积,塑造了复杂的衰老分子图谱。该研究通过对小鼠大脑中300个关键基因的时空表达轨迹分析,揭示了免疫、代谢和修复相关基因在衰老过程中如何动态调控,为我们提供了全新的视角。
首先,研究发现,随着年龄增长,与免疫反应相关的基因显著上调,显示出炎症在大脑衰老中的核心作用。例如,小胶质细胞中负责免疫调节的 Pdcd1(程序性死亡受体1编码基因)在衰老过程中显著上升,其表达水平与年龄高度相关(Spearman相关系数ρ = 0.93)。这种变化可能反映了随着衰老,大脑内部的炎症反应逐渐增强。同时,与补体系统相关的基因 C3 也在衰老过程中强烈上调,进一步佐证了大脑炎症环境的加剧。
与此同时,与代谢和修复相关的基因则呈现出截然不同的轨迹。研究显示,在少突胶质细胞和神经干细胞中,参与抗氧化和DNA修复的关键基因 Cat(编码抗氧化酶催化酶)和 Bmp4(参与组织修复的信号因子)表达逐渐下降。这种“逐步减少”的轨迹表明,随着衰老,大脑的修复能力正在逐渐衰退,可能为细胞损伤和神经退行性病变的发生埋下隐患。
更重要的是,基因表达的变化并不均匀地分布于整个大脑,而是表现出显著的空间异质性。例如,干扰素响应基因 Stat1 在多个细胞类型中表现为“晚期增加”的轨迹,尤其是在白质区域(如胼胝体),这提示了白质可能是衰老的“热点”。而参与代谢途径的 Gamt 基因(与肌酸合成相关)则在神经元中表现为“逐步减少”,显示出神经元代谢功能的逐渐低下。
这些基因的时空轨迹为我们描绘了大脑衰老的动态分子图景,也提示了细胞和区域之间在衰老过程中的不同“命运”。研究还发现,这些基因表达变化与神经退行性疾病的通路存在显著重叠,进一步凸显了其生物学意义。
空间衰老时钟:解码细胞的生物年龄
在衰老研究中,精准量化细胞的生物年龄是理解衰老进程的关键。然而,传统方法往往局限于分子标记的线性分析,无法全面捕捉细胞在复杂组织环境中的老化状态。该研究突破性地提出了一种“空间衰老时钟”(spatial ageing clocks)的方法,通过结合空间转录组学和机器学习,为量化细胞衰老提供了一个强大的新工具。
“空间衰老时钟”基于小鼠大脑的高通量MERFISH数据,利用机器学习模型训练了多种细胞类型的基因表达特征与年龄的关联。研究团队通过创新性的“SpatialSmooth”方法,在每种细胞类型内构建了邻域图,逐步平滑空间邻近细胞的基因表达数据,从而既保留了空间信息,又显著提高了预测精度。结果表明,该方法在14种细胞类型中均表现出较高的预测性能,Pearson相关系数R值均超过0.7,包括T细胞、神经干细胞(NSC)等罕见细胞类型。
通过这些时钟,研究不仅能够量化每个细胞的生物年龄,还可以识别特定细胞类型的“加速衰老”或“延缓衰老”状态。例如,研究发现,小胶质细胞和T细胞在老年小鼠中表现出显著的“年龄加速”现象,提示它们在衰老过程中可能起到驱动作用。而神经干细胞则显示出生物年龄显著低于实际年龄的特性,进一步确认了其“促年轻化”潜力。
更为重要的是,空间衰老时钟为研究疾病和干预提供了一个前所未有的工具。通过将该时钟应用于阿尔茨海默病模型小鼠和炎症诱导的加速衰老模型,研究揭示了特定细胞类型(如少突胶质细胞和神经元)的生物年龄显著加速,尤其是在大脑白质区域。这种精细的时空分析能够帮助研究人员锁定疾病早期变化的细胞和区域,为精准治疗提供依据。
此外,空间衰老时钟还能评估干预效果。在运动和基因重编程实验中,该工具成功检测到某些细胞类型(如内皮细胞、血管周细胞)的生物年龄显著“年轻化”,为验证抗衰老措施的有效性提供了一个可量化的指标。
通过这项技术,研究人员不仅能够更全面地解读衰老的复杂过程,还能预测不同细胞类型的老化轨迹。
逆转时间:运动与基因重编程的抗衰老潜力
如果衰老是不可逆的,那么如何延缓甚至逆转大脑的衰老进程?在这一领域,运动和基因重编程作为两种广泛研究的干预方式,展现了独特的抗衰老潜力。该研究利用空间衰老时钟,首次系统性地评估了这些干预措施对不同细胞类型的影响,揭示了它们的作用机制与局限性。
运动的系统性抗衰老效应
研究发现,运动对多个细胞类型展现了强大的抗衰老作用,尤其是在血管相关的细胞中效果显著。例如,在老年小鼠中,运动使内皮细胞(endothelial cells)的生物年龄平均降低了4.9个月,血管周细胞(pericytes)和血管平滑肌细胞(vascular smooth muscle cells, VSMCs)的生物年龄分别降低了3.4个月和4.7个月。这些细胞类型分布在脑部多个区域,而运动对它们的年轻化作用广泛而强大,特别是在白质和皮层区域。这种现象可能与运动带来的全身循环改善和血管新生密切相关。研究还发现,运动对神经母细胞(neuroblasts)在部分区域(如胼胝体附近)也有明显的年轻化作用,可能是因为运动激活了局部的生长因子。
然而,运动的作用并非完全均匀。例如,在神经干细胞(NSCs)所在的侧脑室区域,运动未能显著延缓NSCs的生物年龄。这提示了运动可能更倾向于通过系统性因素(如血管修复)而非直接作用于神经干细胞发挥抗衰老作用。
基因重编程的选择性效果
与运动不同,基因重编程通过激活Yamanaka因子(Oct4、Sox2、Klf4、Myc,OSKM),直接作用于细胞内的分子调控,展现了细胞内在的年轻化潜力。研究显示,NSCs和神经母细胞在基因重编程干预后分别显著年轻化了2.7个月和2.8个月,尤其是在胼胝体区域的修复效果尤为显著。然而,这种干预效果更偏向于少数细胞类型,且其年轻化幅度普遍低于运动。此外,重编程还引发了某些细胞类型(如中型棘状神经元和小胶质细胞)的“提前老化”,提示这种方法可能伴随着副作用。
尽管运动和基因重编程在某些方面展现了显著效果,但两者均存在局限性。运动依赖全身性机制,对某些关键细胞类型(如NSCs)的直接影响有限;而基因重编程尽管靶向明确,却可能带来细胞功能失调或非预期老化。这些结果表明,单一干预可能难以覆盖所有衰老机制,未来或需结合多种方法,针对不同细胞类型制定个性化策略。
衰老干预的新希望
衰老的脚步不可阻挡,但它的影响可以被延缓,甚至部分逆转。该研究的发现,为探索大脑衰老的干预策略提供了崭新的科学依据,并为未来开发治疗神经退行性疾病的新型疗法指明了方向。
首先,研究揭示了不同细胞类型在衰老中的独特作用和动态变化。例如,T细胞的显著促衰老效应和神经干细胞(NSCs)的强大促年轻化能力,凸显了针对这些“关键角色”进行靶向干预的潜力。未来的治疗策略可以集中于抑制T细胞的促炎作用,例如通过调控干扰素-γ(IFN-γ)等炎症因子,减少其对周围细胞的促衰老影响。同时,激活或移植NSCs,也有望通过局部促年轻化效应,改善大脑的再生和修复能力。
其次,该研究的“空间衰老时钟”技术为精准治疗提供了全新工具。通过精确量化不同细胞类型的生物年龄,该工具能够帮助研究人员更早地发现特定区域和细胞的衰老迹象。例如,大脑白质区域在衰老过程中表现出基因表达和细胞功能的显著退化,这为早期诊断阿尔茨海默病等疾病提供了重要线索。未来,类似的技术还可以用于监测抗衰老干预的效果,为治疗方案的优化提供实时反馈。
此外,干预措施的组合应用可能是未来研究的重点。该研究表明,运动通过血管修复发挥了系统性抗衰老作用,而基因重编程则直接作用于细胞内部过程。将两者结合,或联合其他方法(如免疫调控或药物治疗),可以覆盖更多衰老机制,从而实现协同效应。例如,在衰老关键区域联合应用运动干预与NSC移植,可以同时改善局部微环境和细胞功能,进一步增强抗衰老效果。
最后,未来的研究将进一步探索衰老的根本机制,并推动精准治疗的发展。以MERFISH为代表的高通量空间转录组技术,结合人工智能和基因编辑技术,可能成为攻克衰老相关疾病的利器。这些技术将帮助我们更加全面地理解衰老的动态网络,从单一细胞到复杂组织层面提供多维度的解决方案。
衰老研究已经进入了一个全新的时代。从针对性靶向治疗到综合性干预策略,这些进步为延缓大脑衰老带来了前所未有的希望。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


