《细胞》子刊:“小恶魔”大起底!小细胞肺癌究竟为何如此凶残?
来源:奇点糕 2021-11-19 13:36
小细胞肺癌(SCLC)是肺癌中恶性程度最高的类型,占所有肺癌病例的15%,其增殖速度快并且预后极差,早期患者的五年生存率为15%-30%,而晚期患者则不到1%[1]。对于延长患者的生存期,在一线化疗中加入免疫治疗带来的效果很有限[2]。究其原因,还是科学家们对SCLC异质性特征及其背后涉及的分子通路了解的不多。想要知道的更多?那自然是像我们看图片
小细胞肺癌(SCLC)是肺癌中恶性程度最高的类型,占所有肺癌病例的15%,其增殖速度快并且预后极差,早期患者的五年生存率为15%-30%,而晚期患者则不到1%[1]。
对于延长患者的生存期,在一线化疗中加入免疫治疗带来的效果很有限[2]。究其原因,还是科学家们对SCLC异质性特征及其背后涉及的分子通路了解的不多。
想要知道的更多?那自然是像我们看图片一样——需要更高分辨率的数据。
近日,由纪念斯隆凯特琳癌症中心的Dana Pe’er和Charles M. Rudin领衔的研究团队在Cancer Cell期刊发表重要研究成果[3]。
他们对来自49个肺癌相关的组织样本的155098个细胞进行了单细胞测序(其中包括54523个SCLC细胞),发现了一个出现在多个亚型中的以PLCG2高表达为特征的SCLC细胞亚群,这些细胞有着干细胞样和高转移潜力的特征,并且与更差的预后有关,对于临床治疗具有重大意义。
肺癌可分为小细胞肺癌和非小细胞肺癌(包括肺腺癌、肺鳞癌、肺腺鳞癌等),尽管在形态学上SCLC在患者间看起来并无二致,但大量的研究数据显示,SCLC可根据ASCL1、NEUROD1、POU2F3(SCLC-A、-N和-P型)以及YAP1这四个基因的差异表达分为不同的亚型[4]。
然而这样的分类带来了新的问题,这些亚型与肿瘤分期、转移潜力和免疫微环境的关系仍然未知。
为了深入探究这些问题,Pe’er和Rudin团队对来自49个样本(21个SCLC、24个LUAD以及4个癌旁组织)的155098个细胞(54523个SCLC细胞)进行了单细胞测序。SCLC和LUAD队列都包括接受过治疗和无治疗史患者,同时所取的样本也包括转移和原位组织。
与LUAD相比,SCLC的拷贝数变异数量更多,并且SCLC在患者间的异质性也更大,甚至在没有接受过治疗的患者中也是这样。
接着,研究人员利用邻接图的方法对54523个SCLC细胞重新进行了亚型无监督聚类。基于之前报道的四个基因ASCL1、NEUROD1、POU2F3和YAP1,可以分成三类,分别是SCLC-A、SCLC-N、SCLC-P。但事实上还有一类研究人员认为属于TP53型。
由于YAP1表达量较低,所以没有发现SCLC-Y,这个分析结果得到了各类间标志基因表达量差异验证。
在重现了已有结论后,Dana Pe’er和Charles M. Rudin团队开始探究SCLC各种亚型与肿瘤发展的关系。由于他们的数据里只有一个样本属于SCLC-P型,因此接下来的分析便集中于SCLC-A和-N型。
与已有研究一致的是,他们发现SCLC-A大多是原位肿瘤,而SCLC-N则大部分是转移瘤,并且SCLC-N的患者间异质性要比SCLC-A大得多。这些证据支持了临床前模型中SCLC-N可以由SCLC-A进化而来的现象[5]。
在差异表达和通路分析中,他们发现SCLC-A中上调的是调控细胞周期发展的基因,而SCLC-N则呈现出促进肿瘤转移的基因表达模式,这表明SCLC-N与肿瘤的转移有关。
由此可见SCLC的各亚型的转录组之间存在很大的差异,这与SCLC患者大都有着较差的预后形成反差。研究人员猜测在大部分患者的肿瘤中应该存在一种与不良预后相关的细胞亚群,才能解释这样的反差。
他们利用SCLC细胞的单细胞数据进行了聚类分析,共得到25个不同的细胞亚群,大部分亚群都只存在于单一的肿瘤样本中,但是22号亚群却在许多肿瘤样本中都存在,并且有着最高的亚型不确定性,表明22号亚群细胞有干细胞特征。
果然,基因富集分析发现22号亚群中的细胞中上调了与肿瘤转移和神经干细胞相关的基因。这些上调的基因中,差异最大的基因是PLCG2,研究人员认为它可能是促进肿瘤转移的驱动基因。
与设想一致的是,和肺部的原位瘤相比,转移瘤中的PLCG2表达量更高,并且在肝转移瘤中的表达量最高,这是SCLC最常见的转移部位。
为了得到更有力的证据,研究人员接着做了体外培养和小鼠实验。在体外培养实验中,他们分别在PLCG2低表达的细胞系(SHP-77)中过表达PLCG2,以及在PLCG2高表达的细胞系(H526)中敲除PLCG2,之后又将这两种处理过的细胞系移植到小鼠体内。
实验结果表明,在体外PLCG2的表达赋予了细胞更强的迁移能力和侵袭性;而在小鼠体内,PLCG2的表达同样使得肿瘤细胞有更强的转移潜力。
这些结果表明PLCG2很有可能是促进肿瘤转移的驱动基因。回到最开始的问题,在大多数患者中存在的PLCG2高表达22号细胞亚群是否与更差的预后有关呢?
研究人员在一个独立的SCLC队列中发现:患者肿瘤组织中表达PLCG2的细胞比例与总生存期呈负相关(r=-0.34,p=0.04)。这个队列的生存分析也发现:表达PLCG2的细胞比例较高的患者总生存期更短。
但是PLCG2高表达毕竟只是22号亚群细胞的一个特征,更进一步的分析表明:患者肿瘤组织中22号亚群细胞的比例与总生存期呈更强的负相关(r=-0.65,p=0.009),生存分析的结果也是一致的。研究人员据此认为有干细胞样、强转移能力并且高表达PLCG2的22号亚群细胞,对SCLC患者的预后有较大的影响。
Dana Pe’er和Charles M. Rudin团队接着研究了SCLC其他的一些特征。
一直以来,SCLC被认为是一种免疫“冷”肿瘤(缺乏免疫细胞),因此免疫治疗的效果很有限。但最近的研究认为SCLC的免疫微环境存在亚型之间的异质性。
研究人员利用流式细胞术在他们的样本以及一个独立队列中发现:不论是SCLC-N还是SCLC-A中的免疫细胞(CD45+)数量都比LUAD少,并且SCLC-N的更少。
然后他们利用MIBI(多路离子束成像)技术得到了每个肿瘤样本中的免疫细胞在空间中的分布,并且根据在800800范围内免疫细胞的数量将肿瘤分成了“冷”、“热”(免疫细胞数量>250)肿瘤。结果发现大部分的SCLC样本都属于“冷”肿瘤,并且SCLC-N型更为明显。
SCLC各亚型间免疫微环境总体的差异分析完,研究人员接着探究了T细胞在亚型间的差异。他们利用非负矩阵分解方法将他们SCLC样本中的免疫细胞分成30类,其中7类对应的是不同类型的T细胞。经过对比发现,SCLC-N有更多的Treg和耗竭CD8+ T细胞,SCLC-A则有更多的效应CD8+ T细胞和Tgd。
并且SCLC-N中效应CD8+ T细胞与Treg数量的比值更低,后续的成像技术分析得到了一致的结果,有研究证明这个比值更低在多种癌症中意味着更差的预后[6]。
最后,研究人员分析了SCLC样本中髓样细胞的特征。他们对SCLC样本中的髓样细胞根据单细胞测序数据进行了重聚类,产生了7种单核/巨噬细胞(Mono/M)、4种中性粒细胞、2种树突状细胞。
随后,由于功能的相似性,他们将7种Mono/M细胞亚群与特发性肺纤维化(IPF)患者的髓样细胞进行比较,发现Mono/M1与IPF相关的髓样细胞基因表达特征最相似。
在结合了LAUD和肺部正常组织中的髓样细胞后,研究人员对三种样本中的髓样细胞再次进行了聚类,他们发现与IPF类似的Mono/M细胞在SCLC中的比例更高,甚至在未经治疗的样本中也是一样。
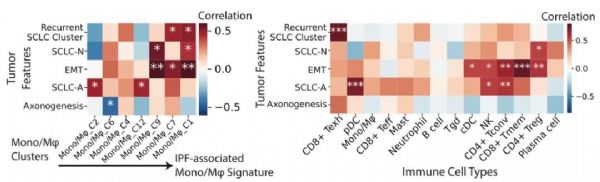
于是,研究人员猜测这类纤维化的Mono/M细胞可能通过与特定的SCLC细胞亚群互作来促进肿瘤发展。他们发现SCLC-A与Mono/M2和12显着相关,而SCLC-N则与Mono/M1和9相关,并且之前讨论过的22号细胞亚群与Mono/M1和7显着相关。
这就再次回到了22号细胞亚群,研究人员又分析了它与非髓样免疫细胞亚群的关系,发现它与耗竭CD8+T细胞有显着关联。后续的成像分析证明了这些结论。
最终,Dana Pe’er和Charles M. Rudin团队认为:22号细胞亚群可能存在于以耗竭CD8+T细胞,以及纤维化的Mono/M细胞为特征的免疫微环境中。(生物谷Bioon.com)
小编推荐会议 2021 (第四届)单细胞多组学研究与临床应用峰会
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。