研究发现肥胖的潜在治疗新靶点
来源:上海药物所 2023-06-05 10:47
肝脏作为生物体脂代谢的中心枢纽,主要依赖于其所分泌的肝因子,实现与其他组织器官之间的信号流通和调控反馈,尤其是在能量代谢过程中扮演着重要角色。
肝脏作为生物体脂代谢的中心枢纽,主要依赖于其所分泌的肝因子,实现与其他组织器官之间的信号流通和调控反馈,尤其是在能量代谢过程中扮演着重要角色。然而,肝内脂代谢的调节机制与肝因子表达分泌调控尚未被完全阐明。葡萄糖醛酸C5异构酶 (Glucuronyl C5-epimerase ,Glce) 作为细胞膜上广泛存在的硫酸乙酰肝素蛋白聚糖(HSPG)糖链合成修饰的重要异构化酶,基因高度保守,但是否参与肥胖症的发生发展及其调控机制尚不清楚。
中国科学院上海药物研究所研究员丁侃团队/李佳团队联合复旦华山医院教授花荣团队,在《肝脏病学杂志》(Journal of Hepatology)上,发表了题为Hepatic glucuronyl C5-epimerase combats obesity by stabilizing GDF15的研究成果,报道了肝脏Glce介导GDF15的分泌影响机体肝脂代谢的稳态平衡。
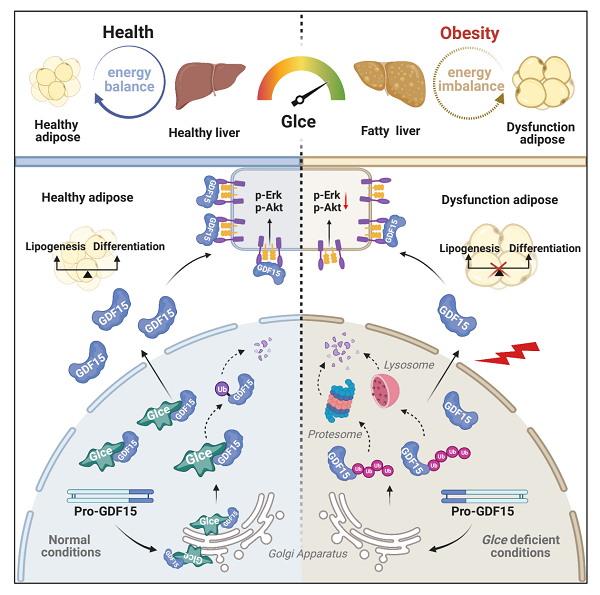
研究团队通过比较具有不同身体质量指数(BMI)值的肥胖患者肝脏中Glce的表达发现其与BMI值和HOME-IR等代谢指数呈负相关。同时,肝脏特异性敲除Glce小鼠模型体内实验表明,Glce敲除后棕色脂肪组织产热功能受损,白色脂肪组织分化程度增加,小鼠血糖耐受能力与胰岛素敏感性均显著下降,血清总胆固醇和甘油三酯含量升高,加剧了高脂饮食诱导的脂代谢紊乱。研究进一步结合分泌组学分析发现,在Glce敲低或敲除小鼠肝细胞培养基中,生长分化因子15 (Growth differentiation factor-15,GDF15) 水平降低,体内GDF15蛋白回补可减缓肝脏Glce缺失引发的肥胖和肝损伤表型,而Glce或其酶活突变体在体内过表达也能削弱高脂饮食诱导下小鼠体重增长、脂肪过度分化和肝损伤进程。机制上,研究发现,Glce过表达可促进GDF15前体形式向成熟形式转化,且Glce沉默可减少GDF15的生成,同时进一步促进GDF15蛋白上K48和K63连接形式的泛素化增加。上述研究表明,肝脏中Glce可通过影响GDF15蛋白的分泌,维持机体能量代谢稳态。
该研究揭示了新的代谢调控分子Glce介导肝脏-脂肪“cross-talk”信号传导调节能量稳态的重要作用,并加深了科学家对人体肝脏中Glce与肥胖或NAFLD/NASH等代谢综合性疾病相关性的认知,提示了Glce及其介导的GDF15信号通路或可成为对抗肥胖的潜在靶点。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


