Journal Of Experimental Medicine:红细胞和裂殖子表面新表征的疟疾抗原可诱导寄生虫抑制抗体
来源:生物谷 2021-08-27 17:10
尽管在流行地区进行了数十年的密集公共卫生干预,但恶性疟原虫(Pf)每年仍夺走超过四十万条生命,全球抗击疟疾的努力遇到了对一线抗疟药物和杀虫剂迅速出现的耐药性。
尽管在流行地区进行了数十年的密集公共卫生干预,但恶性疟原虫(Pf)每年仍夺走超过四十万条生命,全球抗击疟疾的努力遇到了对一线抗疟药物和杀虫剂迅速出现的耐药性。一个新兴的共识是,下一代亚单位疫苗需要结合来自不同生命周期阶段的多种保守抗原,以实现和维持针对疟疾的高效菌株跨越、灭菌和传播阻断免疫。
研究者之前使用来自纵向出生队列中耐药或易感的2岁坦桑尼亚儿童的血浆对血液期Pf3D7菌株cDNA Lambda Zap文库(MR4)进行全蛋白质组差异筛选,在坦桑尼亚耐药而非易感儿童的血浆中发现了PF3D7_1134300,这是一个可能由11号染色体上的一个基因编码的蛋白。该蛋白的生物信息学分析预测了一个6684 bp的单拷贝基因,在迄今为止研究的所有人类(Pf、间日疟原虫、卵形疟原虫、疟疾疟原虫和诺氏疟原虫)和非人类灵长类动物、啮齿动物和禽疟寄生虫中都有同位同源。
图片来源:https://doi.org/10.1084/jem.20200170
该研究证明了由PF3D7_1134300编码的蛋白质在寄生液泡(PV)之外输出到红细胞质膜的外表面,并且也在裂殖子的表面表达。基于其独特的双表面定位,将该蛋白质命名为Pf红细胞膜和裂殖子抗原1(PfEMMA1),并将相应的基因命名为PfEMMA1。研究者展示了小鼠抗PfEMMA1超免疫Ig和人类亲和纯化的抗PfEMMA1抗体在体外限制寄生虫的生长。此外,源自PfEMMA1的伯氏疟原虫(Pb)直系同源物的基于重组蛋白的疫苗具有免疫原性,可以在已建立的均致死性严重疟疾小鼠模型中介导自我治愈或延长生存期。在坦桑尼亚儿童的纵向队列中,高水平的自然获得的人类抗PfEMMA1抗体与显著降低的寄生虫密度有关,这些发现支持研究者的假设,即针对新型疟疾表面抗原PfEMMA1的抗体介导了对疟疾的保护。
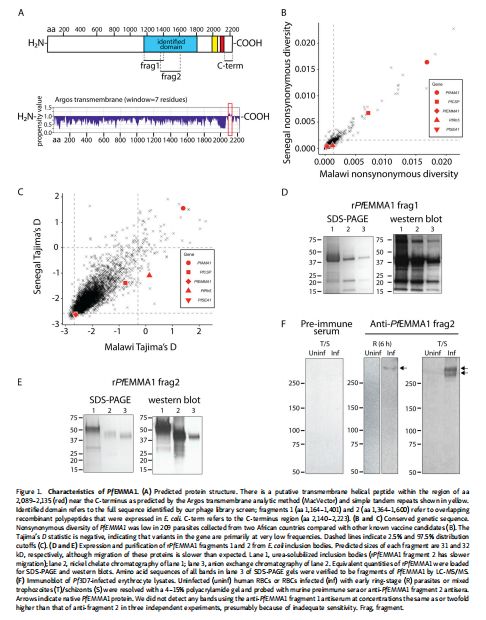
PfEMMA1的特性 图片来源:https://doi.org/10.1084/jem.20200170
PfEMMA1不编码疟原虫输出元件/宿主靶向信号(PEXEL/HT)结构域、信号肽或糖磷脂酰肌醇锚定序列,与许多其他PEXEL阴性蛋白不同,PfEMMA1不包含保守的N端序列,而在C端附近有一个预测的跨膜结构域,对应于疏水区域和α-螺旋结构。PfEMMA1显示成对非同义核苷酸多样性的平均水平(πNS:3.6×10−4,塞内加尔第55个百分点;3.2×10−4,马拉维第52个百分点),这与恶性疟原虫环子孢子蛋白(PfCSP)和恶性疟原虫株裂殖子顶端膜抗原1(PfAMA1)中存在的高核苷酸多样性形成对比。此外,Tajima’s D(一种基于多样性的统计数据,可以检测选择和/或人口变化)在两个种群中的PfEMMA1值都很低(-2.64,塞内加尔第二个百分位;-2.62,马拉维第六个百分位)。研究者用两种密码子优化、重组表达和纯化的多肽免疫BALB/cJ小鼠(片段1和2;38-个氨基酸重叠),通过用鼠抗PfEMMA1片段2抗血清探测Pf3D7感染的红细胞的裂解物,证实PfEMMA1编码天然寄生虫蛋白;使用蛋白质印迹分析在早期环状寄生虫中检测到一条蛋白质带,在混合滋养体/裂殖体阶段寄生虫中检测到一条双蛋白质带;单(MW, 308 kD)和双(MW, 289 和 304 kD)带大小近似于未修饰的全长PfEMMA1的分子量(263 kD)。
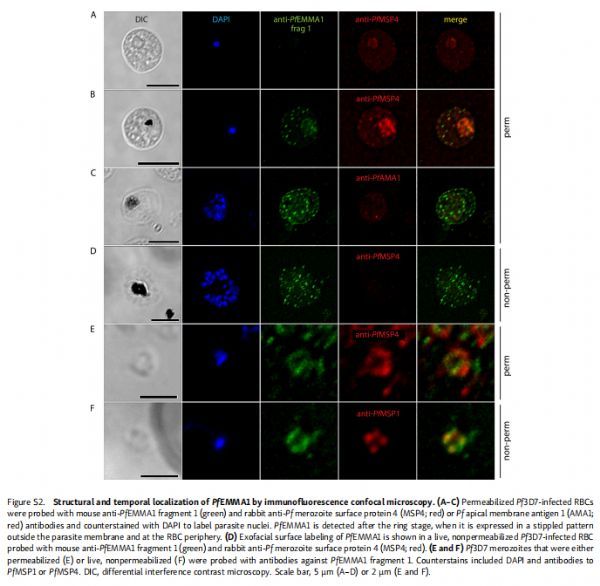
通过免疫荧光共聚焦显微镜对PfEMMA1的结构和时间定位 图片来源:https://doi.org/10.1084/jem.20200170
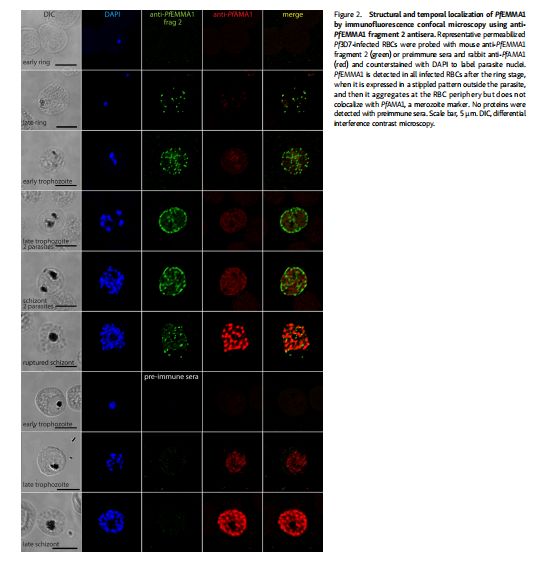
使用抗PfEMMA1片段2抗血清通过免疫荧光共聚焦显微镜对PfEMMA1的结构和时间定位
图片来源:https://doi.org/10.1084/jem.20200170
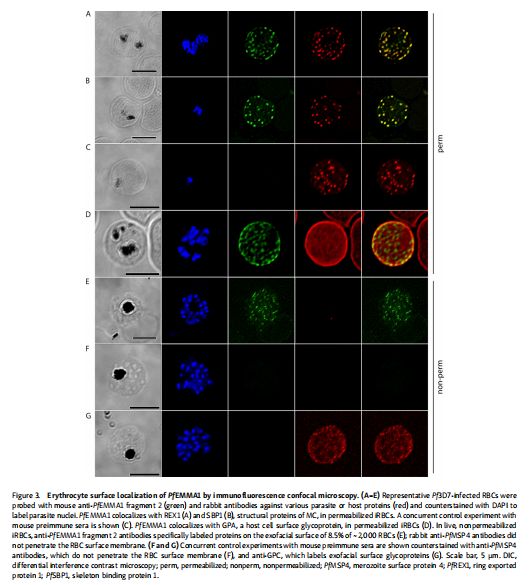
通过免疫荧光共聚焦显微镜对PfEMMA1的红细胞表面定位 图片来源:https://doi.org/10.1084/jem.20200170
为了确定PfEMMA1的细胞定位,研究者使用抗PfEMMA1片段1和片段2的抗血清对透化恶性疟原虫感染的红细胞(iRBC)进行免疫荧光(IF)共聚焦显微镜检查,并表明PfEMMA1与使用特异性识别细胞内血型糖蛋白A(GPA)表位的抗GPA抗体检测到的GPA密切相关;为了确定PfEMMA1是否暴露在红细胞质膜的外表面,使用了抗PfEMMA1 片段1和片段2抗体探测活的、非透化的、裂殖体感染的红细胞,观察到使用免疫前血清未检测到的抗PfEMMA1抗体的弥漫性斑点染色模式;恶性疟原虫裂殖子表面蛋白4(PfMSP4)和血型糖蛋白C (GPC)抗体复染证实红细胞质膜是不可渗透的,表明天然PfEMMA1暴露在受感染红细胞的外表面。
PfEMMA1是一种新型的、保守的血液阶段疟疾蛋白,在iRBC和裂殖子的表面都有表达。因此,针对PfEMMA1的抗体可能针对寄生虫发展的时间和阶段分开的两个脆弱部位,未来的研究将需要描绘PfEMMA1的精确功能,包括其在红细胞侵袭、细胞粘附和免疫调节中的潜在作用。PfEMMA1的免疫抑制可以提供针对导致人类疟疾的最危险物种的新治疗选择。(生物谷 bioon)
参考文献
Ian C. Michelow et al. A newly characterized malaria antigen on erythrocyte and merozoite surfaces induces parasite inhibitory antibodies. JOURNAL OF EXPERIMENTAL MEDICINE (2021 Aug 03) doi:https://doi.org/10.1084/jem.20200170
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。