Cell Systems:新研究表明BRAF抑制剂与SFK抑制剂组合使用有望更有效治疗黑色素瘤
来源:生物谷原创 2025-03-28 11:57
这项研究的一个关键发现是,该团队将SFK活化与活性氧(ROS)联系起来,活性氧是在BRAF抑制下形成的细胞应激反应。随着活性氧水平的飙升,SFK活性飙升,帮助黑色素瘤细胞耐受治疗。
在一项新的研究中,由系统生物学研究所(ISB)和麻省理工学院(MIT)的研究人员领导的一个研究团队发现了黑色素瘤细胞用来逃避靶向治疗的一种隐形生存策略,为改善治疗结果提供了一种有前景的新方法。相关研究结果发表在Cell Systems杂志上。

该团队确定了一种非遗传、可逆的适应机制,使黑色素瘤细胞能够在BRAF抑制剂治疗下存活。通过识别和阻断这种早期反应,他们提出了一种联合疗法,可以延缓耐药性并提高现有治疗的有效性。
破解黑色素瘤的药物逃逸密码
黑色素瘤是一种最致命的皮肤癌,通常是由BRAF基因突变引起的,这是因为BRAF基因的突变会导致肿瘤生长失控。虽然BRAF抑制剂(如vemurafenib)最初会阻止肿瘤生长,但许多肿瘤会迅速适应并存活下来,导致治疗失败。
与由基因突变驱动的传统耐药性不同,这项研究揭示了一个早期的动态适应过程,该过程发生在药物治疗后的几小时到几天内,远在遗传耐药性形成之前。令人惊讶的是,这一过程并不依赖于重新激活BRAF-ERK通路,这是常见的耐药机制。
该团队使用基于前沿质谱的磷酸蛋白质组学和深度转录组学分析,绘制了BRAF抑制剂治疗几分钟、几小时和几天内黑色素瘤细胞的分子变化图。
论文共同第一作者、系统生物学研究所生物信息学科学家Chunmei Liu博士说,“我们发现,虽然BRAF-ERK信号通路被迅速而持久地抑制,但癌细胞并不依赖于ERK的重新激活来生存。相反,它们触发了另一个替代性的SRC家族激酶(SFK)信号通路,这促进了癌细胞生存和最终复发。”
把弱点变成靶标
这项研究的一个关键发现是,该团队将SFK活化与活性氧(ROS)联系起来,活性氧是在BRAF抑制下形成的细胞应激反应。随着活性氧水平的飙升,SFK活性飙升,帮助黑色素瘤细胞耐受治疗。然而,这种适应是可逆的——当治疗被取消时,癌细胞恢复到原来的状态。
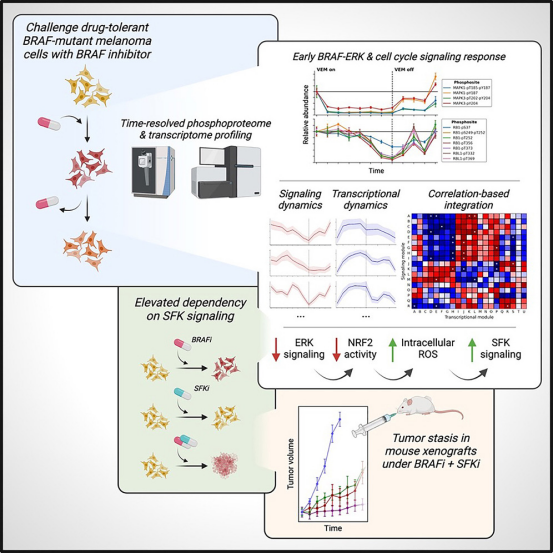
在认识到这一致命弱点之后,该团队测试了一种组合方法:将BRAF抑制剂与SFK抑制剂达沙替尼(dasatinib)组合使用。
论文共同通讯作者、系统生物学研究所副教授Wei Wei博士说,“通过添加达沙替尼,我们阻断了这种适应性逃逸机制,显著降低了黑色素瘤细胞的存活率,并稳定了动物模型中的肿瘤。”
重要的是,单独抑制SFK对黑色素瘤细胞几乎没有影响,这突显了在耐药性完全形成之前,需要一种战略性的联合治疗来抑制黑色素瘤的适应。论文共同通讯作者Jim Heath教授博士说,“这种方法有可能延长BRAF抑制剂的有效性并改善患者的预后。”
展望未来
除了揭示药物适应的关键机制外,这项研究还强调了早期干预以防止其发生的重要性。它还强调了ROS积累和SFK激活作为识别可能受益于这种联合治疗的患者的潜在生物标志物。
还需要开展进一步的临床前研究和临床试验来验证这种联合治疗策略,并确定其更广泛的临床应用潜力。(生物谷 Bioon.com)
参考资料:
Qianwen Wang et al, Signaling and transcriptional dynamics underlying early adaptation to oncogenic BRAF inhibition, Cell Systems (2025). DOI: 10.1016/j.cels.2025.101239.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


