Nat Commun:负载可电离脂质纳米颗粒iLAND的mRNA药物在高尿酸血症治疗和相关疾病预防方面显示出巨大的潜力
来源:生物谷原创 2024-08-26 13:45
本研究通过采用返祖策略,设计表达Uox的mRNA,并将其装载到基于A1-D1-5的可电离脂质的LNP递送系统中。
高尿酸血症(HU)是一种代谢疾病,由肾脏排泄不足、产生过多或肠道排泄不足引起的血清尿酸(SUA)水平过高引起。处理较高水平的SUA可能有助于管理、预防和治疗这些临床状况。由于编码尿酸氧化酶(Uox)基因的突变,尿酸(UA)在一些哺乳动物中,特别是在人类中,成为嘌呤代谢的酶促最终产物。在参与尿酸代谢的酶序列中,Uox是第一个将尿酸代谢成尿囊素的酶。
各种常规治疗方式通常用于治疗HU,如丙戊酸(尿酸)和别嘌呤醇(黄嘌呤氧化酶抑制剂)。丙戊酸增加排尿,从而增强尿酸盐晶体的排泄,而别嘌呤醇通过抑制黄嘌呤氧化酶减少尿酸的产生来缓解症状,然而,排尿增多会增加尿酸盐晶体的排泄,从而导致肾脏损伤。
同时,UA的产生减少可能引起低尿酸血症,从而干扰机体的正常代谢功能。同样,重组聚乙二醇化的哺乳动物尿酸酶(pegloticase)也被广泛用于酶解UA为尿囊素,然而,pegloticase具有免疫原性的缺点,它也产生抗pegloticase抗体,增加药物清除率、疗效损失和输液反应。此外,临床经验表明,使用pegloticase治疗的患者更容易发生痛风发作。
蛋白质和酶替代疗法通过核酸(mRNA, DNA等)或直接蛋白质递送进行,然而,与蛋白质治疗相比,mrna介导的蛋白质表达替代治疗性蛋白质有几个潜在的优势。mRNA的传递促进了细胞质中短暂的蛋白质表达,从而绕过核入口并限制了基因组的整合。mRNA既不是最终产物,也不是遗传信息,mRNA是一个快速的转变,因此,这为治疗性mRNA提供了很大的灵活性,以扩大其应用范围。
然而,由于mRNA的不稳定性和细胞内内化的剥夺,mRNA的快速降解限制了mRNA治疗药物的临床应用。由于存在载体整合异常的风险,使用病毒载体传递mRNA可能会调节转基因表达。因此,非病毒mRNA传递方法允许瞬时蛋白表达,以避免与病毒载体相关的基因组整合风险。
为了解决这个问题,可电离脂质或类脂质可以与mrna形成不同的递送平台,如脂质纳米颗粒(LNP)和脂质体。已经报道了几种可电离脂质和阳离子脂质用于核酸递送。由于核心成分的存在,可电离LNPs在生物液体中是中性的,而在低ph的内体酸性环境中变为阳离子。与Lipofectamine 2000相比,这种转变导致质子海绵状效应,因为胺基的存在破坏了膜,导致细胞内mRNA内体/溶酶体逃逸,这些特点使电离LNP成为一个更强大的核酸传递平台。

图片来源:https://doi.org/10.1038/s41467-024-50752-9
近日,来自北京理工大学生命科学学院的研究者们在Nat Commun杂志上发表了题为“Atavistic strategy for the treatment of hyperuricemia via ionizable liposomal mRNA”的文章,该研究制备出负载可电离脂质纳米颗粒iLAND的mRNA (mUox),该mRNA药物在高尿酸血症治疗和相关疾病预防方面显示出巨大的潜力。
高尿酸血症与痛风、高血压、糖尿病和心血管疾病的风险增加有关。大多数哺乳动物通过尿酸氧化酶(Uox)维持正常的血清尿酸(SUA),这种酶将难溶性尿酸代谢为高溶性尿囊素。相反,Uox在漫长的进化过程中成为人类和猿类的假基因。
在这里,研究者展示了一种治疗高尿酸血症的返祖策略,该策略基于肝细胞中Uox的内源性表达。研究者将表达Uox (mUox)的mRNA包封在可电离LNP中,LNP由热稳定的可电离脂质A1-D1-5 (N1, n4 -二(2-羟基十二烷基)氨基)丙基)琥珀酰,,DOPE(1,2-二油基- asn -甘油-3-磷酸乙醇胺),CHO(胆固醇)和DMG-PEG2000(1,2-二肉豆醇-乙酰甘油-3-甲氧基聚乙二醇-2000)组成。优化后的LNP被称为可电离脂质辅助核酸传递系统(iLAND)。iLAND包封mUox形成mUox@iLAND,用于转染Hepa1-6细胞表达Uox。
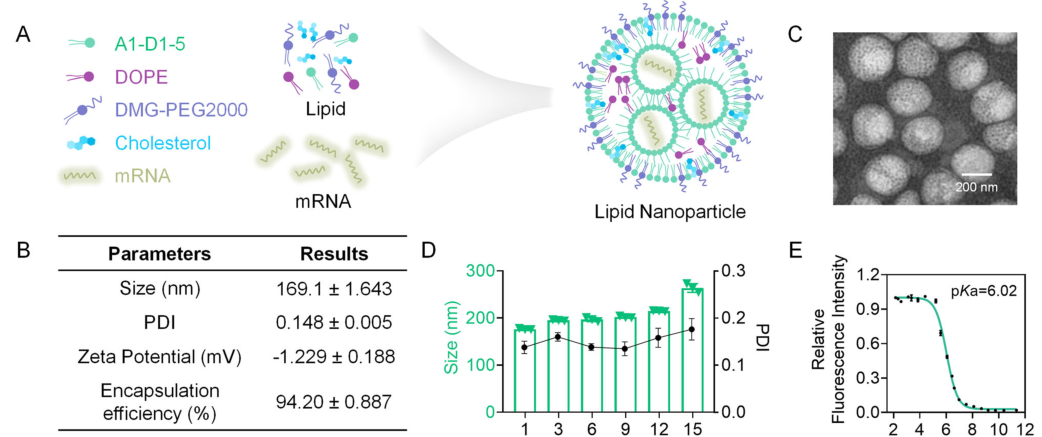
mUox@iLAND的物理化学特性和细胞进入
图片来源:https://doi.org/10.1038/s41467-024-50752-9
研究者将mUox@iLAND静脉注射HU小鼠,观察其生物分布、Uox表达及抗HU效果。结果证明mUox@iLAND给药后在肝脏内有效蓄积,并长期停留,有效降低UA水平。最后,研究者在两种不同的HU小鼠模型中展示了mUox@iLAND的治疗潜力,其中一种是内部开发的持久小鼠模型,结果显示mUox@iLAND成功地将mUox运送到肝脏,降低了高水平的SUA,提高了尿囊素的水平。
因此,该研究实现了一种有效的制剂,可以潜在地用于建立基于mrna的蛋白质或酶表达疗法。结果表明,iLAND建立了mRNA传递的有效平台,而mUox@iLAND则具有治疗高尿酸血症和预防相关疾病的前瞻性治疗潜力。
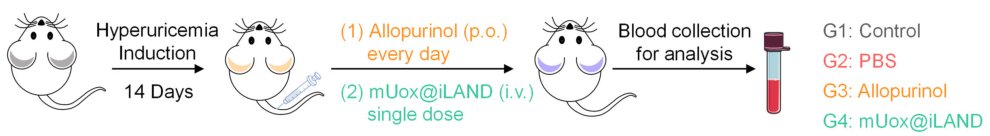
mUox@iLAND治疗高尿酸血症过程示意图
图片来源:https://doi.org/10.1038/s41467-024-50752-9
综上所述,本研究通过采用返祖策略,设计表达Uox的mRNA,并将其装载到基于A1-D1-5的可电离脂质的LNP递送系统中。在两种啮齿类动物模型中观察到有效和持久的降低SUA,以及理想的安全性,其中一种是内部建立的。该研究为高尿酸血症的治疗提供了一种有希望的基于mrna的治疗方案。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


