Cell重磅:复旦团队利用AI技术,从全球微生物中一性发现近百万种候选抗生素
来源:生物世界 2024-06-12 09:15
这项研究证明了人工智能方法从全球微生物组中鉴定功能性抗菌肽的能力,为抗生素开发者提供了多种新线索,并标志着一个充满希望的抗生素发现新时代的开始。
复旦大学类脑智能科学与技术研究院与美国宾夕法尼亚大学的研究人员合作,在国际顶尖学术期刊 Cell 上发表了题为:Discovery of antimicrobial peptides in the global microbiome with machine learning 的研究论文。
该研究提出了一种基于机器学习(Machine Learning)的方法,用于预测全球微生物群中的抗菌肽(AMP),利用来自环境和宿主相关栖息地的63410个宏基因组和87920个原核基因组的大量数据集,识别并创建了一个包含近100万种候选抗菌肽序列库——AMPSphere,研究团队还免费公开了这个抗菌肽序列库。
为了验证预测结果,研究团队从中合成了100中抗菌肽,并在体外和体内实验中验证了其对抗临床相关耐药病原体和人体肠道细菌的的活性,结果显示,其中有79中抗菌肽有活性,有63种能够特异性地完全抑制一种病原体的生长,这些活性抗菌肽通过破坏细菌膜发挥抗细菌活性。这项研究证明了人工智能方法从全球微生物组中鉴定功能性抗菌肽的能力。

近年来开发的基于人工智能的计算方法能够加快我们识别新型抗生素的能力,包括抗菌肽(AMP)。而最近,甚至有研究利用机器学习和蛋白质组挖掘方法在已灭绝生物中识别出了抗菌肽,进一步扩展了我们已知的抗菌药物库。
抗菌肽(AMP)在自然界的生命中普遍存在,通常是10-100个氨基酸长度的多肽,能够干扰微生物的生长,其最常见的作用是破坏细菌细胞壁的完整性并导致细胞破裂。天然抗菌肽可以通过蛋白酶解或非核糖体合成产生,当然,它们可以编码在基因组中。
细菌在自然环境中处于一种微妙的平衡状态,既相互对抗又相互依存。抗菌肽在调节这种微生物相互作用方面发挥着重要作用,既可以排斥竞争菌株,又可以促进合作。例如,沙门氏菌属、金黄色葡萄球菌属、霍乱弧菌和李斯特菌属等病原体会产生抗菌肽以清除竞争对手(甚至是自己同类),从而使它们能够占据自己的生态位。
抗菌素具有成为潜在治疗药物的潜力,并且已有一些抗菌素作为抗病毒药物在临床上使用,还有一些具有免疫调节特性的抗菌肽正在进行临床试验,用于治疗酵母菌和细菌感染。虽然大多数抗菌肽具有广谱活性,但也有一些只对同一物种或同属近亲有活性,与传统广谱抗生素相比,这些抗菌肽是更具针对性的药物。此外,与传统抗生素不同,许多抗菌肽的耐药性进化速度较慢,并且与对其他广泛使用的抗生素类的交叉耐药性无关。
由于技术限制,宏基因组分析在抗菌肽研究中的应用受到限制,主要源于难以区分真正的蛋白质编码序列与假阳性序列。因此,在基因组分析或宏基因组分析中,小型开放阅读框(smORF)的重要性长期被忽视。
近年来,在与人类相关的smORF的宏基因组分析方面取得了重大进展。这些进展采用了机器学习(Machine Learning,ML)技术来识别属于特定功能类别的smOR编码的蛋白质。例如,2022年3月,中国科学院微生物研究所王军团队在 Nature Biotechnology 期刊发表论文,利用预测的smORF从人类肠道微生物组的宏基因组样本中发现了超过2000种候选抗菌肽,这项研究展示了机器学习方法从宏基因组数据中挖掘功能肽并加速发现有希望的候选抗菌肽以供深入研究的潜力。
值得注意的是,人类肠道微生物仅代表微生物多样性的一部分,这表明在全球范围内的多样化栖息地中,从原核生物中发现抗菌肽仍有巨大潜力。
在这项最新研究中,研究团队利用机器学习(Machine Learning)技术预测并整理编目了公共数据库中的全球微生物组的抗菌肽。通过对63410个公开可用的宏基因组和87920个高质量微生物基因组进行计算分析,研究团队发现了大量抗菌素多样性,进而创建了AMPSphere,这是一个包含863498个非冗余肽序列的集合,其中包括从宏基因组数据中提取的候选抗菌肽(c_AMP)。令人惊讶的是,这些c_AMP序列中的大多数此前尚未被描述过。分析显示,这些c_AMP仅存在于特定的栖息地,并且在泛基因组中并非核心基因。
此外,研究团队从AMPSphere中选择合成了100种候选抗菌素(c_AMP),发现其中79种具有抗菌活性,其中63种在体外对临床上重要的ESKAPEE病原体具有抗菌活性,这些病原体是当前重要的耐药菌,分别是屎肠球菌(E)、金黄色葡萄球菌(S)、肺炎克雷伯菌(K)、鲍曼不动杆菌(A)、铜绿假单胞菌(P)、肠杆菌(E)、大肠埃希菌(E)。
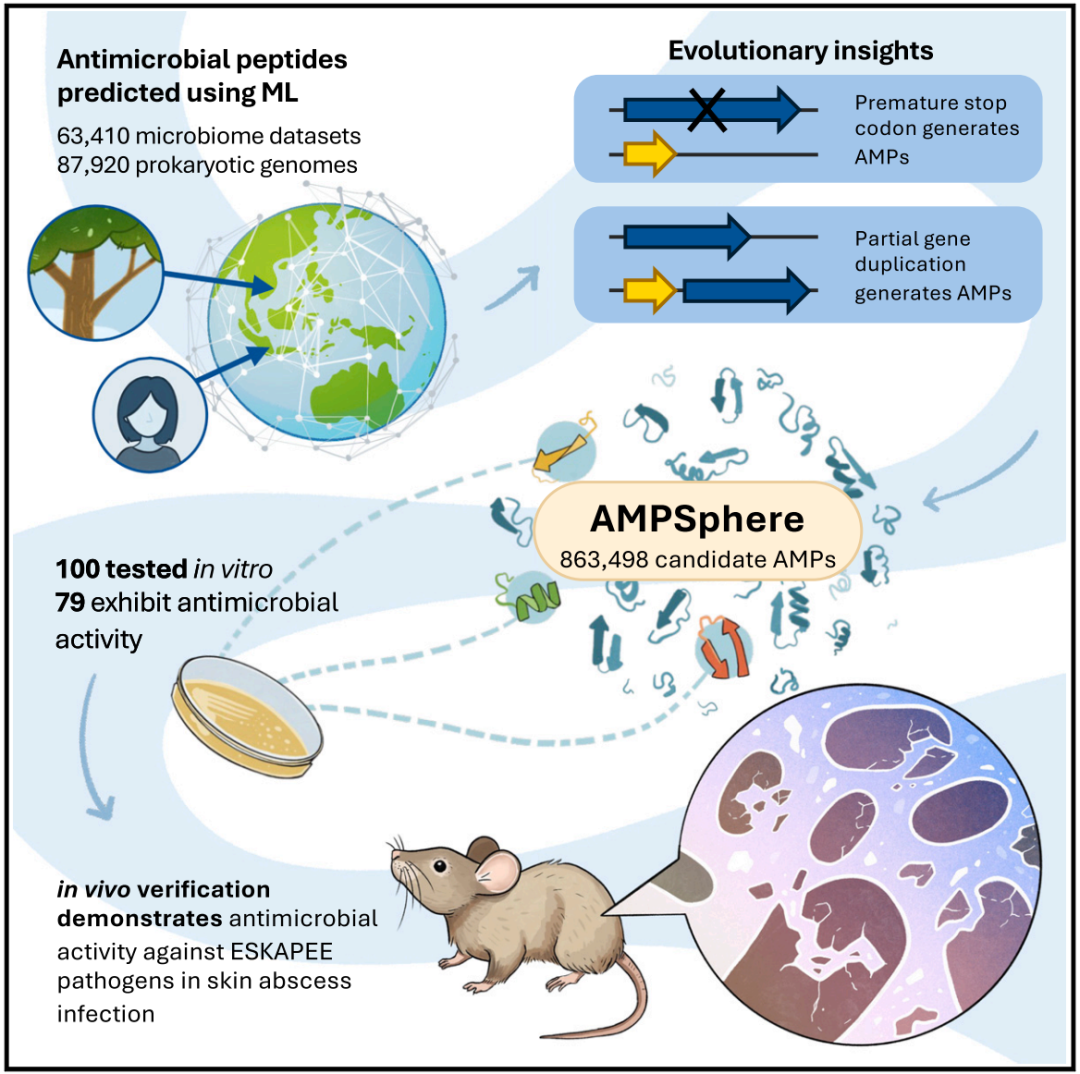
研究团队进一步将这些抗菌肽与加密肽(Encrypted Peptides)进行了比较(加密肽是隐藏在蛋白质序列中的肽序列,通过计算挖掘得到),证明了这些抗菌肽靶向细菌膜的能力,以及它们倾向于采用α-螺旋和β-结构。值得注意的是,其中主要的候选抗菌肽在临床前动物模型中也显示出很有前景的抗感染活性。
总的来说,这项研究证明了人工智能方法从全球微生物组中鉴定功能性抗菌肽的能力,为抗生素开发者提供了多种新线索,并标志着一个充满希望的抗生素发现新时代的开始。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


