Nature:迟洪波团队利用单细胞CRISPR筛选,在体内绘制肿瘤T细胞命运调控网络
来源:生物世界 2023-11-17 13:54
这项研究揭示了肿瘤内CTLs分化和功能的多样性及关键的调控转录因子,并为整合CTLs细胞命运基因调控网络和改善肿瘤免疫反应的潜在靶点提供了一个系统框架。
美国圣裘德儿童研究医院迟洪波团队在 Nature 期刊发表了题为:Single-cell CRISPR screens in vivo map T cell fate regulomes in cancer 的研究论文。
该研究使用单细胞CRIPSR筛选,在体内绘制了肿瘤T细胞命运调控网络。揭示了促使耗竭T细胞前体/祖细胞(Tpex)细胞退出静息状态以及增强终末耗竭T细胞(Tex)细胞增殖状态的关键调控转录因子,并用以改善肿瘤免疫疗法。

在迟洪波教授的指导下,周培培、史豪、黄宏龄等博士在CTLs中利用单细胞CRIPSR筛选(scRNA-seq)系统性绘制了CTLs基因调控网络并发现了其分化的检查点及关键的转录调控因子(IKAROS–TCF-1、ETS1–BATF和RBPJ–IRF1)。
首先,他们发现Tpex细胞退出静息状态并连续分化为中间型Tex1细胞(有较强的功能和增殖能力的一群Tex细胞),这一过程由IKAROS和ETS1差异调控。IKAROS促进Tpex1(有较弱增殖能力的一群Tpex细胞)的代谢激活及其分化为Tpex2细胞(有较强增殖能力的一群Tpex细胞)。
敲除IKAROS抑制了CTLs的功能,增加了肿瘤内CTLs的干细胞性的同时降低了细胞代谢以及mTORC1信号通路的活性,暗示IKAROS缺陷可能使细胞滞留在过度静止的状态。并且,敲除IKAROS导致的CTL细胞积累无法单独或响应ICB改善抗肿瘤免疫反应。
相反,敲除ETS1通过增强mTORC1信号通路活性和代谢重编程来调控Tpex2到Tex1分化过程,并且在多个肿瘤模型中增强了过继细胞疗法(ACT)和免疫检查点阻断疗法(ICB)抗肿瘤效果,并且ETS1基因表达量与癌症患者对ICB的响应呈负相关。
在机制上,他们揭示了TCF-1和BATF可以分别被IKAROS和ETS1负向调控,是IKAROS和ETS1在CTL细胞中的靶点。
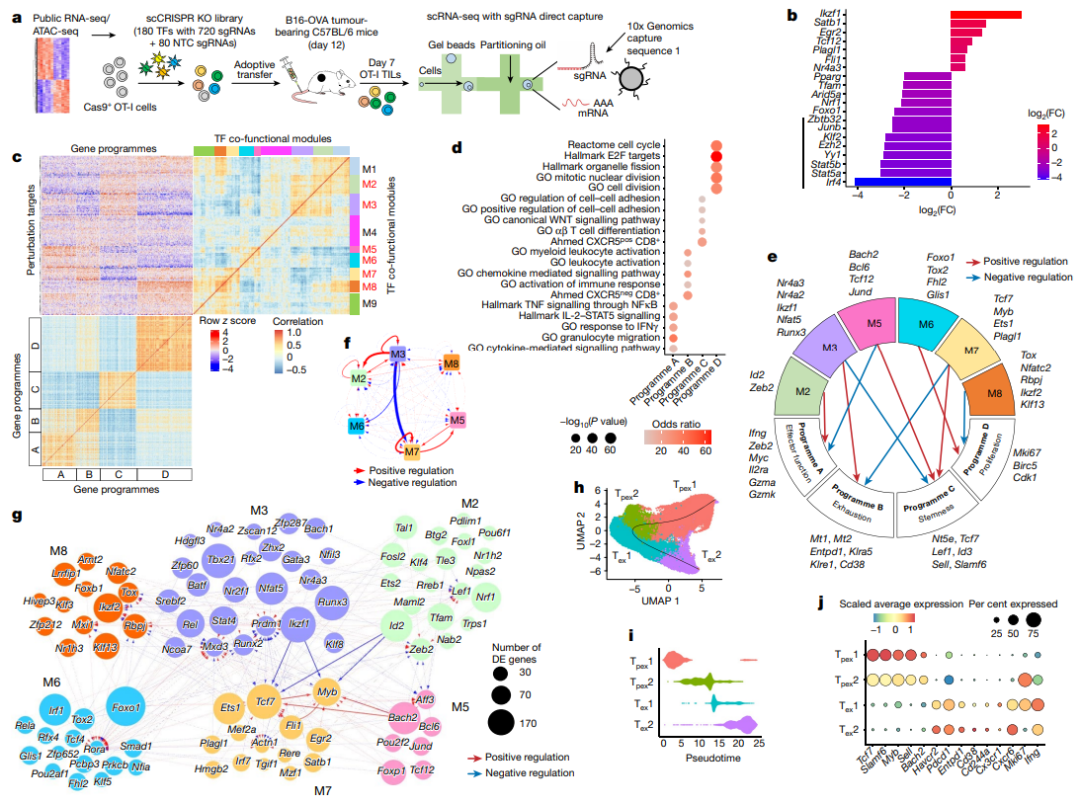
肿瘤内CTLs的体内scCRISPR筛选揭示协同功能模块和基因程序的连通性
其次,他们发现敲除RBPJ阻断了中间型Tex1向终末Tex2细胞(有较弱的功能和增殖能力的一群Tex细胞)分化,同时通过增加Tex细胞的增殖能力来扩大Tex1细胞累积。并且,敲除RBPJ在多个肿瘤模型中改善了ACT和ICB的抗肿瘤效果。另外,RBPJ基因的表达量与来自癌症患者CTLs的终末Tex分化以及癌症患者对免疫检查点阻滞疗法的低反应性正相关。
在机制上, RBPJ通过抑制IRF1转录因子的活性来促进了中间型Tex1到终末型Tex2细胞的分化。因此,敲除RBPJ通过增强有较强功能和增殖能力的Tex1细胞的分化来改善ACT和ICB的抗肿瘤效果。
总的来说,这项研究揭示了肿瘤内CTLs分化和功能的多样性及关键的调控转录因子,并为整合CTLs细胞命运基因调控网络和改善肿瘤免疫反应的潜在靶点提供了一个系统框架。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


