《自然·医学》:三英战肠癌!双免疫+化疗方案治疗RAS突变晚期肠癌有效率超60%
来源:奇点糕 2023-08-13 19:49
总而言之,PD-L1抑制剂+CTLA-4抑制剂+化疗组成的联合方案,用于不可手术的MSS型CRC患者确实疗效不错,希望该方案能够进一步走向临床III期研究,并尽量实现安全性和精准性的优化啦。
近日,法国研究者们在《自然·医学》发表了一项临床I/II期研究成果,首次揭示由PD-L1抑制剂(度伐利尤单抗)+CTLA-4抑制剂(tremelimumab)组成的双免疫方案+标准化疗,一线治疗携带RAS突变的MSS型晚期CRC客观缓解率(ORR)高达64.5%,患者中位无进展生存期(PFS)为8.2个月。
双免疫方案在ORR和PFS两项关键疗效指标上,都显著优于既往化疗或免疫单药治疗用于MSS型晚期CRC的表现,且研究者们还对患者转录组学情况、免疫微环境特征等展开了深入分析,相关信息有望在未来指导更精准的CRC免疫联合治疗。

论文首页截图
本次研究共纳入了57例不可手术切除的RAS突变型晚期CRC患者,其中51例接受了微卫星状态评估,48例为MSS型并组成后续疗效分析集。由于研究的联合治疗用药较多(双免疫+mFOLFOX方案),3-4级不良事件的发生率达67%,且有7例患者因不良事件停药,但绝大多数不良事件都被判定为化疗相关。
研究主要终点设定为疗效分析集患者3个月时的PFS率,双免疫+化疗方案交出的数字是90.7%,显著优于研究者预计的70%,患者12个月PFS率则为26.9%,同时64.5%的ORR也达到了次要疗效终点,中位缓解持续时间则是8.5个月。
在总生存期(OS)方面,中位随访时间达36个月时,全部患者的中位OS尚未达到,12和24个月OS率分别为81.1%和57.6%。而截至此次分析Cut-off时,仍有8例患者处于治疗后的完全缓解状态,生存时间有望再创新高。
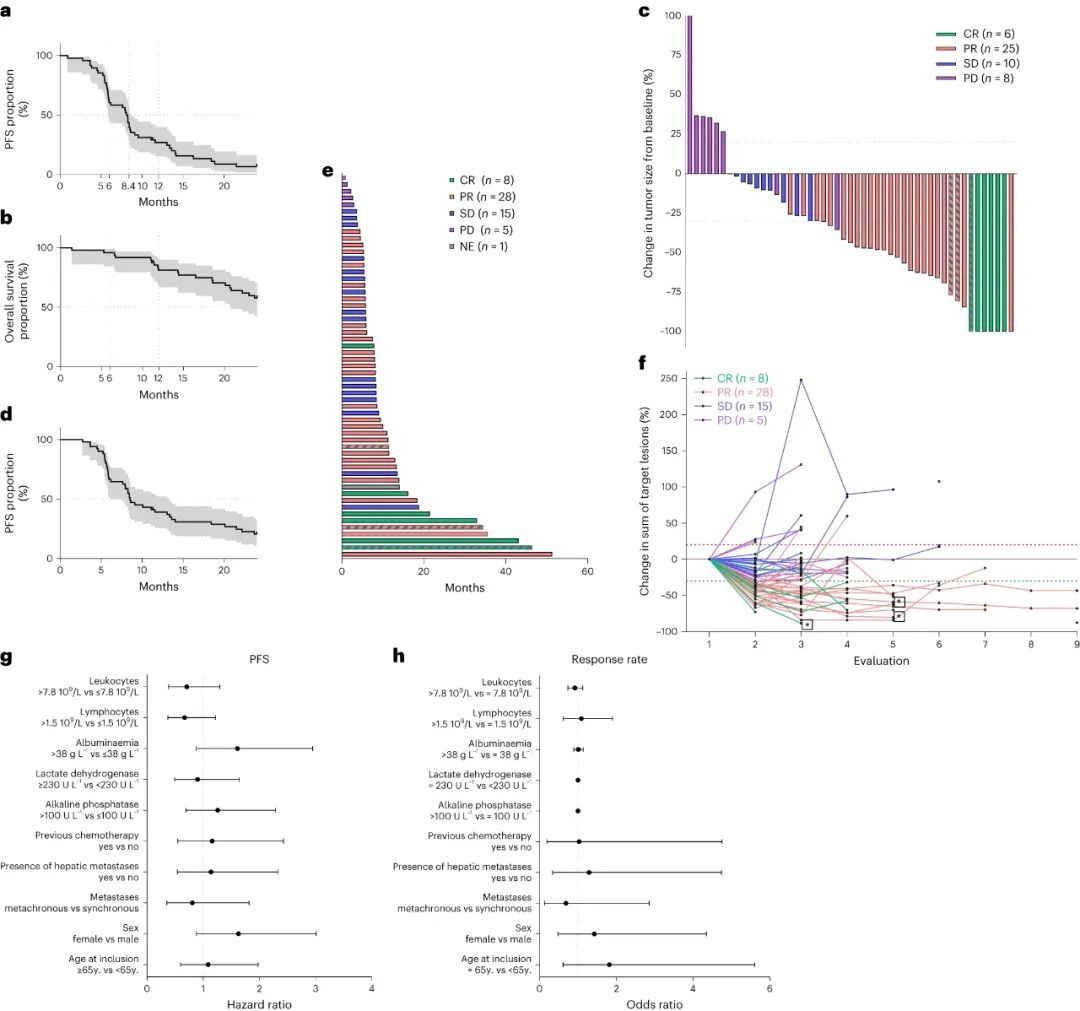
患者PFS、OS等疗效指标情况
双免疫+化疗方案的优异表现,无疑值得进一步深度探索,那么有哪些临床特征、基因变异和生物标志物,能够用来指引双免疫+化疗方案的使用呢?
首先在基因变异方面,仅肿瘤突变负荷(TMB)有一定的疗效预测价值,TMB>5.8个/Mb与患者PFS较长显著相关(HR=0.41),但这一结论未能在外部数据库资料(如TCGA)中得到验证,而KRAS、TP53等共突变则与PFS无显著相关性。
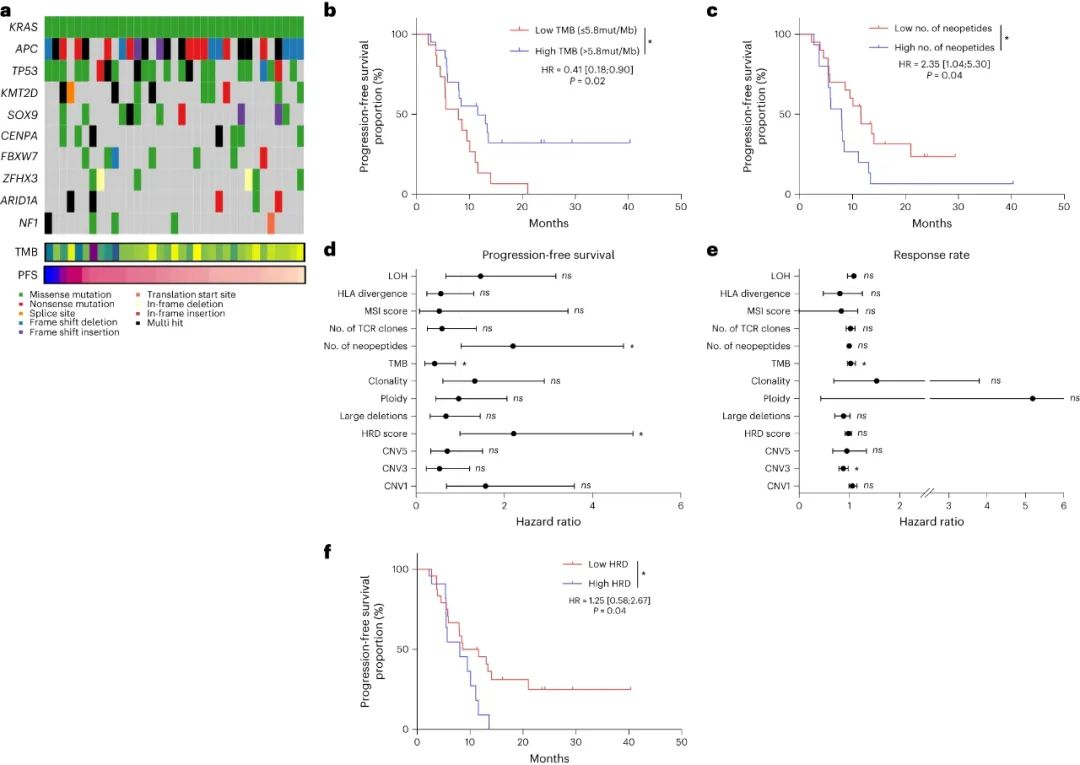
基因变异及相关标志物与疗效的相关性
转录组学分析则显示,双免疫+化疗方案要想大展拳脚,需要免疫细胞的充分浸润、吸引T细胞的趋化因子发挥作用,此外肿瘤中的间质成分也应较少,如CTLA-4的mRNA在肿瘤微环境中高表达,是唯一与PFS较长相关的免疫特征预测指标。
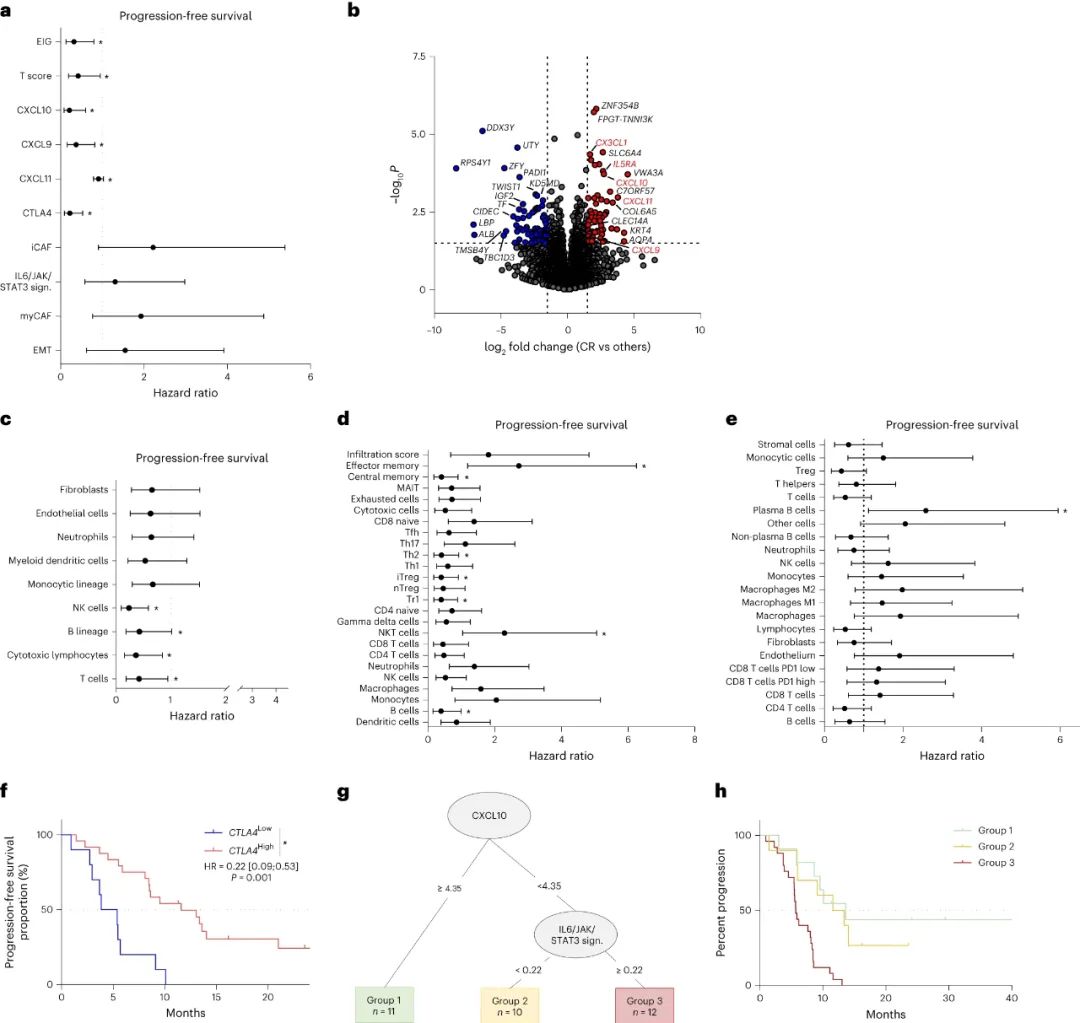
转录组学分析标志物与疗效的相关性
免疫组化检测的PD-L1表达水平(PD-L1 CPS),与患者预后并无显著相关性,但CD8+T细胞浸润到肿瘤核心部位,且PD-L1组织化学评分(H-score)较高,就与患者PFS较长有关。
此外,炎性肿瘤相关成纤维细胞(iCAFs)往往对抗肿瘤免疫应答不利,因此研究者们通过分析证实,iCAFs表面特异性高表达的核心蛋白聚糖(decorin)水平较低,也预示着患者的PFS较长。
而未对双免疫+化疗方案治疗应答的患者,肿瘤间质中普遍存在更多的I型胶原(COL1),它们可能充当了阻止免疫细胞浸润的屏障,因此COL1也可作为预测疗效标志物的一部分(CD3+/COL1比值,因应答患者肿瘤中多见CD3+免疫细胞)。
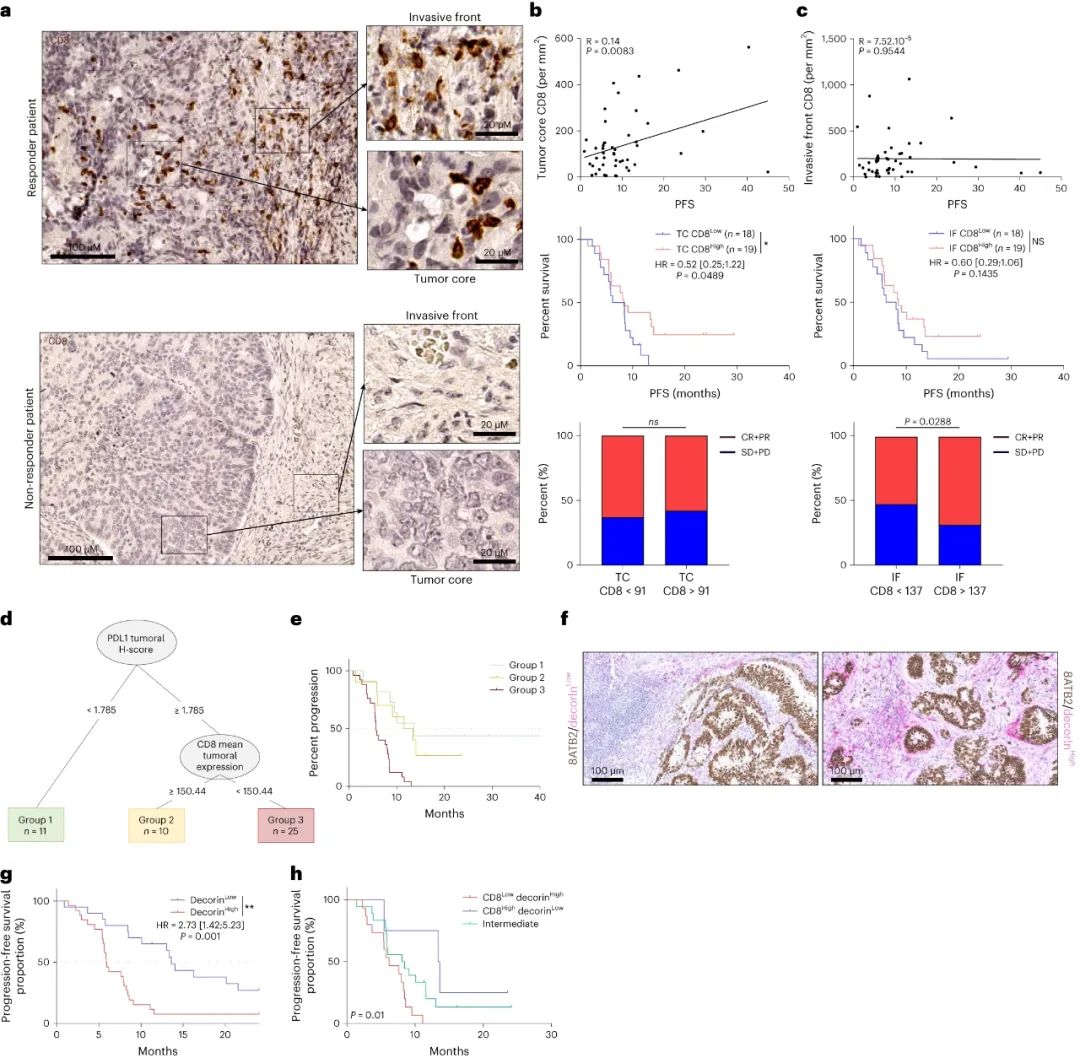
免疫组化分析情况
总而言之,PD-L1抑制剂+CTLA-4抑制剂+化疗组成的联合方案,用于不可手术的MSS型CRC患者确实疗效不错,希望该方案能够进一步走向临床III期研究,并尽量实现安全性和精准性的优化啦。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


