Science:哈佛大学用人类心脏细胞造了一只鱼,可持续游动108天
来源:生物世界 2022-02-14 08:29
心脏就像一台不知疲倦的永动机,生命不息跳动不止。但是心脏规律的跳动并不是由大脑发出的指令,而是心脏中的心肌细胞控制着整个心脏的跳动。然而,控制该过程的机制尚不完全清楚。受到斑马鱼的形态和运动姿势的启发,来自哈佛大学和埃默里大学的研究团队首次利用人类干细胞来源的心肌细胞培育出了完全自主的生物杂交鱼。该研究以:An autonomousl
心脏就像一台不知疲倦的永动机,生命不息跳动不止。但是心脏规律的跳动并不是由大脑发出的指令,而是心脏中的心肌细胞控制着整个心脏的跳动。然而,控制该过程的机制尚不完全清楚。
受到斑马鱼的形态和运动姿势的启发,来自哈佛大学和埃默里大学的研究团队首次利用人类干细胞来源的心肌细胞培育出了完全自主的生物杂交鱼。
该研究以:An autonomously swimming biohybrid fish designed with human cardiac biophysics 为题发表在国际顶尖学术期刊 Science 上,借助这种专注于人类心脏关键调控特征的能够自主游泳的生物杂交鱼,研究人员揭示了心肌泵反馈机制的重要性。
该研究团队还表示,这一发现在未来可能会协助开发一种由活心肌细胞制成的人造心脏,以治疗那些存在心肌功能严重缺陷的患者。
生物杂交鱼的设计和构建
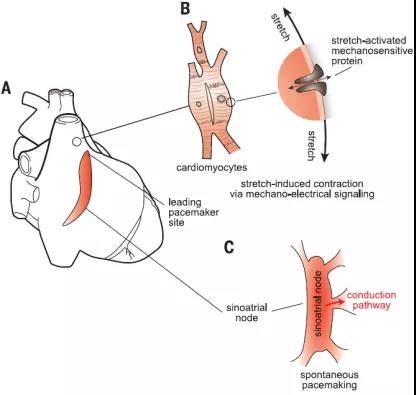
在循环系统中,电信号和心脏自律性在调节心肌收缩速度和强度方面起着至关重要的作用。心脏的自律性源于窦房结,它在结构和功能上与周围的心肌隔离,并在没有外部刺激和直接神经干预的情况下发起自发电活动。
随后,研究人员利用心脏控制系统的原理设计出了生物杂交鱼,可以使流体泵送系统的效率与天然的鱼类流体泵送系统相当。利用心脏功能的基本特征,可以实现自主的自我起搏和独立的运动控制。
这类生物杂交鱼拥有拮抗肌肉双分子层和几何绝缘的心脏组织节点,其中含有人类干细胞来源的心肌细胞(CMs)。在生物杂交鱼的肌肉双分子层结构中,CMs 的两侧被机械耦合在一起,因此一侧肌肉的收缩能够直接转化为对侧肌肉的轴向拉伸,导致拮抗肌肉的兴奋和收缩。
为了复制窦房结的电绝缘结构,他们通过一个出口通道,在 G 节点和肌肉组织之间建立电连接。因此,生物杂交鱼的肌肉双分子层和 G 节点共同使其产生连续的节奏来调节肌肉的拮抗,从而产生自发且协调的身体-尾鳍运动。
为了系统描述肌肉双分子层的运动学,他们通过外部光遗传刺激控制生物杂交鱼的拮抗肌肉收缩。通过蓝色和红色发光二极管光脉冲交替刺激肌肉双分子层,在红光刺激下,左侧肌肉组织开始收缩;蓝光刺激后诱导右侧肌肉组织收缩,以近乎直的姿势收回尾巴,生物杂交鱼产生了有节奏的向前持续推力来实现前进。
接下来,他们测试了人类干细胞来源的心肌细胞重建的拮抗肌收缩是否可以通过机械电信号维持自发节律性收缩。结果发现,生物杂交鱼一侧的自发激活和收缩通过肌肉组织间的机械耦合能够导致另一侧的随后拮抗收缩,这些自发的对抗性收缩使得鱼身体发生交替的弯曲运动,并有节奏地持续向前移位。这些现象证明了肌肉双层的自发节律性收缩。
考虑到生物杂交鱼的自主拮抗肌肉收缩,难免会有人质疑这种自发的活动是否能够长期发挥作用。最后,研究人员使生物杂交鱼自发活动持续了 108 天,相当于心脏的 3800 万次跳动。结果发现,这种自主游泳的生物杂交鱼在第一个月内不断提高肌肉收缩幅度、最大游泳速度和肌肉协调能力,并在 108 天内保持了良好的游泳性能。这些数据证明了肌肉双分子层系统和电信号作为一种手段促进体外肌肉组织的成熟的潜力。
综上所述,研究人员从心脏的生物物理学中汲取设计灵感,在国际上首次利用人类干细胞来源的心肌细胞制造出这种自主生物杂交鱼,可以持续游动 100 天以上。通过自建一个「心脏」来复制心脏工作中的关键生物物理原理,可助力于未来更细致的心脏疾病的研究。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


