Cell子刊:熊伟/陈珏/李敏等解析暴饮暴食的肠-脑轴神经环路机制
来源:生物世界 2023-10-07 13:10
作者进一步对OD小鼠进行全脑c-Fos染色并对潜在的候选核团进行化学遗传及光遗传操纵。当丘脑室旁核PVT被激活时,小鼠出现了明显的OD症状;而当OD建模小鼠的PVT被抑制时,其过度进食的症状得到了明显

接下来为了验证肠道微生物在OD中的作用,作者使用四联抗生素清除了未进行过OD建模小鼠肠道中的绝大多数微生物,发现这些小鼠出现了稳定且极端的过度进食行为。由此可知肠道微生物在进食调节中担任极为重要的“守卫”角色。将健康小鼠的粪便微生物定殖到小鼠肠道中,可以显著缓解OD小鼠的暴饮暴食症状。而将OD小鼠的粪便微生物反向定殖到健康小鼠体内,却无法复制过度进食的症状。这些结果表明,节食史联合压力应激导致的OD很有可能是由于益生菌的减少而非有害微生物的增多引起的。通过 16s rDNA 测序,作者发现了OD小鼠肠道中乳酸菌属和瘤胃菌属的微生物显著减少,而这些微生物是维持健康肠道环境必不可少的组成。
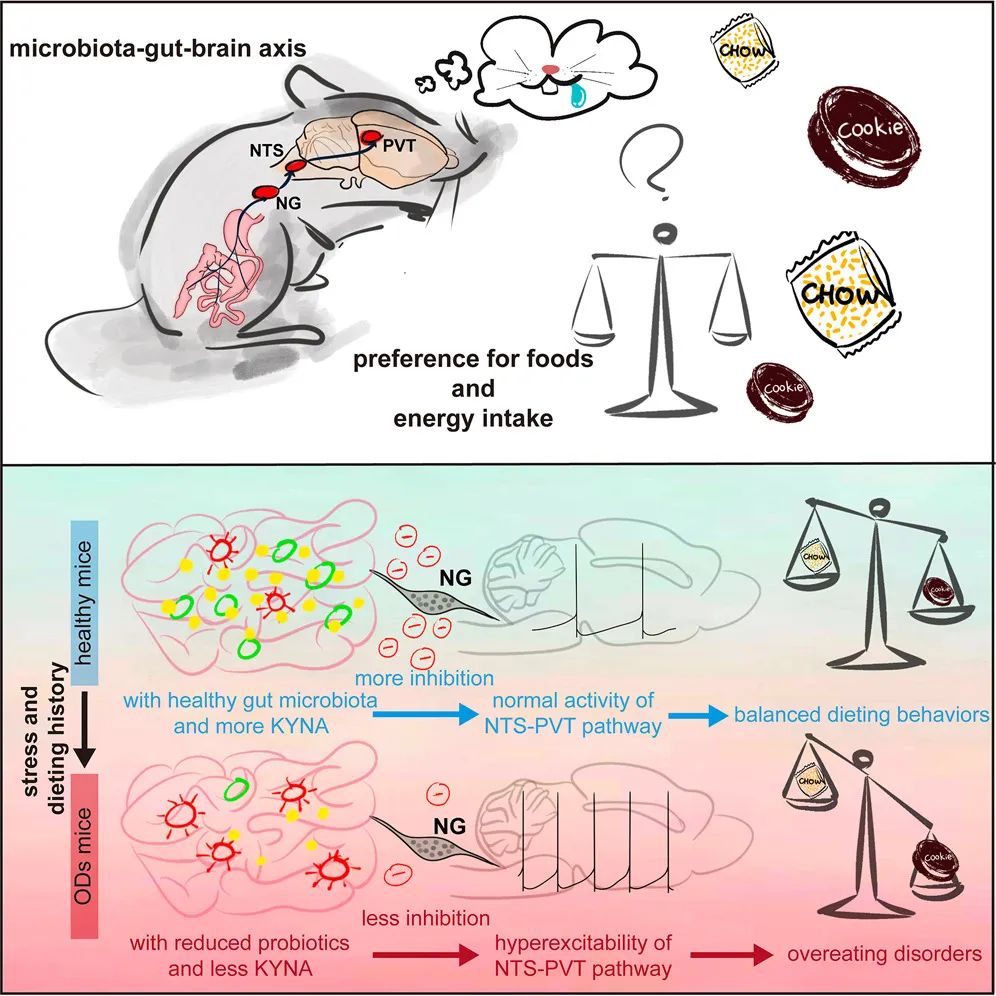
作者进一步对OD小鼠进行全脑c-Fos染色并对潜在的候选核团进行化学遗传及光遗传操纵。当丘脑室旁核PVT被激活时,小鼠出现了明显的OD症状;而当OD建模小鼠的PVT被抑制时,其过度进食的症状得到了明显的缓解。在起始于PVT的环路逆行示踪中,研究人员发现孤束核NTS直接投射到PVT,并通过全细胞膜片钳和在体光纤记录的方法在OD小鼠的PVT和NTS中记录到了显著高于对照组的神经活动,提示NTS-PVT环路在过度进食障碍中产生了过高的兴奋。通过病毒追踪手段和迷走神经横断术,作者进一步找到了接收来自肠道信息的迷走神经 (Vagus) -NTS-PVT投射环路,形成由肠道指导暴食行为的“通路”基础。
进一步的代谢组学研究发现在ODs小鼠的肠道众多代谢物中,犬尿酸(Kynurenic acid, KYNA)水平显著降低。补充肠道KYNA可以抑制Vagus-NTS-PVT环路的过度激活,从而缓解OD小鼠过度进食症状。对临床神经性贪食症(Bulimia nervosa, BN)患者肠道中的微生物及代谢物进行分析,发现了同属于瘤胃菌属的 Faecalibacterium_prausnitzii菌丰度远低于其在健康志愿者肠道中的水平。肠道KYNA水平在BN患者中也显著降低。随后,作者将Faecalibacterium_prausnitzii菌定殖到OD小鼠肠道中后,发现小鼠的过度进食行为伴随着KYNA水平回升得到了明显改善。
综上,这项工作通过对微生物检测、外周-中枢神经环路鉴定及肠道代谢物分析的多方位探究,阐明了介导过度进食障碍的微生物-肠-脑轴机制,提示肠道微生物与中枢神经乃至行为之间相辅相成的重要关系,并为过度进食障碍相关疾病提供了潜在的治疗方向与策略。
值得一提的是,熊伟教授课题组前期发展了一系列多尺度代谢组学新技术(PNAS, 2017; Anal Chem, 2019a,b;Nature Methods, 2021;Nature Machine Intelligence, 2023;Science Bulletin, 2023),发现了皮肤代谢物尿刊酸跨器官介导日光照射影响大脑学习记忆的神经环路机制,并阐明了其它多种代谢分子在神经环路及脑网络中的功能(Cell, 2018;Nature Communications, 2021;Cell Reports, 2020; Molecular Psychiatry, 2022;Nature Metabolism, 2022;Science Advances, 2023;Cell Metabolism, 2023)。此次解析肠道代谢物通过肠脑轴影响中枢摄食行为的工作,将其团队神经代谢领域的研究范畴进一步扩大到了外周肠道,为多角度多维度理解全身神经代谢网络与功能奠定了基础。
上述相关内容可参考熊伟教授课题组网站(http://x-lab.ustc.edu.cn/)。
据悉,中国科学技术大学生命科学与医学部博士后范思佳、郭薇薇为该论文共同第一作者,中国科学技术大学熊伟、上海精神卫生中心陈珏和安徽医科大学李敏为共同通讯作者。上海精神卫生中心彭素芳、中国科学技术大学尹浩与冯艾荣参与了合作研究。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


