《自然·神经科学》:终于实锤了!中国科学家首次证实,线粒体呼吸链复合体IV缺陷与渐冻症存在因果关系
来源:网络 2025-03-14 10:32
张晓荣/马元武团队在人体研究数据和大鼠模型数据的基础上,证实在散发性ALS患者体内广泛存在的CIV缺陷,是导致渐冻症的重要原因之一。
渐冻症,也就是肌萎缩侧索硬化症(ALS),是一种致命的神经退行性疾病。
一旦确诊渐冻症,预期生存时间通常仅有3到4年。
从上面的数据就可以看出,对于绝大多数渐冻症患者而言,目前仍没有有效的治疗手段。
虽然科学家已经确定了100多个与渐冻症相关的基因,例如SOD1、TARDBP、C9orf72和FUS等,并基于上述基因变异开发了相关的药物。
然而,携带上述基因突变的主要是家族性ALS(fALS,占ALS的10%左右),散发性ALS(sALS,占ALS的90%左右)的潜在致病机制在很大程度上仍不为人知。
今天,由中国医学科学院张晓荣和马元武领衔的研究团队,在著名期刊《自然·神经科学》上发表一篇重磅研究论文[1],有望为渐冻症的治疗破局。
他们发现,在散发性ALS患者体内广泛存在(50%以上的患者)的线粒体呼吸链复合体IV(CIV)缺陷,是导致渐冻症的原因之一。更重要的是,他们还构建了相关的大鼠ALS模型,再现了渐冻症患者的一系列关键表型。
毫无疑问,这项研究成果会加深科学家对渐冻症的了解,更会加速具有广泛治疗价值的药物的研发。

▲ 论文首页截图
张晓荣/马元武团队注意到,在之前的一项研究中,研究人员发现46%的散发性ALS(sALS)患者表现出细胞色素c氧化酶(COX)(复合体IV [CIV])缺陷[2]。
鉴于CIV与线粒体细胞呼吸密切相关,以及之前发现的一些基因突变患者也表现出线粒体功能受损,这些让他们想知道CIV缺陷与渐冻症之间的关系。
他们先收集了40名已故散发性ALS患者的血液样本,并分析了其中的线粒体DNA序列。分析结果显示,其中50%的病例携带6692A缺失,导致COX亚基I(COXI)过早出现终止密码子。还有一名患者携带9478T缺失,导致COX亚基III(COXIII)翻译过早终止。
不难看出,散发性ALS患者体内确实存在CIV缺陷的情况。
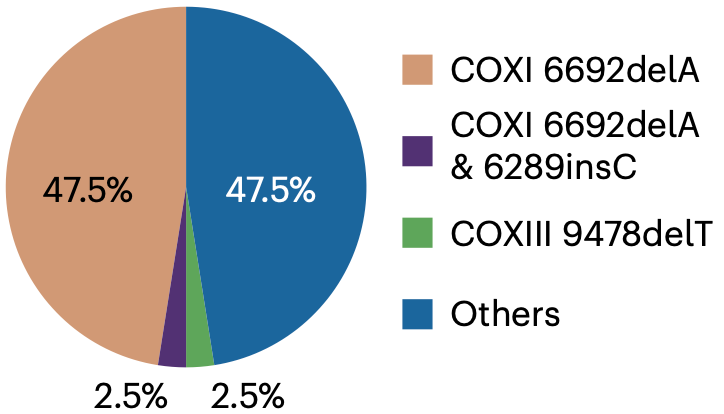
▲ 患者的基因突变情况
在分析渐冻症患者和对照受试者的运动神经元(MN)蛋白质组数据之后,张晓荣/马元武团队进一步确认,与对照组相比,渐冻症患者的运动神经元表现出多个CIV亚基表达水平较低的现象,例如COXII、COXIII、COX5A、COX5B、COX6C、COX7C和COX7B等。
此外基于329名渐冻症患者的数据,他们还发现,CIV表达较低的渐冻症患者的存活时间比CIV表达较高的患者短。
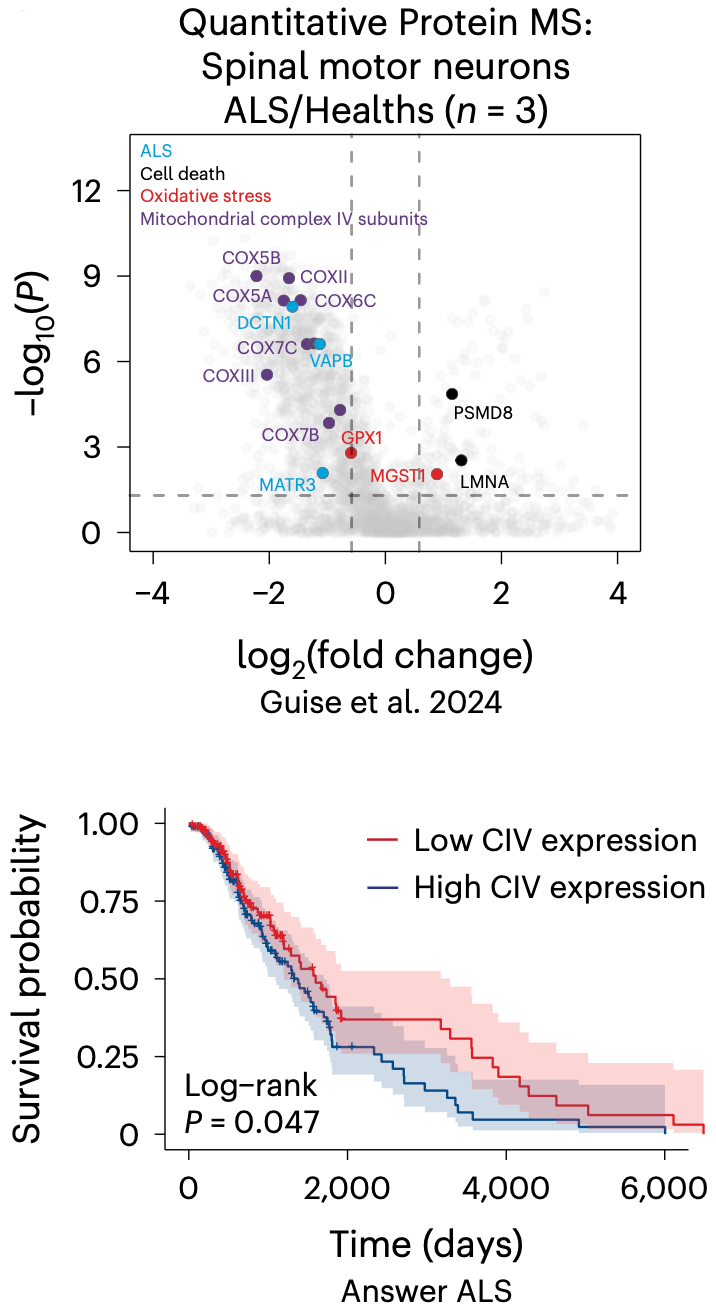
▲ 渐冻症患者CIV水平低(上)
CIV水平越低,患者预后越差(下)
在上述研究结果的基础上,张晓荣/马元武团队提出了一个假设:CIV缺陷会选择性地损害中枢神经系统中运动神经元的功能,从而导致渐冻症。
接下来的问题是,造模能不能复现渐冻症患者的特征。
借助基因编辑技术,研究人员在大鼠神经元线粒体基因组的CIV亚基编码基因COXI、COXII和COXIII中,特异性引入了过早终止密码子。
总体上看,与对照组相比,大多数COXI、COXII和COXIII突变大鼠在出生后第一个月基本正常,但之后逐渐出现类似渐冻症的症状。由于COXII和COXIII突变大鼠在成年后,会出现更典型的类似渐冻症的表型,因此他们重点对这两种突变大鼠进行了详细的特征描述。
跟预计的一样,COXII和COXIII突变大鼠腰脊髓中的COXII和COXIII蛋白含量大幅减少。从表型上看,COXII和COXIII突变大鼠表现出进行性体重减轻、骨骼肌萎缩、脊柱后凸、瘫痪和进行性运动障碍,与渐冻症患者症状的发展过程相似。
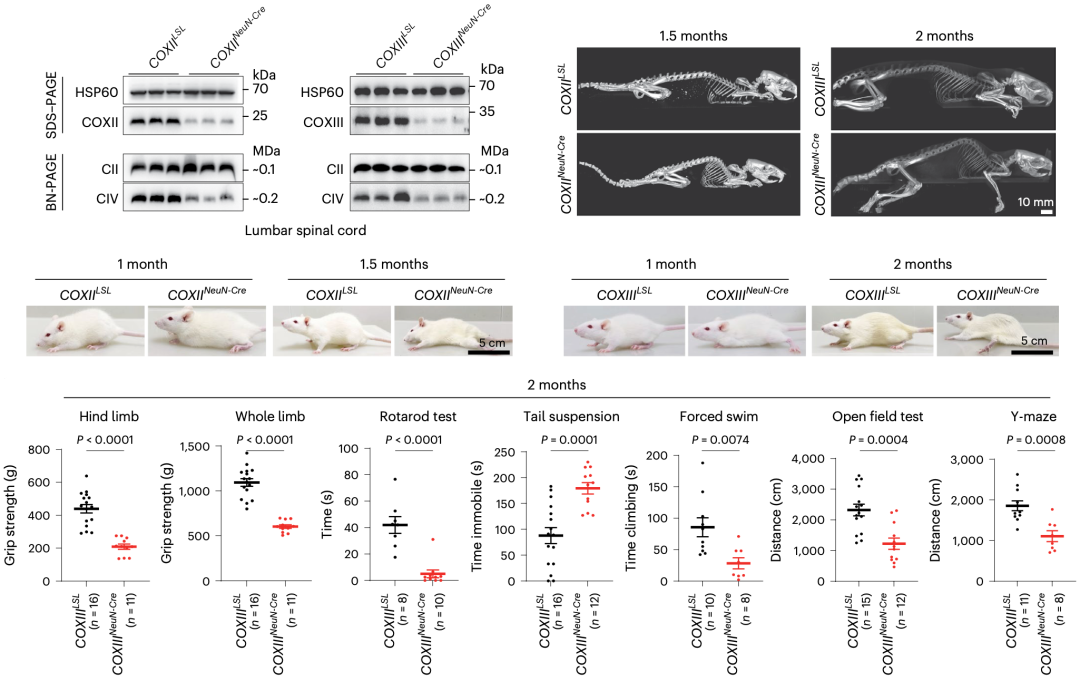
▲ 大鼠的渐冻症表型
张晓荣/马元武团队还注意到,与对照组相比,突变大鼠的大脑和脊髓运动神经元的许多标记基因转录水平显著降低,而其他类型的神经元几乎不受影响。
颗粒度更小的研究结果还显示,脊髓前角中的α运动神经元的特异性标记物,在蛋白质和RNA水平上都有所减少,而γ运动神经元的特异性标记物的表达没有显著变化。这说明,即使是运动神经元,受CIV缺陷的影响也存在差异性。
值得注意的是,瘫痪的COXII和COXIII突变大鼠的腹根运动神经元轴突显著缺失,而位于背根的感觉神经元轴突变化极小。基于这些发现,研究人员认为,与渐冻症患者相一致,腰脊髓中α运动神经元的选择性缺失,可能是导致CIV缺陷大鼠瘫痪的原因。
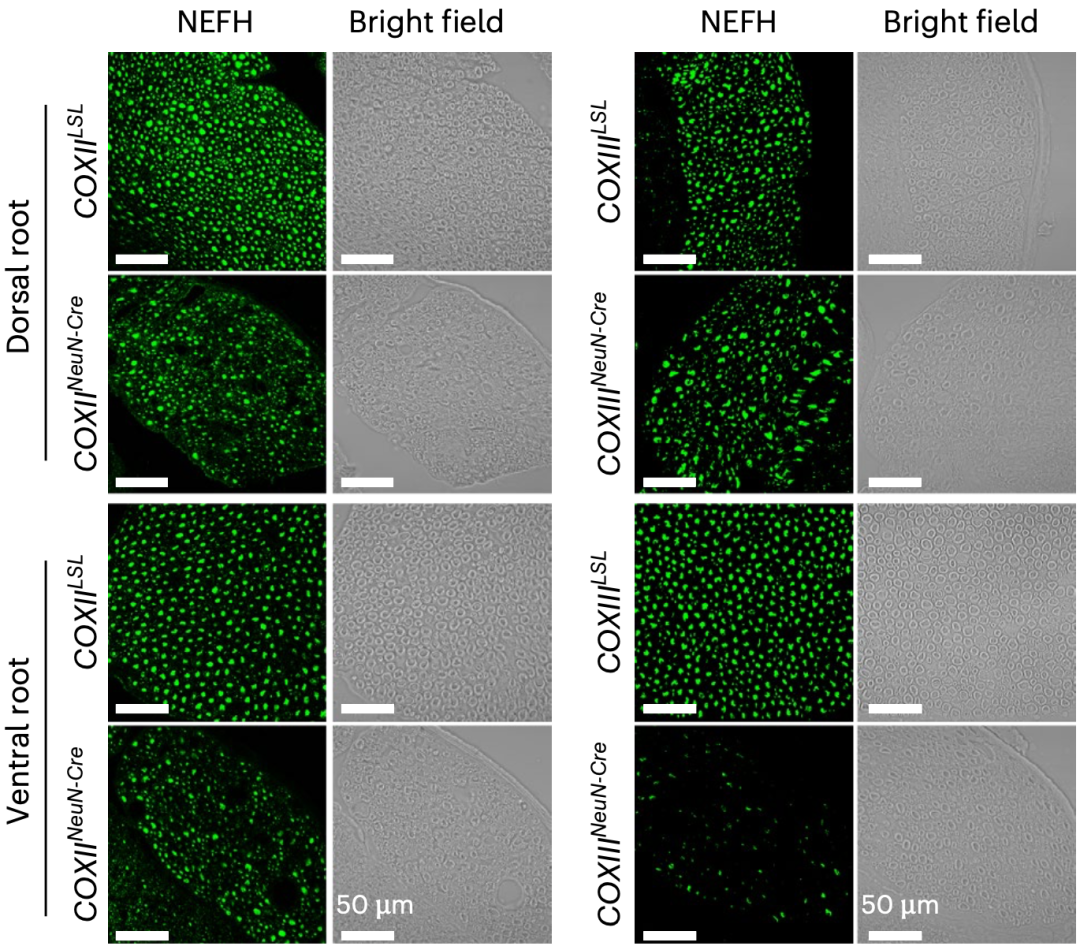
▲ 背根感觉神经元(上)和腹根运动神经元(下)的变化
除了上述变化之外,张晓荣/马元武团队还在COXII和COXIII突变大鼠身上观察到了,胫骨前肌和腓肠肌的重量,在疾病晚期显著减轻;胫骨前肌肌纤维的平均尺寸也显著缩小;胫骨前肌的神经肌肉接头显著减弱。
不难看出,渐冻症患者的肌肉萎缩和神经肌肉接头完整性受损,也在小鼠模型身上复现了。
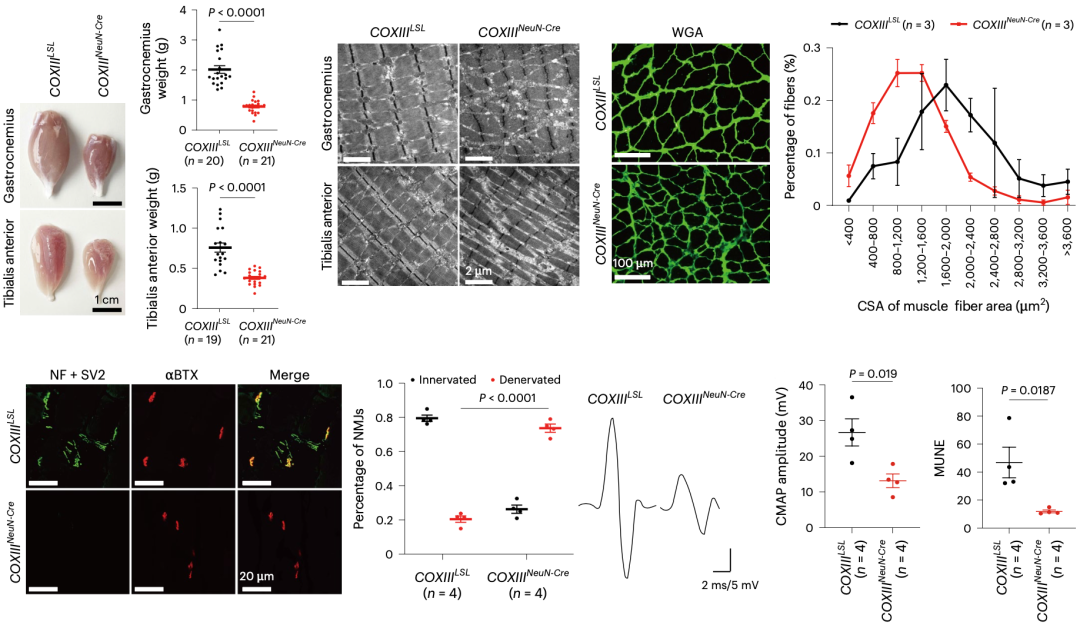
▲ 大鼠模型的肌肉和神经肌肉接头变化
在研究的最后,张晓荣/马元武团队基于单核RNA测序技术,确认模式大鼠的神经炎症和细胞死亡加剧。这些变化也与渐冻症患者的运动神经元类似。
总的来说,张晓荣/马元武团队在人体研究数据和大鼠模型数据的基础上,证实在散发性ALS患者体内广泛存在的CIV缺陷,是导致渐冻症的重要原因之一。而且他们构建的大鼠模型,忠实地再现了渐冻症的病理和相关症状特征,例如运动神经元缺失、神经肌肉接头异常、肌肉去神经支配、运动障碍和瘫痪等。
考虑到散发性ALS占全部渐冻症的90%,在CIV缺陷和渐冻症之间建立因果联系,不仅让我们有了认识渐冻症的新角度,还为散发性ALS的药物研发提供了一个强大的动物模型。
期待后续研究尽快跟进,早日为广大散发性ALS患者找到有效疗法。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


