多篇研究成果解读科学家们在癌症免疫疗法研究领域取得的新进展!
来源:生物谷原创 2025-04-30 09:34
前列腺癌免疫治疗的新希望!PIM抑制剂助力免疫疗法突破、新研究为针对儿童癌症的免疫疗法铺平了道路、新型抗癌药物或能让免疫疗法变得更加有效
本文中,小编整理了近期科学家们发表的多篇重要研究成果,共同解读他们在癌症免疫疗法研究领域取得的新进展,分享给大家!
【1】Cancer Immunol Res:前列腺癌免疫治疗的新希望!PIM抑制剂助力免疫疗法突破
doi:10.1158/2326-6066
在癌症治疗领域,免疫疗法的出现无疑是一场革命,其能通过激活人体自身的免疫系统来攻击癌细胞,从而为多种癌症患者带来新的希望,然而对于前列腺癌患者来说,免疫检查点抑制剂的效果却不尽如人意,这种疗法在其它癌症的治疗中取得了显著的疗效,但在前列腺癌中却一直未能发挥其应有的作用;这背后的原因一直困扰着科学家们。
近日,一篇发表在国际杂志Cancer Immunology Research上题为“Inhibition of PIM kinase in tumor-associated macrophages suppresses inflammasome activation and sensitizes prostate cancer to immunotherapy”的研究报告中,来自亚利桑那大学健康科学中心等机构的科学家们通过研究揭示了前列腺癌免疫疗法的新潜力,有望为前列腺癌的免疫治疗带来新的曙光。
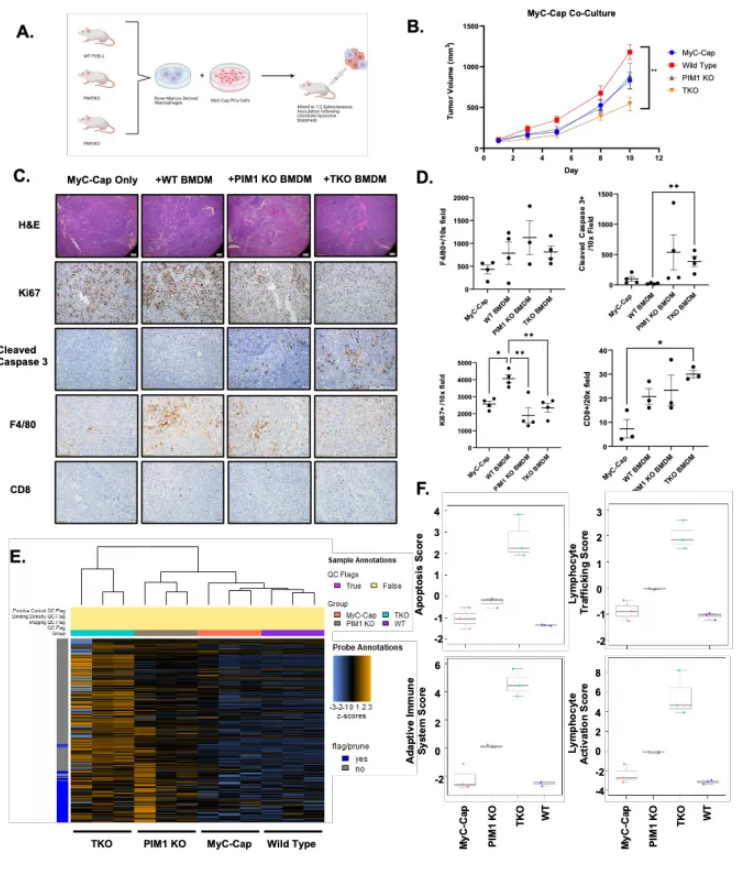
巨噬细胞中PIM表达的缺失会激活机体的免疫反应并抑制肿瘤生长
前列腺癌是男性中最常见的癌症之一,仅次于皮肤癌。据美国癌症协会数据显示,大约每8名男性中就有1人会在一生中被诊断出前列腺癌,这种癌症的治疗一直面临着诸多挑战,尤其是免疫疗法的失效。免疫检查点抑制剂能通过阻断癌细胞上的检查点蛋白,释放T细胞的攻击能力,从而让免疫系统能够消灭癌细胞。然而在前列腺癌中,这种疗法的效果却不理想,研究人员推测,这可能与前列腺肿瘤微环境中的免疫抑制有关,而肿瘤相关巨噬细胞(TAMs)在其中扮演了关键角色。
在这项研究中,研究人员通过研究首次发现,PIM1激酶(一种促进细胞生长和癌细胞增殖的蛋白激酶)在肿瘤相关巨噬细胞中的过度表达是导致免疫疗法失效的关键因素,PIM1激酶不仅能帮助癌细胞生长和迁移,还在肿瘤免疫微环境中发挥着重要作用。研究人员通过使用PIM抑制剂成功重新编程了肿瘤相关巨噬细胞,使其从抑制T细胞活性转变为支持T细胞攻击癌细胞,这一过程不仅增加了T细胞在前列腺中的增殖,还增强了它们摧毁前列腺癌细胞的能力。
doi:10.1016/j.cell.2024.12.014
在一项新的研究中,来自卡罗林斯卡研究所和阿斯特丽德-林格伦儿童医院的研究人员确定了儿童免疫系统如何根据年龄对不同类型的癌症作出反应。这一发现揭示了儿童和成人免疫反应之间的显著差异,并有可能为癌症儿童提供新的量身定制的治疗方法。
相关研究结果于2025年1月20日在线发表在Cell期刊上,论文标题为“Systems-level immunomonitoring in children with solid tumors to enable precision medicine”。
论文通讯作者、卡罗林斯卡研究所妇女与儿童健康系儿科免疫学教授、阿斯特丽德-林格伦儿童医院儿科医生Petter Brodin说,“免疫系统的激活对我们抗击癌症的能力至关重要,但儿童和成年人之间有所不同。如果我们要正确治疗儿童癌症,我们需要了解癌症儿童的免疫系统如何被激活和调节,以及哪些因素会影响他们的免疫反应。”
这项研究纳入2018年至2024年间在阿斯特丽德-林格伦儿童医院被诊断患有不同类型实体瘤的191名0至18岁的儿童。这些作者分析了肿瘤组织和血液样本,以确定肿瘤中的基因突变,并确定哪些基因在免疫系统中是活跃的,哪些是不活跃的。Brodin教授解释说,“癌症的精准医学主要关注肿瘤的特性。通过表征免疫系统,我们引入了一个全新的维度,这将有助于塑造儿童癌症治疗的未来。”
【3】Cancer Cell:新型抗癌药物或能让免疫疗法变得更加有效
doi:10.1016/j.ccell.2024.11.006
基于T细胞的免疫疗法已经被证明在治疗弥漫性大B细胞淋巴瘤(DLBCL,diffuse large B cell lymphoma)和滤泡性淋巴瘤(FL,follicular lymphoma)上是有效的,但预测反应和理解药物耐受性的发生,对于科学家们而言一直是一大挑战。
近日,一篇发表在国际杂志Cancer Cell上题为“EZH2 inhibition enhances T cell immunotherapies by inducing lymphoma immunogenicity and improving T cell function”的研究报告中,来自美国威尔康乃尔医学院等机构的科学家们通过进行一项临床前研究发现,一种称之为EZH2抑制剂的新兴抗癌药物或能极大地增强一些癌症免疫疗法的治疗潜力。
这种抑制剂能靶向作用EZH2酶,EZH2酶在肿瘤细胞中的活性被认为是很多癌症发生的重要因素;文章中,研究人员发现,EZH2的抑制联合基于T细胞的免疫疗法,在促使非霍奇金B细胞淋巴瘤缩小方面要比单独使用免疫疗法的效果更好。研究者Wendy Beguelin博士表示,这些令人鼓舞的临床前研究结果或许能促进我们在淋巴瘤患者中启动EZH2抑制剂联合免疫疗法治疗的研究。
基于T细胞的免疫疗法包括称之为CAR-T细胞的工程化改造抗癌T细胞,其在一些淋巴瘤患者和其它血液恶性癌症患者中往往能有效减少或消除癌症发生的迹象,然而,在大多数情况下,癌症的迹象最终会复发。本文研究结果表明,抑制EZH2或许能帮助增强这些免疫疗法的效力和持久性,EZH2是一种特殊酶类,在正常情况下其能通过控制特定基因的表达来帮助编程细胞行为,EZH2基因的突变会促使酶类变得更具活性,如今这被认为是淋巴瘤发生的常见特征,而且抑制该酶类的功能或能让淋巴瘤患者获益,即使其机体中存在非突变的EZH2,依然如此。
【4】JAMA Oncol:新型免疫疗法组合有望治疗人类致死性甲状腺癌
doi:10.1001/jamaoncol.2024.4019
侵袭性甲状腺癌(aggressive thyroid carcinoma)包括放射性碘难治性(RAIR)分化甲状腺癌(DTC)、甲状腺髓样癌(MTC)和甲状腺未分化癌(ATC),其往往与显著的发病率和死亡率明显相关,且患者的治疗选择非常有限。如今,研究人员在甲状腺癌亚型中发现了不同的免疫谱系特征,这就表明其或许对于免疫检查点抑制剂敏感。
近日,一篇发表在国际杂志JAMA Oncology上题为“Dual Immune Checkpoint Inhibition in Patients With Aggressive Thyroid Carcinoma—A Phase 2 Nonrandomized Clinical Trial”的研究报告中,来自达纳法伯癌症研究所等机构的科学家们通过进行一项临床试验,结果发现,一种免疫疗法似乎能有效治疗致死性的甲状腺癌亚型。

尽管非常罕见,但侵袭性的甲状腺癌仍然是致死性的,且患者的治疗选择非常有限。在当前的临床试验中,研究人员开始测试药物纳武单抗(nivolumab)和易普利姆玛(ipilimumab)的组合性免疫疗法的疗效,这两种药物能防止癌症抑制宿主机体的免疫系统功能。文章中,研究人员让49名患有不同类型侵袭性甲状腺癌的患者每两周服用一次药物,最多持续两年时间;基于本文研究结果,仅有9%的分化型甲状腺癌患者对疗法能产生反应,而甲状腺髓样癌患者并未表现出对疗法产生反应的迹象。
【5】JCI:临床试验表明,预防癌症的局部免疫疗法或能训练机体的免疫系统来抵御癌前病变
doi:10.1172/JCI183274
近年来,皮肤癌发病率的持续上升凸显了改善人类皮肤癌预防的必要性。近日,一篇发表在国际杂志Journal of Clinical Investigation上题为“T helper 2 cell–directed immunotherapy eliminates precancerous skin lesions”的研究报告中,来自麻省总医院等机构的科学家们通过研究揭示了一种新型免疫疗法是如何预防鳞状细胞癌的,患者治疗后的效果能持续5年时间,这种疗法首次能激活机体适应性免疫系统的特定组分,尤其是CD4+ T辅助细胞,而这是在传统癌症治疗中并不涉及的,这一研究成果强调了类似的免疫疗法在预防全身其它癌症方面的潜力。
研究者Shawn Demehri教授说道,人类鳞状细胞癌的一个独特挑战就是,随着时间推移,患者发生多个新型病变位点的风险会增加,这就会使得癌症的预防成为护理的重要组成部分。我们发现,这种药物组合能通过一种不同于当前免疫疗法所使用的机制来预防癌症发生,这或许就表明,这些药物或能通过不同的机制来治疗和预防癌症。研究人员的愿景是为癌症患者的护理提供全面、综合和研究知情的方法,从而帮助患者完成从预防和早期检测到治疗和生存的整个护理过程。
鳞状细胞癌是人类第二大常见的皮肤癌类型,通常由阳光损伤所引起的癌前斑点(precancerous spots)表明机体鳞状细胞癌的风险会增加,但移除单个斑点并不能显著降低机体患癌的风险;最近研究人员通过研究发现,利用维生素D类似物(钙化三醇,calcipotriol)结合化疗(5-FU)或能通过激活患者自身的免疫系统来清除癌前斑点并预防癌症发生,然而,在这项临床试验之前,其作用机制研究人员并不清楚。
【6】PNAS:癌症免疫疗法的新突破!DDX54或有望成为关键靶点
doi:10.1073/pnas.2412310122
在癌症治疗的战场上,免疫检查点抑制剂(ICI)如同一位英勇的战士帮助免疫细胞更有效地攻击癌细胞。然而其也面临一个尴尬的困境:在所有接受治疗的患者中,仅有不到20%的患者能从中获益。这意味着大多数患者在满怀希望地接受治疗后,却不得不面对治疗无效的残酷现实。这种低响应率的现状无疑给癌症治疗蒙上了一层阴影,也让科学家们迫切地寻找新的策略来提高免疫治疗的效果,从而让更多的患者能够重燃生命的希望。
免疫疗法,尤其是通过抗PD-1或抗PD-L1抗体来激活免疫系统攻击癌细胞的方法,被认为是癌症治疗领域的一次革命性突破。然而肿瘤突变负荷(TMB)作为预测免疫治疗响应的关键生物标志物却在实际应用中暴露出明显的局限性。尽管高TMB的肿瘤理论上应该对免疫检查点抑制剂有更好的反应,但仍有约30%的肿瘤被归类为“免疫沙漠型”肿瘤,即尽管TMB高,但机体的免疫细胞仍难以浸润到肿瘤内部,从而就会导致治疗效果不佳。这种免疫细胞浸润受限的现象使得免疫治疗在这些患者中难以发挥应有的作用,这就极大地限制了免疫治疗的广泛应用。
近日,一篇发表在国际杂志Proceedings of the National Academy of Sciences上题为“DDX54 downregulation enhances anti-PD1 therapy in immune-desert lung tumors with high tumor mutational burden”的研究报告中,来自韩国科学技术院等机构的科学家们通过深入研究免疫逃逸肺癌患者的转录组和基因组数据,并运用系统生物学技术推断基因调控网络,成功地将DDX54鉴定为肺癌细胞免疫逃逸的关键调控因子,结果发现,通过抑制DDX54就能显著增加免疫细胞对肿瘤的浸润,并显著提高免疫治疗的效果。
这项研究中,研究人员通过对同种异体小鼠模型进行研究后发现,抑制DDX54就能显著增加抗肿瘤免疫细胞(如T细胞和自然杀伤细胞)的浸润,并极大地改善对免疫治疗的反应。利用单细胞转录组学和空间转录组学分析进一步显示,针对DDX54的联合治疗能促进T细胞和记忆T细胞的分化,这些细胞能抑制肿瘤生长同时减少调节性T细胞和耗竭T细胞的浸润,而且其通常还会促进肿瘤的生长。从机制上讲,抑制DDX54就能失活JAK-STAT、MYC和NF-κB等信号通路,从而下调免疫逃逸蛋白CD38和CD47的表达,这不仅减少了促进肿瘤发展的循环单核细胞的浸润,还促进了发挥抗肿瘤作用的M1型巨噬细胞的分化。
【7】癌症治疗的“双面间谍”?Cell:中国科学家揭秘细菌免疫疗法的关键作用机理
doi:10.1016/j.cell.2025.02.002
细菌免疫疗法,听起来像是科幻电影中的情节,但它确实是一种具有巨大潜力的抗癌策略。然而,要想充分发挥它的威力,科学家们需要解开一个复杂的谜题:细菌如何在逃避免疫系统“追杀”的同时,又能激活抗肿瘤免疫反应?近日,一项发表在Cell杂志上的研究为我们揭开了这一谜题的关键部分。
这项研究由中国科学院深圳先进技术研究院等机构的科学家们主导,他们通过基因工程改造了一种名为“设计细菌1”(DB1,Designer Bacteria 1)的减毒菌株。DB1在肿瘤组织中能够“安家落户”并大量繁殖,而在正常组织中则会被迅速清除,从而实现了精准的“肿瘤靶向”和“肿瘤清除”效果。
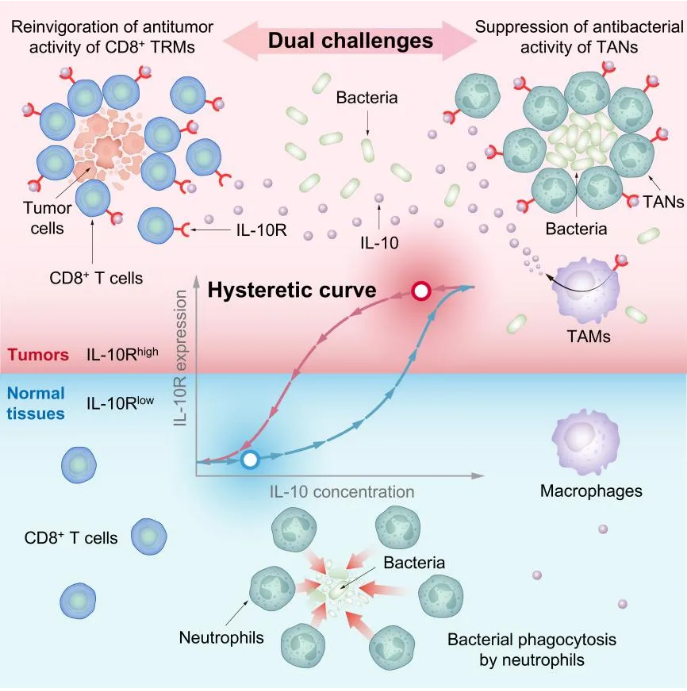
为了理解DB1如何做到这一点,研究人员深入研究了细菌与肿瘤之间的“互动”。他们发现,DB1的抗肿瘤效果与肿瘤中的组织驻留记忆CD8+ T细胞(TRM细胞)密切相关。这些细胞在DB1治疗后被重新激活并大量增殖,成为清除肿瘤的“主力军”。而这一过程的关键“推手”是一种名为白介素-10(IL-10)的细胞因子。
IL-10通过与TRM细胞上的IL-10受体(IL-10R)结合,激活了STAT3蛋白,进而促进了IL-10R的进一步表达。这种正反馈回路使得TRM细胞对IL-10的反应更加敏感,形成了一种“记忆效应”——即使在IL-10水平下降后,TRM细胞仍然保持高水平的IL-10R表达。这种“滞后效应”不仅帮助DB1逃避免疫系统的清除,还增强了TRM细胞的抗肿瘤活性。
【8】PNAS:琥珀酸维生素E或能有效控制肿瘤生长并增强免疫疗法的疗效
doi:10.1073/pnas.2407910121
高水平的脂肪量和肥胖相关蛋白(FTO)与肿瘤生长增加和对免疫疗法耐受相关。近日,一篇发表在国际杂志Proceedings of the National Academy of Sciences上题为“Targeting DTX2/UFD1-mediated FTO degradation to regulate antitumor immunity”的研究报告中,来自芝加哥大学等机构的科学家们通过研究发现,琥珀酸维生素E(VES,vitamin E succinate)或能作为一种有效的制剂,通过促进FTO的降解来控制肿瘤的生长。
表观遗传学和表观转录组学在不改变基因序列的前提下在修饰基因表达方面扮演着重要角色,N6-甲基腺苷(m6A, N6-methyladenosine)就是这样一种机制,即甲基基团能被添加到RNA上腺苷的N6位置,而添加这些甲基基团能增强RNA的稳定性,然而,利用酶类进行移除(比如FTO)就能促进肿瘤的发展。FTO是研究人员发现的首个m6A甲基化酶,如今其已经被证明在多种癌症中能被上调,这项研究中,研究人员通过研究识别出了能降解FTO的候选物质。
FTO甚至在其在RNA修饰过程中的作用被完全阐明之前就引起了肥胖研究领域科学家们的关注,研究者Yu-Ying He表示,早在2019年的研究中我们就观察到了黑色素瘤中FTO水平的升高,我们识别出了诸如紫外线辐射和砷暴露等环境因素会促进FTO水平的升高,从而导致黑色素瘤和其它癌症中RNA修饰水平减少。尽管目前研究人员已经识别出了多种小分子FTO抑制剂,但由于其未知或不良的毒性特性,这些抑制剂的临床用途仍然受到限制。
【9】Cell:科学家识别出能帮助癌细胞躲避CAR-T细胞免疫疗法的特殊蛋白
doi:10.1016/j.cell.2024.11.007
嵌合抗原受体(CAR)-T细胞免疫疗法治疗后B细胞恶性肿瘤患者的疾病长期持久缓解仍然不尽如人意,通常是由于患者机体的抗原逃逸所导致的,恶性B细胞转化和致癌生长依赖于有效的ATP合成,尽管其背后的潜在机制研究人员并不清楚。
近日,一篇发表在国际杂志Cell上题为“YTHDF2 promotes ATP synthesis and immune evasion in B cell malignancies”的研究报告中,来自希望之城贝克曼研究所等机构的科学家们通过研究找到了能帮助癌细胞躲避CAR-T细胞疗法的关键罪魁祸首,CAR-T细胞疗法能利用宿主机体的免疫系统寻找并杀死肿瘤细胞,这种疗法通常用于某些类型的白血病和淋巴瘤(诸如血液癌症),然而,一些狡猾的癌细胞已经学会了如何躲避宿主机体的免疫系统避免被破坏,相关研究结果有望帮助开发出更为个体化的疗法来改善癌症患者的生存情况。
文章中,研究者发现,名为YTHDF2的特殊蛋白在促进血液癌症的发生过程中扮演着重要角色,随后他们开发出了能靶向作用并抑制YTHDF2蛋白的新型药用化合物CCI-38,其能减少侵袭性血液癌症的生长,这种方法或能改善成功癌症疗法的可能性。Jianjun Chen博士说道,我们相信,利用CCI-38来靶向作用YTHDF2或能显著提高CAR-T细胞疗法对血液癌症细胞的治疗有效性。
【10】Sci Adv:科学家识别出一种隐蔽抗原或能作为针对卵巢癌的新型免疫疗法靶点
doi:10.1126/sciadv.ads7405
CD3+ T细胞和CD8+ T细胞向卵巢癌(OC,ovarian cancer)浸润的增加与患者更好的预后有关,但其背后所涉及的具体抗原研究人员并不清楚,最近有研究报道,HLA(人类白细胞抗原,human leukocyte antigen)I型能展现来自非编码基因组区域的肽类,其称之为非经典肽或隐肽,但其免疫原性特征尚未得到充分研究。
近日,一篇发表在国际杂志Science Advances上题为“Immunogenic cryptic peptides dominate the antigenic landscape of ovarian cancer”的研究报告中,来自梅奥诊所等机构的科学家们通过研究发现了一种名为隐蔽抗原(cryptic antigen)的新型免疫疗法靶点,其或许是帮助机体免疫系统抵御卵巢癌肿瘤的关键,相关研究结果或能帮助改善卵巢癌的治疗。
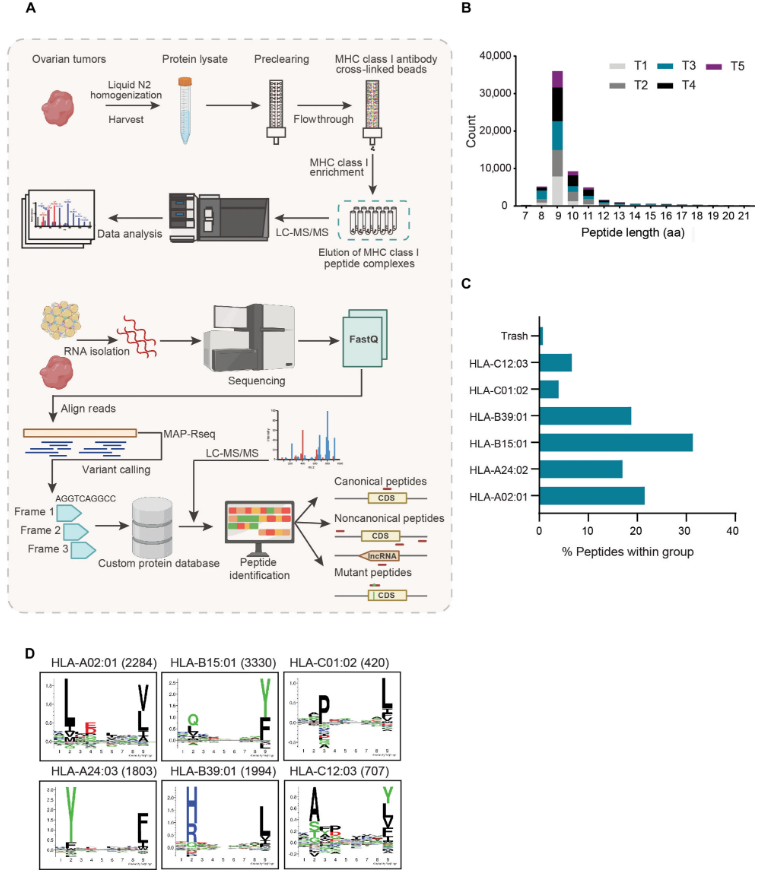
在卵巢癌中识别出HLA I型配体组
由于卵巢癌的疾病症状有限,其在扩散之前并不能被发现,在晚期阶段对其进行治疗就变得相当具有挑战性,而且当前的免疫疗法和检查点抑制剂疗法的成功率也非常有限。隐蔽抗原是称之为表位(epitopes)的蛋白质的一部分,其通常还是隐藏的或免疫系统无法进入的,或许存在于肿瘤细胞中,通过靶向作用这些抗原,免疫系统就能被有效动员起来并攻击癌症。
研究者Marion R. Curtis说道,这些研究发现强调了科学家们需要寻找卵巢癌靶向抗原替代来源的必要性,发现T细胞能识别的肿瘤相关抗原对于开发针对卵巢癌的免疫疗法的成功至关重要,在卵巢癌中,卵巢中细胞生长繁殖地速度较快且会入侵并摧毁机体健康的组织。T细胞是机体适应性免疫系统中的关键组分,其识别并对特殊靶点产生反应的能力对于其功能非常重要,而且其在癌症发生和治疗中也扮演着重要角色,对于机体免疫系统抵御感染至关重要。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


