《细胞》子刊:癌细胞真会“躲猫猫”!科学家发现散播肿瘤细胞逃避免疫杀伤之谜,竟然是T细胞遇不到它
来源:奇点糕 2024-02-06 11:39
Cyrus M. Ghajar等人提出三点应对策略,证明当添加数百万个能够识别和杀伤DTC的T细胞时,乳腺癌小鼠的免疫系统能够有效发挥监视作用并几乎全灭DTC。
1950年,物理学家恩里科·费米提出:如果银河系中存在大量的文明,那么为什么我们还没有发现它们的迹象?
是啊,这个问题同样困惑着免疫细胞。
少量散播肿瘤细胞(DTC)从乳腺癌等实体瘤脱落后,会在骨髓、肺部等部位休眠5年、10年、20年或更长时间,被唤醒后再次增殖活跃引起更加危险的转移性肿瘤。明明DTC就存在于那里且势单力薄,为何体内进行“星际巡游”的免疫细胞仍然无法清除掉它们呢?
关于费米悖论的解释有很多种,“黑暗森林法则”便是其一。对于免疫细胞的疑惑,美国Fred Hutchinson Cancer Center的Stanley R. Riddell、Cyrus M. Ghajar等人提出了“相对稀缺性”的概念,论文于近日发表在《癌细胞》期刊上[1]。
“相对稀缺性”的背后其实就是简单的概率问题。为了消灭威胁,免疫系统首先必须找到它们,但是放眼于偌大的人体“宇宙”,DTC数量太少了,能够摧毁它们的抗原特异性T细胞在庞大的免疫细胞群体中实际占比也并不够数,这导致两者可能根本不会有贴贴的机会!
对此,Cyrus M. Ghajar等人提出三点应对策略,证明当添加数百万个能够识别和杀伤DTC的T细胞时,乳腺癌小鼠的免疫系统能够有效发挥监视作用并几乎全灭DTC。

论文首页截图
在三阴性乳腺癌患者中,即使原发肿瘤在免疫检查点抑制剂治疗中达到了完全缓解,也无法激发足够强大的免疫反应来清除残留的散播肿瘤细胞(DTC),诱发更棘手的复发或转移性乳腺癌。
于是许多人认为,DTC使用了些小伎俩逃脱免疫监视,比如下调自身主要组织相容性复合物(MHC-I)的表达,这些分子对于免疫系统识别和清除肿瘤细胞至关重要,从而模糊T细胞的视线,避免被攻击。
起初,Cyrus M. Ghajar等人利用乳腺癌小鼠模型进行实验时也是得出此结论。他们发现,杀伤原发肿瘤后,骨髓中的抗原特异性CD8+T细胞保持着效应表型和记忆表型,即便如此DTC依旧存在,其MHC-I表达较增殖活跃的肿瘤细胞大大降低。
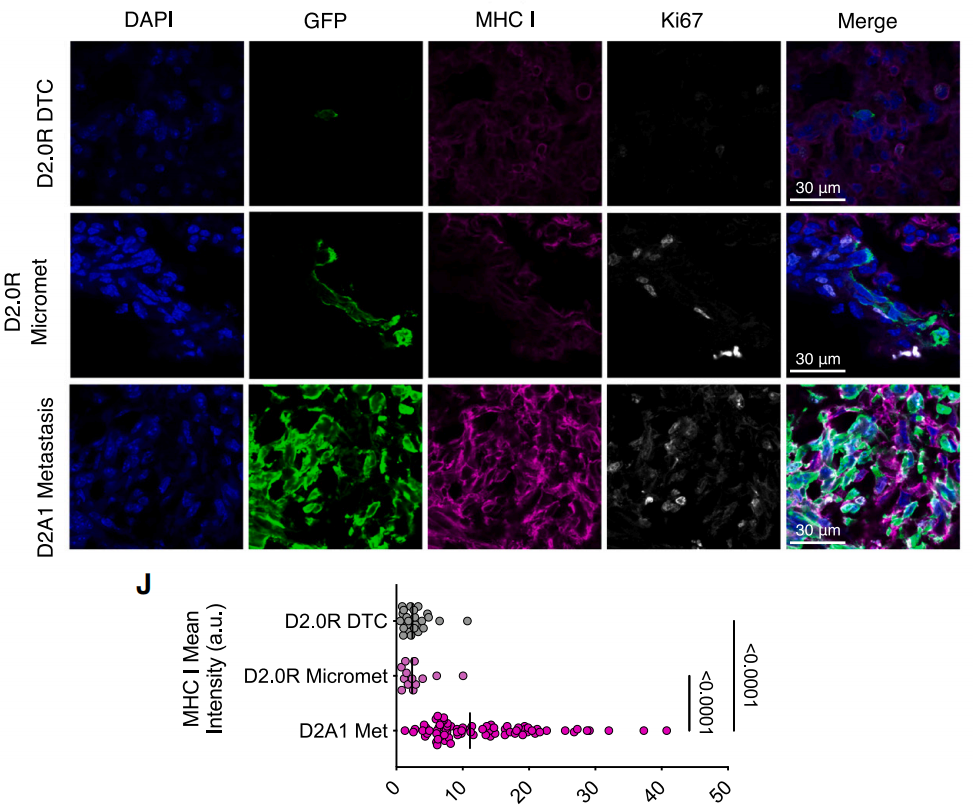
DTC的MHC-I表达水平降低
但他们很快就抛弃了这一想法。
在体外实验中模拟微血管环境时,可以观察到T细胞实际上是能够很凶猛地清除84%-97%的肿瘤细胞,无论其处于休眠还是增殖活跃状态。再或者,给免疫缺陷小鼠注射MHC-I表达水平低的肿瘤细胞之后,过继转移抗原特异性T细胞,也可以观察到显著的清除效果。
与此同时,仅使用低剂量IFN-γ增强小鼠DTC的MHC-I表达时,并不会提高T细胞的杀伤能力。
这些意味着,仅靠下调MHC-I的小伎俩,DTC无法与T细胞抗衡。尽管它的确通过降低MHC-I的表达来尝试逃避免疫监视,但这种降低程度并不足以阻止抗原特异性T细胞的有效识别和杀伤,说明还有其它因素发挥作用。
回想一下,到底哪个环节出了问题?
刚才考验T细胞的杀伤效果时,无论体外培养还是给小鼠过继转移T细胞,其实都有为T细胞与DTC创造更多的相遇机会,当过继转移的T细胞剂量加大时,两者之间直线距离缩短。
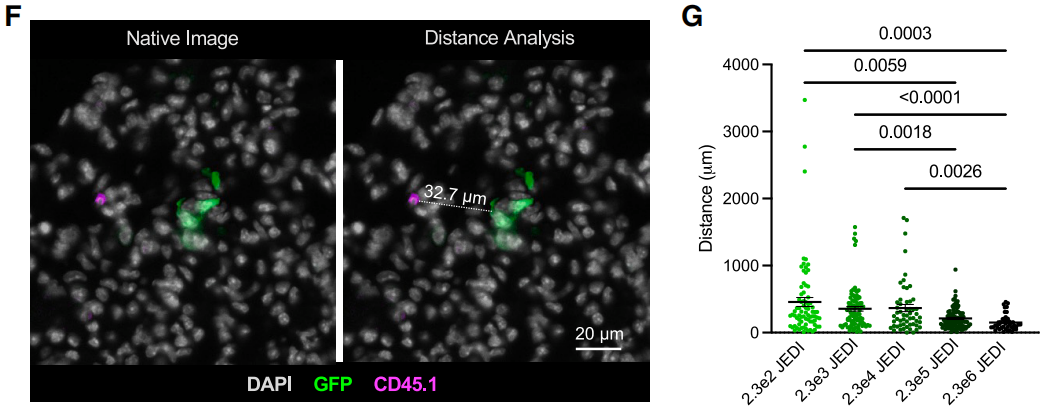
抗原特异性T细胞越多,与DTC之间的直线距离越短
这让研究者们提出一个大胆的假设——并非T细胞打不过,只是它们压根碰不到面儿而已!
经验证,果真如此,研究者们将这个现象称为“相对稀缺性”。他们通过使用几种策略来提高抗原特异性T细胞与DTC的比率、增加两者相互作用的频率,结果都实现了有效杀伤。
第一种策略是注射T细胞疫苗,激发乳腺癌小鼠自身抗原特异性CD8+T细胞的扩增约18倍,可清除肺内53%的DTCs。
第二种策略是T细胞受体基因改造T细胞疗法(TCR-T),将小鼠自身T细胞上表达的天然受体进行改造,使它们能够更好地识别肿瘤细胞特异性抗原,体外培养后过继转移给小鼠,清除效率为79%-87%。
第三种策略是嵌合抗原受体T细胞疗法(CAR-T),这回是给小鼠自身T细胞上配备一些新式武器以进行武力升级,体外培养后过继转移给小鼠,清除效率可达98%。
为了进一步测试临床转化价值,研究者们在高表达人类HER2的乳腺癌小鼠模型中进行验证。结果显示,使用曲妥珠单抗衍生的HER2靶向CAR-T细胞[2](该药物已处于I期临床试验[NCT 03500991])治疗,能够有效清除小鼠肺部62%-74%的DTCs。
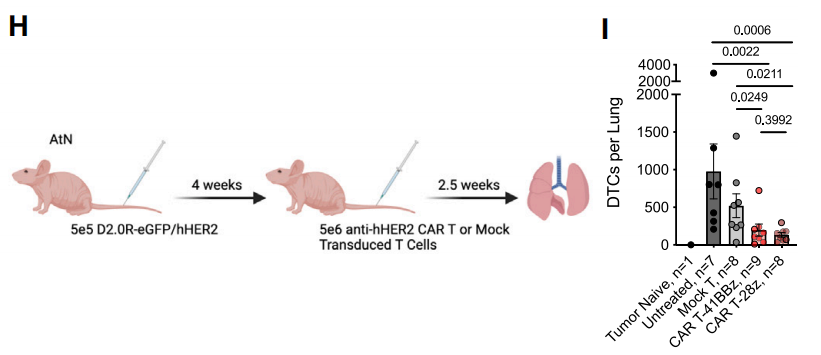
HER2特异性CAR-T细胞有效清除DTC
总之,按照Cyrus M. Ghajar等人首次揭示的“相对稀缺性”免疫逃逸机制来看,既然DTC的MHC-I表达降低对于T细胞杀伤来说不是什么难事儿,那么我们所要考虑的便是如何为抗原特异性T细胞创造与猎物相遇的机会,这为减少DTC残留、避免复发或转移性肿瘤的发生提供了有趣的见解。
但这只是一个课题的开端。因为研究者们发现,不管是依靠TCR-T细胞疗法、CAR-T细胞疗法获得增援,还是靠疫苗提高内源性T细胞的数量,虽然扩大T细胞的势力能够有效杀伤DTC,可终究无法达到100%完全清除,仍有零星残余。
同期发表的评论文章中提及[3],如果将Cyrus M. Ghajar等人的策略与免疫检查点抑制剂等免疫疗法相结合,或许可进一步根除DTC。或者也可以动员其它免疫细胞,如巨噬细胞、树突状细胞、自然杀伤细胞等,尽可能降低DTC造成的危害。
话说回来,几个月,上海交通大学医学院附属仁济医院翟博领衔的研究团队,在著名期刊《癌症通讯》上发表了的一项重磅研究成果,表明CAR-T细胞或许可以消除术后肝癌的微小病灶和循环肿瘤细胞(CTC),从而实现抑制肝癌的复发。
这个方向很值得一试啊!
参考文献:
[1]https://www.cell.com/cancer-cell/fulltext/S1535-6108(23)00439-7
[2]Vitanza, N.A., Johnson, A.J., Wilson, A.L. et al. Locoregional infusion of HER2-specific CAR T cells in children and young adults with recurrent or refractory CNS tumors: an interim analysis. Nat Med 27, 1544–1552 (2021). https://doi.org/10.1038/s41591-021-01404-8
[3]Adam-Artigues, A., Valencia Salazar, L. E., & Aguirre-Ghiso, J. A. (2024). Immune evasion by dormant disseminated cancer cells: A Fermi paradox?. Cancer cell, 42(1), 13–15. https://doi.org/10.1016/j.ccell.2023.12.017
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


