JEV | 苏佳灿/郑磊/井莹莹/王思成发现骨质疏松症的潜在治疗新策略
来源:生物探索 2024-04-11 09:35
该研究进一步证明了BEVs,特别是益生菌EVs在骨退行性疾病中的潜力,为OP治疗提供了创新的解决方案。
上海交通大学、上海大学及南方医科大学多单位合作,苏佳灿、郑磊 、井莹莹及王思成共同通讯在Journal of Extracellular Vesicles 在线发表题为“Synthetic biology-based bacterial extracellular vesicles displaying BMP-2 and CXCR4 to ameliorate osteoporosis”的研究论文,该研究表明基于合成生物学的细菌细胞外囊泡显示BMP-2和CXCR4以改善骨质疏松症。
该研究构建了重组益生菌大肠杆菌Nissle 1917-pET28aClyA-BMP-2-CXCR4 (ECN-pClyA-BMP-2-CXCR4),其中BMP-2和CXCR4与BEVs表面蛋白ClyA融合过表达。随后,分离出工程化BEVs-BMP-2-CXCR4 (BEVs-BC)用于OP治疗。工程BEVs-BC在体内表现出良好的骨靶向性。BEVs-BC具有良好的生物相容性,促进骨髓间充质干细胞成骨分化的能力显著。最后,基于合成生物学的BEVs-BC显著阻止了卵巢切除(OVX)小鼠模型的OP。综上所述,该研究利用合成生物学技术一步构建了集骨靶向和成骨于一体的BEVs-BC,为OP提供了一种有效的策略,具有很大的产业化潜力。

骨质疏松症(Osteoporosis, OP)是一种以骨量减少、骨组织变薄、骨脆性增加为特征的系统性疾病。OP骨折(OPF)是OP最常见的并发症,具有高发病率、高致残率、高死亡率和高医疗费用的特点,严重影响老年患者的生活质量。然而,现有的生物材料和常规方法在治疗OP和OPF方面的效果往往有限。成骨细胞和破骨细胞之间的代谢失衡往往会导致OP。几种促进成骨细胞活性和抑制破骨细胞吸收的药物已被美国食品和药物管理局(FDA)批准。然而,这些药物有一些局限性,包括增加心血管不良反应、病理性骨折、骨肿瘤和免疫功能障碍的风险,这严重限制了它们的临床应用。因此,迫切需要更有效、更安全的方法来治疗OP。
BMP-2是一种众所周知的生长因子,具有促进骨再生和增加骨强度和密度的能力,被广泛用于治疗OP及其并发症。由于其半衰期短,保留效率低,BMP-2不能单独注射。但直接大规模给药可引起严重并发症。因此,仍然需要具有控释系统的先进生物材料来使BMP-2有效地促进骨修复。近年来,越来越多的研究利用细胞外囊泡(extracellular vesicles, EVs)调节骨代谢来治疗OP,因为EVs具有独特的纳米结构、稳定的载药能力和良好的给药生物相容性。
血管内皮细胞衍生的EVs可传递miR-155抑制破骨细胞分化以改善OP。工程化的NIH-3T3细胞衍生的EVs可以传递antagomir-188,促进成骨细胞分化,缓解OP。此外,薯蓣衍生的EVs可以激活骨形态发生蛋白-2 (BMP-2)/p-p38依赖的Runx2途径来预防OP。尽管这些天然和工程化的EVs,包括哺乳动物细胞EVs(MEVs)和植物源性EVs(PEVs)已经显示出良好的治疗效果,但复杂的工程修饰和较低的提取效率严重限制了它们的临床应用。
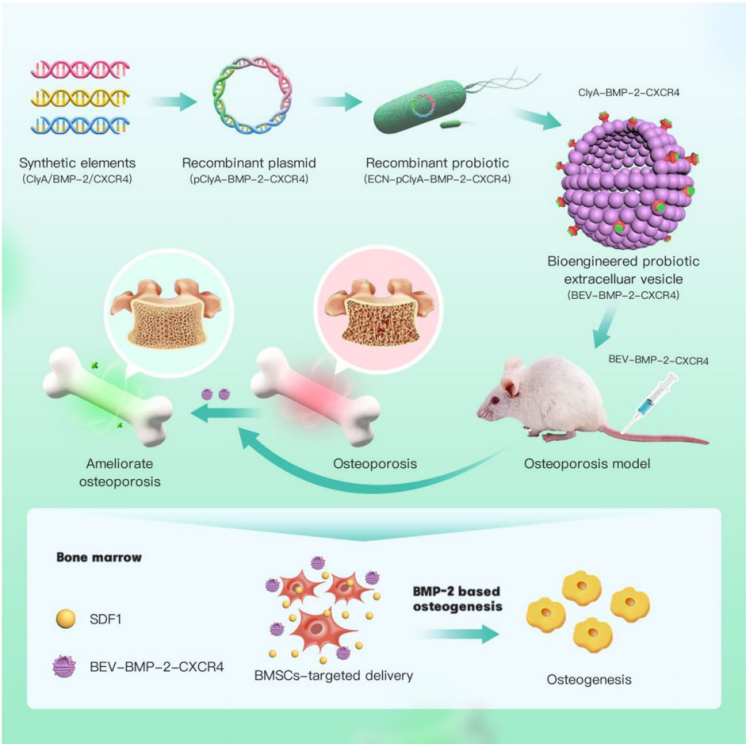
模式图(Credit: Journal of Extracellular Vesicles)
随着合成生物学的快速发展,利用细菌源性EVs(BEVs)成为给药系统中的一颗新星。细菌具有大规模发酵、丰富的基因编辑手段和成熟的高密度发酵技术等优势,使BEVs具有易于工程修饰和临床翻译的特殊特点。BEVs已被报道调节骨代谢和OP的进展。
在之前的研究中,通过对大肠杆菌Nissle 1917 (ECN)进行修饰,使其过表达CXCR4,使BEVs具有骨靶向特性。骨靶向生物工程BEVs- CXCR4可以装载和递送外源性SOST siRNA来改善OP。BEVs-CXCR4-SOST siRNA为OP提供了创新高效的治疗方案。然而,低电穿孔效率严重阻碍了其临床转化过程。因此,利用合成生物学技术一步构建具有骨靶向和骨治疗作用的BEVs具有重要意义。
该研究通过合成生物学方法,构建了一种重组益生菌ECN-pClyA-BMP-2-CXCR4。经过简单的发酵和纯化,我们可以获得具有骨靶向和骨治疗特性的大规模生物工程BEVs-BC。该生物工程BEVs-BC可以靶向骨髓中的BMSCs,通过BMP/SMAD信号通路促进成骨分化,抑制其成脂分化,最终改善OVX诱导的骨质流失。该研究进一步证明了BEVs,特别是益生菌EVs在骨退行性疾病中的潜力,为OP治疗提供了创新的解决方案。重要的是,该研究开发了一种易于获得且功能强大的骨修复生物材料,为未来的临床应用奠定了坚实的基础。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


