《自然·医学》:3名晚期肝癌患者肿瘤完全消失!个体化新抗原癌症疫苗联合PD-1抑制剂果然身手不凡
来源:奇点糕 2024-04-13 13:51
本次公布结果的GNOS-PV02临床I/II期研究,共纳入了36例已接受过仑伐替尼/索拉非尼治疗的晚期肝细胞癌(HCC)患者。
刚刚在美国癌症研究协会(AACR)年会上报告,并以论文形式同步发表在《自然·医学》上的一项最新临床研究[1]数据,就展示了达成肝癌CR这个“Mission Impossible”的一种可能性:为肝癌患者量身定制、编码至多达40个肿瘤新抗原的个性化癌症治疗疫苗GNOS-PV02,与PD-1抑制剂联合用于肝癌患者的后线治疗时,仍有着良好的抗肿瘤活性和出色的安全性,其中3例患者达到了CR!个体化疫苗果然是出手不凡啊。

论文首页截图
相信看过最近几年的研究进展,各位对编码新抗原的治疗性疫苗如何通过激活免疫应答起效都很熟悉,奇点糕也就不多啰嗦作用机制的事情了,不过GNOS-PV02的设计还是值得一提:这款疫苗递送的是DNA质粒,对应在患者肿瘤DNA/RNA测序中找到的肿瘤新抗原,同时还以编码白介素-12(IL-12)的DNA质粒作为佐剂,以皮下注射的方式给药。
本次公布结果的GNOS-PV02临床I/II期研究,共纳入了36例已接受过仑伐替尼/索拉非尼治疗的晚期肝细胞癌(HCC)患者,即GNOS-PV02联合PD-1抑制剂帕博利珠单抗是用于二线治疗;在首先考量的安全性方面,患者未报告≥3级的治疗相关不良事件(TRAEs),且无患者因TRAEs停用GNOS-PV02(1例患者因TRAEs停用帕博利珠单抗)。
而作为研究次要终点的客观缓解率(ORR)才是吸睛的焦点:在已完成≥1次疗效评估的34例患者中,有11例患者达到客观缓解,即全部患者经研究者评估的ORR为30.6%(11/36),其中就包括3例CR,且已有9例缓解在后续疗效评估中被证实;与PD-1抑制剂单药治疗的历史ORR数据(12-18%)相比,加入GNOS-PV02已实现了有显著性的提升(p=0.031)。
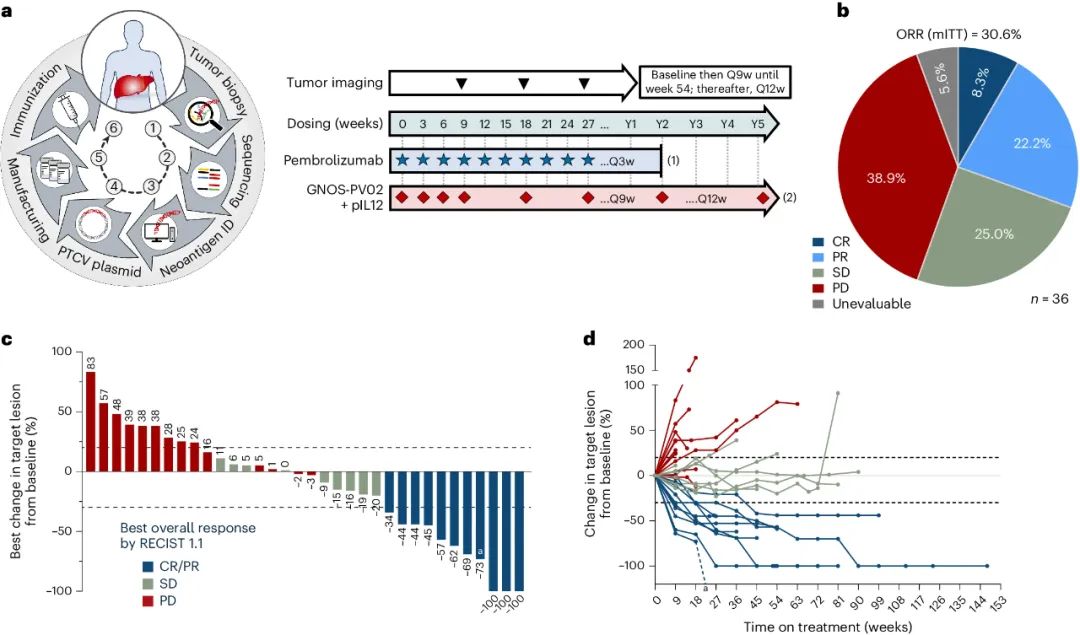
此次研究的疗效数据汇总
38例患者中有3例CR看似不算多,但在此前仑伐替尼/索拉非尼单药治疗的时代,能达到CR的晚期HCC患者往往只有1%左右[2],即使现在是靶免联合治疗时代,它们在一线治疗中的CR率也就是8%的水平[3],而GNOS-PV02还是用在难度更大的二线治疗。此外,全部患者的中位无进展生存期(mPFS)为4.2个月,中位总生存期(mOS)为19.9个月。
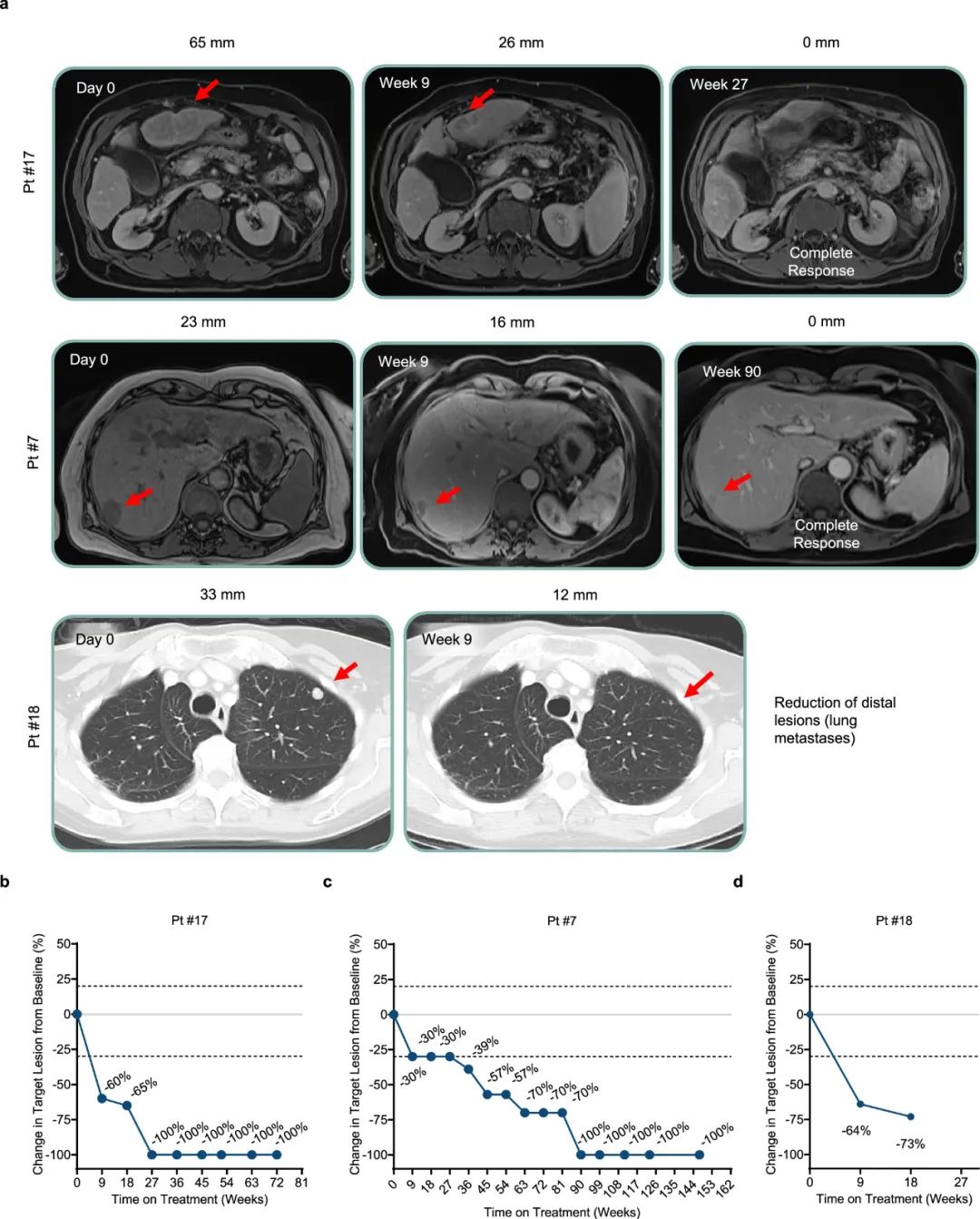
部分应答较好患者的缩瘤情况
免疫原性分析则显示,无论是否经治疗实现缓解,几乎所有患者血样内均可检测到新抗原特异性的T细胞应答,且较治疗前应答强度有明显提升,表现为干扰素γ(IFNγ)应答增强,且CD4+/CD8+T细胞均呈现更好的激活状态,外周血中的各类T细胞克隆均有明显扩增,并向肿瘤部位大量浸润,它们也是响应个体化疫苗递送新抗原的主力军。
但是个体化疫苗毕竟不是无敌的,研究者们以1例先达到部分缓解(PR),但未能持久抑癌的患者为例,描述了癌细胞通过免疫编辑(Immune Editing)实现治疗逃逸的过程,该患者肝脏靶病灶一度缩小了近60%(治疗18周时),但同时在肾上腺检出了新病灶;分析显示,4种经个体化疫苗递送、可激活T细胞强烈应答的新抗原,在肾上腺转移灶中都消失了,这就使CD8+T细胞失去了识别靶标,对肾上腺转移灶的浸润程度远远低于肝脏靶病灶。
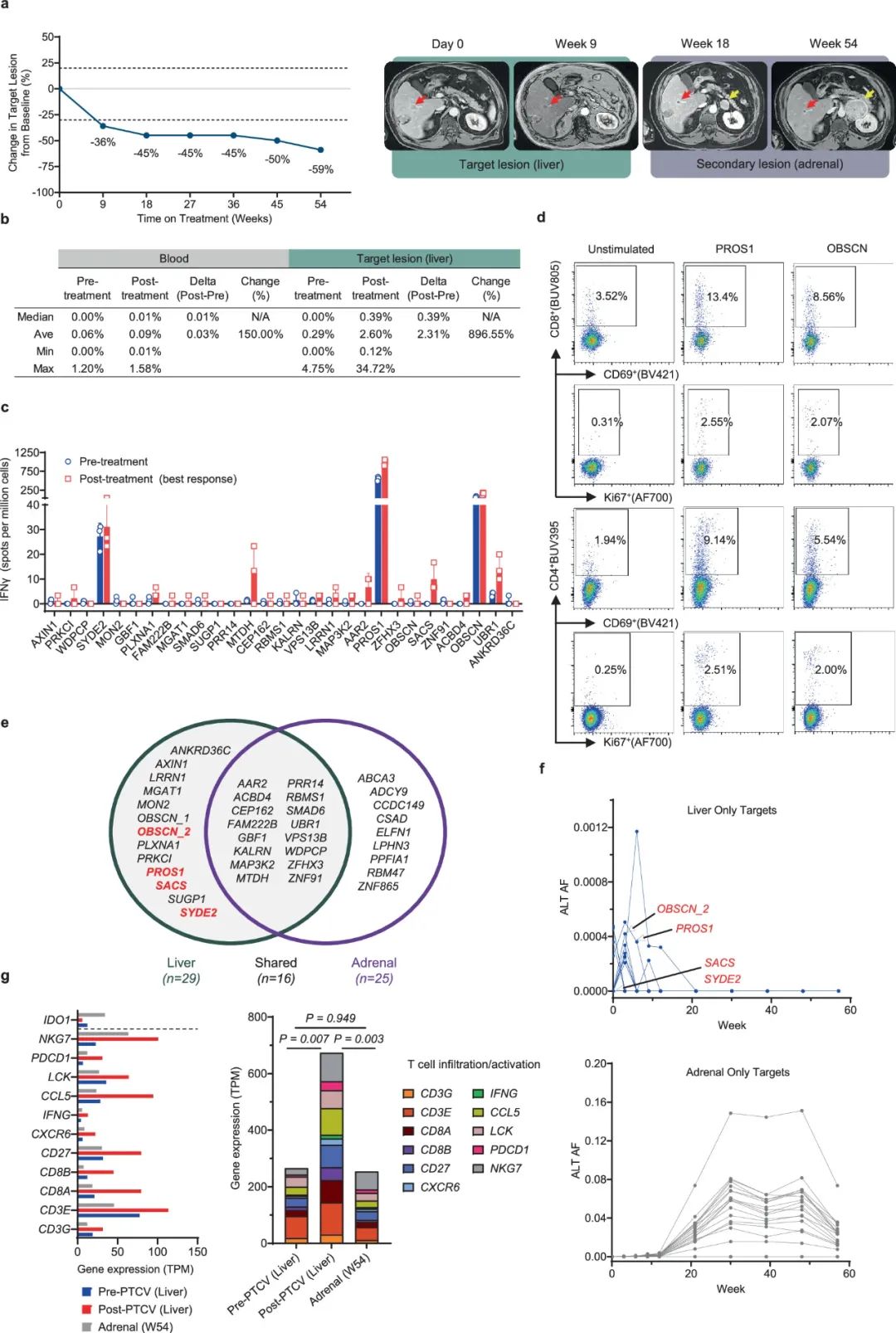
癌细胞可通过免疫编辑躲避个体化疫苗的打击
此外,研究还专门进行了生物标志物层面的分析,发现患者血样中ctDNA的降幅与治疗应答和患者生存预后挂钩,个体化疫苗可编码≥30个新抗原患者的ORR也相对较高(41.2% vs. 23.5%),但患者肿瘤突变负荷(TMB)和基线时甲胎蛋白(AFP)水平不具明显预测价值,研究也没能揭示其它可在治疗前预测疗效的生物标志物。
虽说有了靶向和免疫治疗,但HCC的精准治疗其实还处在“多多益善”的阶段,不管是什么样的手段,只要有效安全就有广阔舞台,而GNOS-PV02这款个体化疫苗绝对有成为舞台明星的潜力,就看未来它的研发和使用要怎么继续推进啦。
参考文献:
[1]Yarchoan M, Gane E J, Marron T U, et al. Personalized neoantigen vaccine and pembrolizumab in advanced hepatocellular carcinoma: a phase 1/2 trial[J]. Nature Medicine, 2024.
[2]Kudo M, Finn R S, Qin S, et al. Lenvatinib versus sorafenib in first-line treatment of patients with unresectable hepatocellular carcinoma: a randomised phase 3 non-inferiority trial[J]. The Lancet, 2018, 391(10126): 1163-1173.
[3]Cheng A L, Qin S, Ikeda M, et al. Updated efficacy and safety data from IMbrave150: Atezolizumab plus bevacizumab vs. sorafenib for unresectable hepatocellular carcinoma[J]. Journal of Hepatology, 2022, 76(4): 862-873.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


