《癌细胞》:mRNA抗癌疗法立大功!BioNTech团队发现,IL-2的mRNA可以让隐身的癌细胞显形
来源:奇点糕 2024-03-18 10:05
研究者们使用LPP纳米递送平台封装了IL-2 mRNA(且融合了人血清白蛋白),将mRNA精准递送到肝细胞再翻译为IL-2蛋白,显著延长了IL-2半衰期,且无明显不良反应。
在《癌细胞》(Cancer Cell)上,因开发mRNA疫苗而声名大噪的BioNTech公司创始人Ugur Sahin与同事发表的最新研究成果显示:用编码白介素-2(IL-2)的mRNA作为治疗手段,可使IL-2成为长效性治疗手段,逆转因癌细胞缺少MHC-I类分子表达而沦为“免疫沙漠”的肿瘤微环境,破解免疫治疗等众多现有抗癌治疗遭遇的耐药。
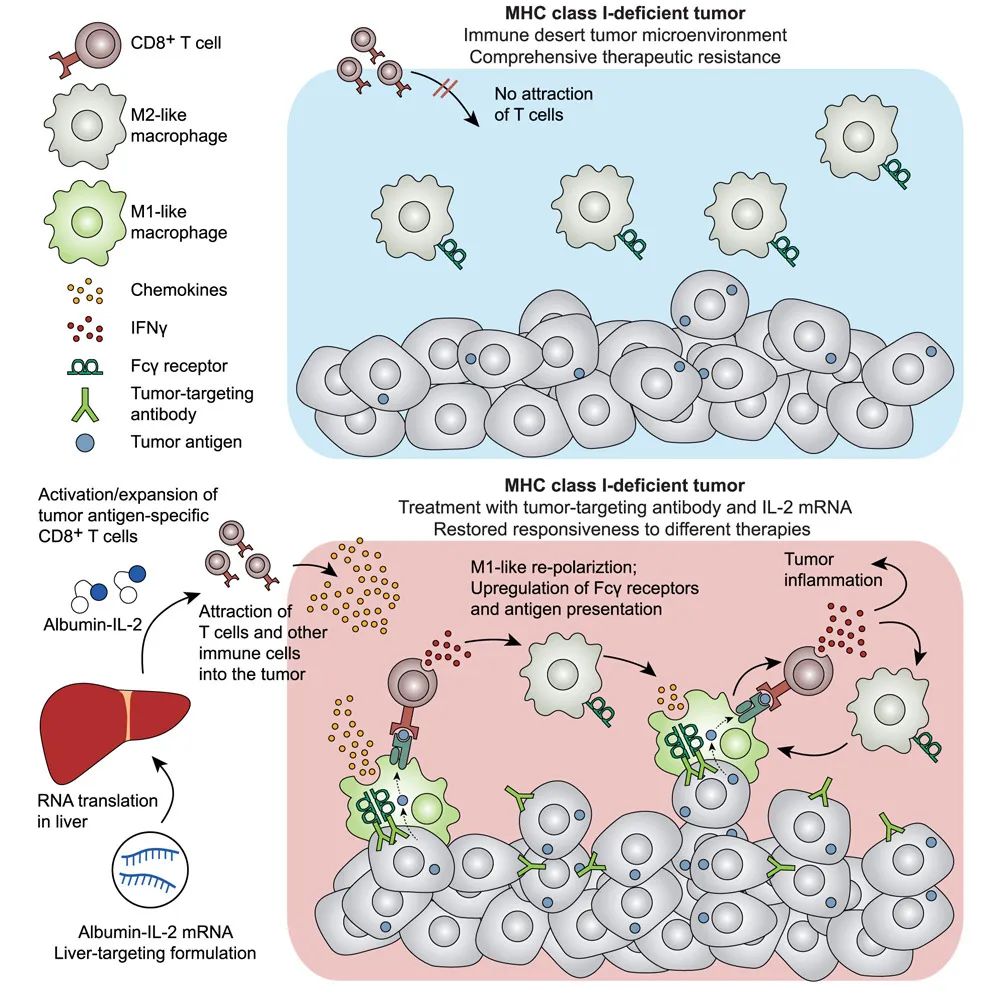
论文核心内容总结
熟悉免疫治疗的读者们,可能早几年就听说过“免疫沙漠”型肿瘤的概念,这片沙漠表征是肿瘤极度缺少免疫细胞浸润,免疫检查点抑制剂治疗因此也巧妇难为无米之炊;而导致沙漠形成的要素之一,就是癌细胞MHC-I类分子表达缺失导致的抗原呈递减少。
而且,“免疫沙漠”影响的绝不仅仅有免疫治疗:BioNTech研究团队通过敲除癌细胞B2m基因(其编码的B2M是所有MHC-I类分子必要组分),在小鼠身上模拟了MHC-I类分子表达缺失的影响,发现化疗、放疗等治疗手段,到了极其缺少免疫细胞浸润的沙漠里,疗效同样会大幅下降,连起效机制和MHC-I类分子关系不大的单抗类靶向药也逃脱不了魔爪。
那问题来了,该怎么才能逆转MHC-I类分子表达缺失的影响呢?研究者们注意到,敲除B2m基因的“免疫沙漠”肿瘤中,许多细胞因子和趋化因子表达也显著下调,其中就有此次研究的主角——IL-2。此前有研究显示,使用IL-2或IL-2通路激动剂可激活NK细胞,而NK细胞对癌细胞的杀伤并不依赖抗原呈递,这样就能绕开MHC-I类分子表达缺失的障碍。
但由于IL-2在体内的半衰期很短,直接注射IL-2治疗会导致种种不便乃至副作用,这时就该让BioNTech引以为傲的mRNA技术出场了:研究者们使用LPP纳米递送平台封装了IL-2 mRNA(且融合了人血清白蛋白),将mRNA精准递送到肝细胞再翻译为IL-2蛋白,显著延长了IL-2半衰期,且无明显不良反应,这种mRNA编码的长效IL-2疗法就进入了下一步实验。
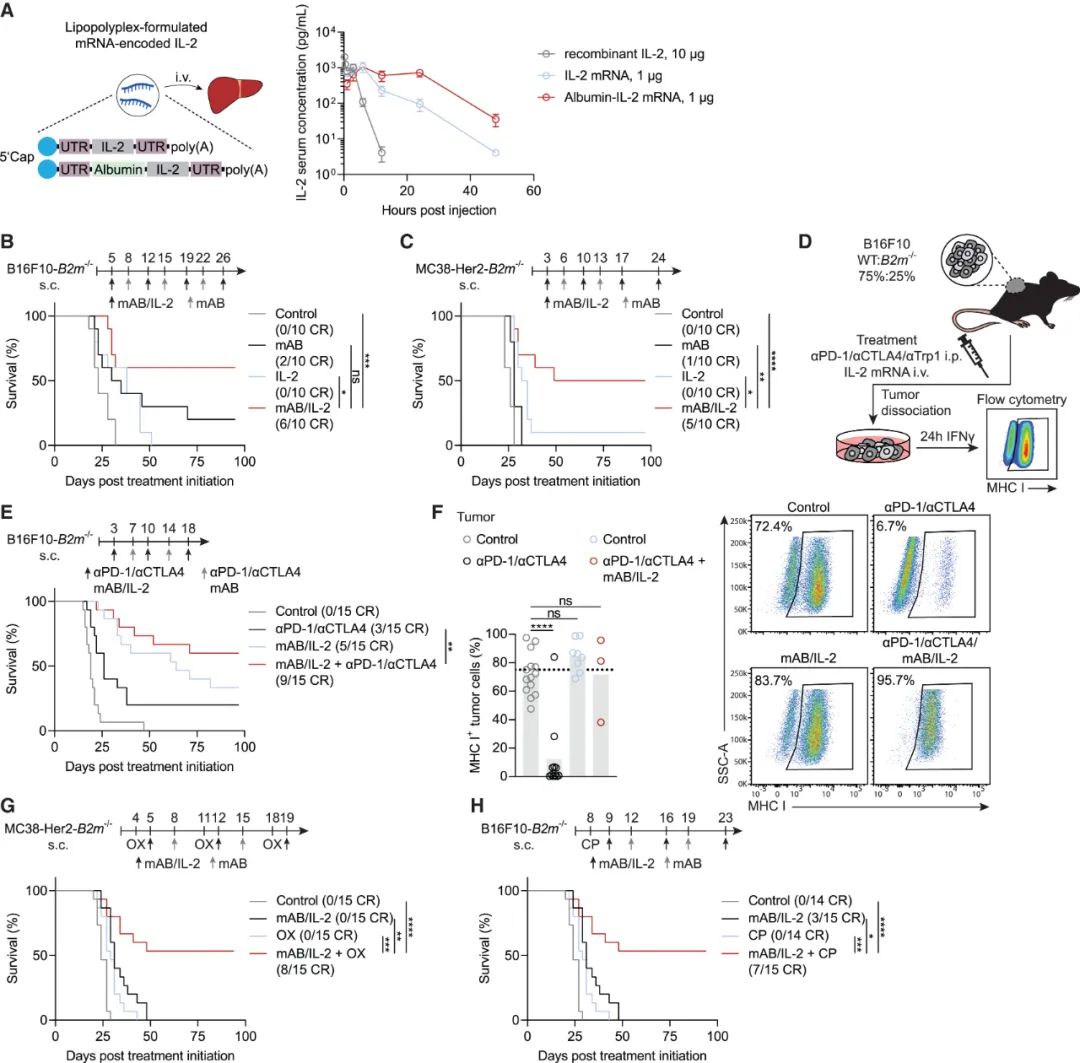
mRNA技术加持让IL-2疗法更实用
研究者们在两个不同的MHC-I类分子表达缺失肿瘤小鼠模型中,将长效IL-2疗法与单抗类靶向药(分别靶向HER2、Trp2)联合使用,发现联合治疗都能够有效抑制肿瘤生长、提高小鼠的长期生存率,还使肿瘤对化疗更为敏感;在长效IL-2疗法与单抗类靶向药的基础上,再联合PD-1抑制剂或CTLA-4抑制剂联合治疗,还能进一步克服MHC-I类表达缺失癌细胞的过度生长。
接下来,就该分析长效IL-2疗法的破局作用机制了:不管是长效IL-2疗法单独使用还是联合单抗类靶向药,都足以改变“免疫沙漠”微环境中缺少免疫细胞浸润的状态,浸润显著增多的包括CD25+CD8+T细胞、CD25+CD4+常规T细胞及KLRG1+NK细胞等,它们的基因表达特征也呈明显的“炎症型”,但其中对抗癌最为关键和不可或缺的当然还是CD8+T细胞。
不过研究者们发现,如果用CSF1R抗体清除掉微环境中的巨噬细胞,也会使长效IL-2疗法+单抗类靶向药联合治疗的作用基本归零,且这些巨噬细胞整体向着有利抗癌的M1型(M1-TAM)极化,共刺激分子配体CD80/CD86表达水平极高,说明它们是激活CD8+T细胞的关键。
巨噬细胞的关键作用是怎么来的呢?进一步分析显示,这些巨噬细胞的抗原呈递相关基因(如H2-Q7、H2-Aa)表达均显著上调,而且受长效IL-2激活的CD8+T细胞会产生干扰素γ(IFNγ),IFNγ则会作用于巨噬细胞,使它们发生显著的重编程,具备抗体依赖性细胞介导的吞噬作用(ADCP)功能,从而吞噬癌细胞并交叉呈递肿瘤新抗原给CD8+T细胞。
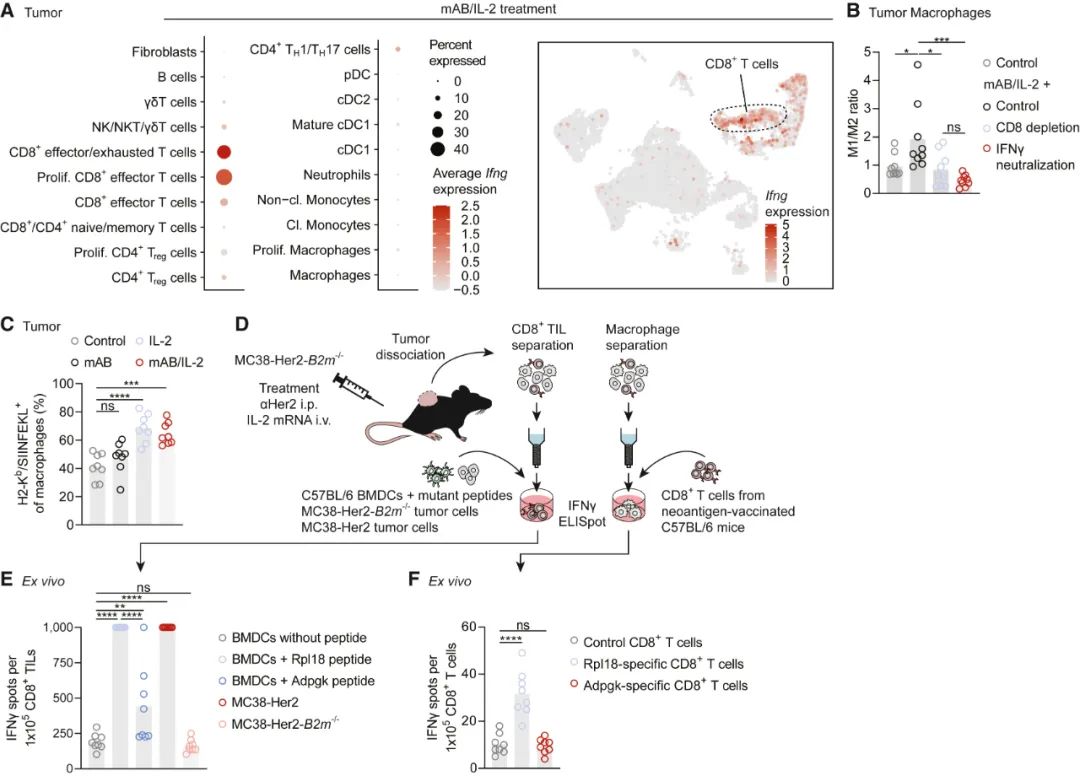
长效IL-2疗法激活的CD8+T细胞和巨噬细胞,可发生肿瘤新抗原交叉呈递
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


