苏州大学陈倩/刘庄团队通过调节肥胖相关肿瘤微环境,提高癌症免疫治疗效果
来源:生物世界 2023-02-27 11:32
该研究开发了一种调节肥胖相关肿瘤微环境的新策略,为肥胖相关肿瘤的免疫治疗提供了有益参考。
由于不健康的饮食习惯及其他因素,全球约有20亿人超重或肥胖。肥胖通常会引起机体的全身性代谢紊乱,从而导致血脂异常、高胆固醇血症、激素水平改变和炎症等等。此外,肥胖还有助于肿瘤的发生和发展。肥胖还会诱导肿瘤微环境(TME)改变,这可能会进一步影响各种癌症治疗的结果,包括肿瘤免疫治疗。
肿瘤免疫治疗是一种革命性的癌症治疗策略,在临床上取得了巨大进展。然而,对于肥胖患者而言,他们的肿瘤免疫治疗通常应答率较低。肥胖会增加免疫老化,导致T细胞衰老,抑制T细胞反应。此外,肥胖引起的肿瘤微环境(TME)局部代谢改变能够影响癌细胞与免疫细胞之间的相互作用。
最近有研究显示,肥胖会下调癌细胞中的脯氨酸羟化酶-3(PHD3)的表达,导致癌细胞耗尽脂肪酸燃料,并显著影响TME中CD8+ T细胞的激活。因此,肥胖相关的TME与较差的抗肿瘤免疫反应密切相关,可能是肿瘤免疫治疗的重要预后因素。
近日,苏州大学陈倩教授、刘庄教授及同济大学附属上海市肺科医院杨洋教授等在 ACS Nano 期刊发表了题为:Regulating the Obesity-Related Tumor Microenvironment to Improve Cancer Immunotherapy 的研究论文。
该研究表明,肥胖会加重免疫抑制性肿瘤微环境(TME),研究团队开发了一种高效基因递送载体——HPD(HA/PEI-Tos/pDNA),能够有效上调肿瘤组织中PHD3的表达,修正免疫抑制性肿瘤微环境(TME),显著增加CD8+ T细胞浸润,从而提高免疫检查点抑制剂介导的免疫治疗的反应性。

肥胖通常会引起全身性代谢紊乱,包括肿瘤微环境(TME)。这是因为在脯氨酸羟化酶-3(PHD3)低水平的TME中,与肥胖相关的适应性代谢耗尽了CD8+ T细胞的主要脂肪酸燃料,导致CD8+ T细胞浸润不良,功能异常。
在这项最新研究中,研究团队发现,肥胖会加重免疫抑制性肿瘤微环境(TME),削弱CD8+ T细胞介导的肿瘤细胞杀伤作用。因此,研究团队开发了一种基因疗法来缓解肥胖相关的肿瘤微环境(TME),以促进癌症免疫治疗。
研究团队通过对甲基苯磺酰改性聚乙烯亚胺(PEI-Tos),结合透明质酸(HA),制备了一种高效基因递送载体——HPD(HA/PEI-Tos/pDNA),该载体可在静脉注射后实现良好的肿瘤转染。
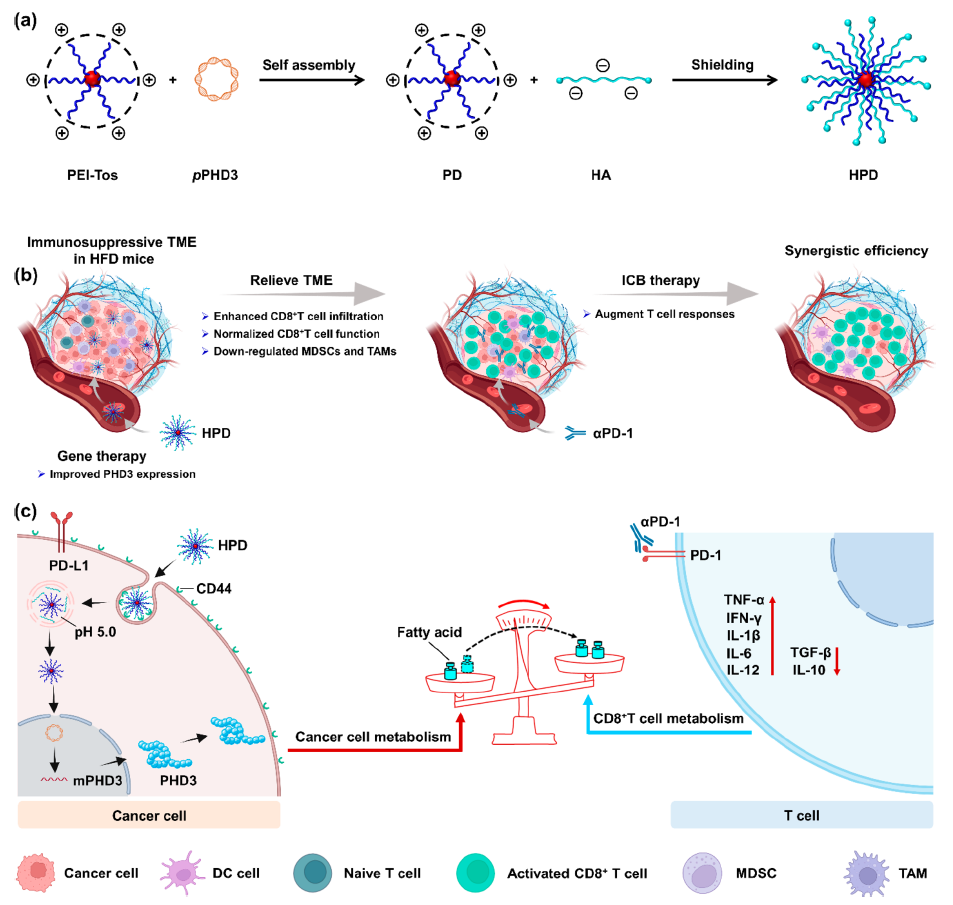
通过HPD载体递送编码脯氨酸羟化酶-3(PHD3)的质粒DNA,可有效上调肿瘤组织中PHD3的表达,修正免疫抑制性肿瘤微环境(TME),显著增加CD8+ T细胞浸润,从而提高免疫检查点抑制剂介导的免疫治疗的反应性。将HPD疗法联合抗PD-1单抗(αPD-1),对患有结直肠癌或黑色素瘤的肥胖小鼠均有良好的治疗效果。
总的来说,该研究开发了一种调节肥胖相关肿瘤微环境的新策略,为肥胖相关肿瘤的免疫治疗提供了有益参考。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


