J Exp Clin Cancer Res:肿瘤代谢物消除癌症发生/进展中的肿瘤抑制功能
来源:生物谷原创 2022-05-23 19:05
全世界每年有多达30万人被诊断为肾细胞癌,透明细胞肾细胞癌(CcRCC)是主要的组织学亚型(∼占所有肾细胞癌的80%)。
全世界每年有多达30万人被诊断为肾细胞癌,透明细胞肾细胞癌(CcRCC)是主要的组织学亚型(∼占所有肾细胞癌的80%)。CcRCC起源于肾单位近曲小管上皮细胞,von Hippel Lindau(VHL)基因失活是其发病机制的早期事件。
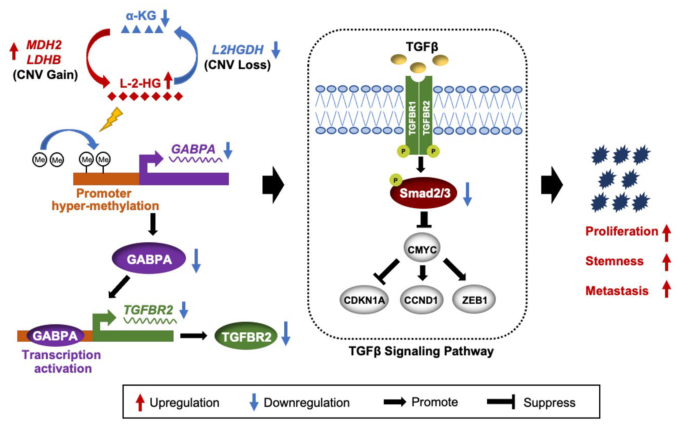
Ets转录因子GABPA长期以来被认为是一种致癌因子,最近被认为是癌症治疗的靶点,因为它对端粒酶活性具有关键作用,但GABPA在肾透明细胞癌(CcRCC)中的作用尚不清楚。此外,ccRCC的特点是代谢重编程并异常积聚L-2-羟基葡萄糖酸(L-2HG),这是一种已被证明通过诱导DNA甲基化促进ccRCC发生和进展的肿瘤代谢物,但其下游效应分子仍未明确。

图片来源: https://doi.org/10.1186/s13046-022-02382-6
近日,山东大学齐鲁医院的研究者们在J Exp Clin Cancer Res杂志上发表了题为“GABPA-activated TGFBR2 transcription inhibits aggressiveness but is epigenetically erased by oncometabolites in renal cell carcinoma”的文章,该研究使用DNA甲基化抑制剂或其他方法恢复GABPA的表达,而不是靶向它,可能是ccRCC治疗的一种新策略。
SiRNAs和表达载体用于调控GABPA和其他因子的表达,并确定细胞/分子和表型的变化。RNA测序和芯片分析鉴定GABPA靶基因。研究者采用小鼠人肾小管上皮细胞癌移植模型,观察GABPA过表达对体内肿瘤发生和转移的影响。用L-2-HG孵育ccRCC细胞,分析GABPA的表达和甲基化情况。研究者对患者标本进行了免疫组织化学和TCGA数据集分析,以评估GABPA对ccRCC生存的影响。
GABPA的缺失虽然抑制了端粒酶的表达,但显著促进了肾癌细胞的增殖、侵袭和干细胞分化,而GABPA的过表达则表现出相反的作用,强烈地抑制了体内的转移和癌变。TGFBR2被确定为GABPA的靶基因,GABPA通过调控转化生长因子β信号来决定ccRCC的表型。
GABPA和TGFBR2在肾细胞癌细胞中相互表型复制。GABPA或TGFBR2的高表达预示着ccRCC患者较长的生存期。CcRCC细胞与L-2-HG孵育可模拟GABPA基因敲除介导的表型改变。L-2-HG通过增加GABPA甲基化抑制GABPA在肾癌细胞中的表达。
GABPA过表达抑制异种移植小鼠肾细胞癌转移和生长
图片来源: https://doi.org/10.1186/s13046-022-02382-6
总之,GABPA可激活TGFBR2转录,从而增强转化生长因子β信号转导,从而抑制肾细胞癌细胞的增殖、干化和侵袭。GABPA的表达对体内转移和致癌能力的抑制作用甚至更强。GABPA基因高甲基化导致的GABPA表达下调在ccRCC肿瘤中广泛存在,这归因于一种真正的肿瘤代谢物L-2-HG的积聚。
这种较低水平的GABPA表达与较差的患者预后有关。因此,GABPA在ccRCC中发挥肿瘤抑制作用,而肿瘤代谢物介导的GABPA的表观遗传沉默是ccRCC进展过程中的一个关键驱动事件。
这些发现不仅有助于更好地了解ccRCC的发病机制,也有助于ccRCC的精确肿瘤学研究。根据体外和体内的结果,恢复GABPA的表达可能是侵袭性肾细胞癌的一种引人注目的治疗策略。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


