外泌体长链非编码RNA MLETA1可能作为肺癌诊断和治疗的预后生物标志物和潜在的治疗靶点
来源:生物谷原创 2023-12-05 14:31
肺癌是世界范围内最常见、最致命的癌症。非小细胞肺癌(NSCLC)约占所有肺癌的85%,约90%的肺癌相关死亡是由于转移所致。因此,迫切需要阐明肺癌转移的潜在机制,寻找肺癌诊断和治疗的早期生物标志物。
肺癌是世界范围内最常见、最致命的癌症。非小细胞肺癌(NSCLC)约占所有肺癌的85%,约90%的肺癌相关死亡是由于转移所致。因此,迫切需要阐明肺癌转移的潜在机制,寻找肺癌诊断和治疗的早期生物标志物。

图片来源: https://doi.org/10.1186/s13046-023-02859-y
近日,来自台湾成功大学的研究者们在J Exp Clin Cancer Res.杂志上发表了题为“Exosomal long noncoding RNA MLETA1 promotes tumor progression and metastasis by regulating the miR-186-5p/EGFR and miR-497-5p/IGF1R axes in non-small cell lung cancer” 的文章,该研究表明lnc - MLETA1是一种重要的外泌体lncRNA,可介导肺癌细胞中的串扰,促进癌症转移,可能作为肺癌诊断和治疗的预后生物标志物和潜在的治疗靶点。
细胞外泌体通过差示超离心从条件培养基中纯化,透射电镜观察,并通过纳米颗粒跟踪分析确定其大小分布。外泌体lncRNA测序(lncRNA - seq)用于鉴定长链非编码rna。通过伤口愈合试验、two‑chamber transwell试验和细胞移动跟踪来确定细胞迁移和侵袭。用小鼠原位和皮下移植人癌细胞,观察肿瘤在体内的转移情况。采用Western blot、qRT-PCR、RNA - seq和双荧光素酶报告基因检测来研究其潜在机制。采用qRT-PCR检测血浆外泌体lncRNA水平。采用MS2标记的RNA亲和纯化(MS2 - TRAP)测定来验证lncRNA结合的miRNAs。
研究者发现一种新的lncRNA, lnc - MLETA1,在高度转移细胞及其分泌的外泌体中表达上调。lnc - MLETA1的过表达增强了肺癌细胞的迁移和侵袭。相反,lnc - MLETA1的敲低会减弱肺癌细胞的运动和转移。有趣的是,外泌体传递的lnc - MLETA1促进了肺癌的细胞运动和转移。反过来,用LNA靶向lnc - MLETA1抑制外泌体诱导的肺癌细胞运动。在机制上,lnc‑MLETA1通过海绵化miR‑186‑5p和miR‑497‑5p促进细胞运动来调节EGFR和IGF1R的表达。临床数据显示,lnc - MLETA1在肿瘤组织中表达上调,可预测肺癌患者的生存。重要的是,血浆中外泌体lnc‑MLETA1的水平与肺癌患者的转移呈正相关。
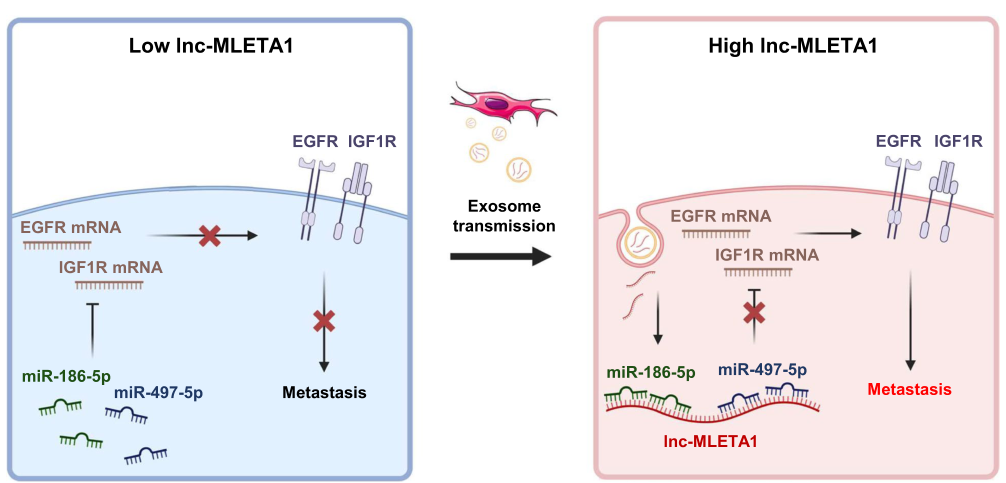
基于lnc - MLETA1的肺癌转移调控机制示意图
图片来源: https://doi.org/10.1186/s13046-023-02859-y
综上所述,lnc-MLETA1是一种重要的外泌体lncRNA,可在肺癌细胞中介导串扰,促进癌症转移,可能作为肺癌诊断和治疗的预后生物标志物和潜在的治疗靶点。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


