《细胞》:好脂肪,办坏事!西湖大学团队揭秘多不饱和脂肪酸促进肿瘤转移的双重机制
来源:奇点糕 2024-12-08 10:24
研究人员系统性地解析了支持卵巢癌细胞远端转移的代谢基础,并揭示了多不饱和脂肪酸(PUFA)在肿瘤转移不同阶段发挥的双重作用。
脂类作为细胞基本组成成分,在生物体中扮演着多种重要角色,包括能量储存、细胞膜的构成、代谢调节等等。那么在癌细胞转移过程中,脂类又扮演了什么角色呢?它们是不是让癌细胞实现成功转移的关键呢?
为了解答这一问题,近期,西湖大学/西湖实验室邹贻龙和王曦团队发表了一项重要研究成果。他们系统性地解析了支持卵巢癌细胞远端转移的代谢基础,并揭示了多不饱和脂肪酸(PUFA)在肿瘤转移不同阶段发挥的双重作用。
具体来说,研究先是发现,与原发肿瘤相比,转移性卵巢癌细胞富含PUFA,随后进一步证实,在肿瘤转移早期阶段,PUFA磷脂合成酶ACSL4可通过调控PUFA代谢,来增强癌细胞的膜流动性和侵袭性,帮助癌细胞穿越血管壁并在目标器官中定植。
而在转移的晚期阶段,高水平的PUFA会经由ECI1和ECH1基因介导的不饱和脂肪酸β-氧化通路,为癌细胞转移后生长提供能量。
研究发表在著名期刊《细胞》上。

论文首页截图
为了找到那些擅长转移的癌细胞具有哪些特点,研究人员通过分析癌症转移图谱(MetMap)和癌症治疗反应门户网站(评估药物敏感性)中的数据,发现卵巢癌等具有高转移潜力的癌细胞对铁死亡诱导剂更敏感。
鉴于铁死亡与脂质氧化有关,研究人员又对10名卵巢癌患者的原发和转移肿瘤细胞进行了脂质组学分析,结果显示,与原发肿瘤相比,转移性卵巢癌细胞中PUFA水平更高,单不饱和脂肪酸(MUFA)水平更低。这一结果提示,肿瘤细胞的脂质组成或许对其转移能力具有调控作用。
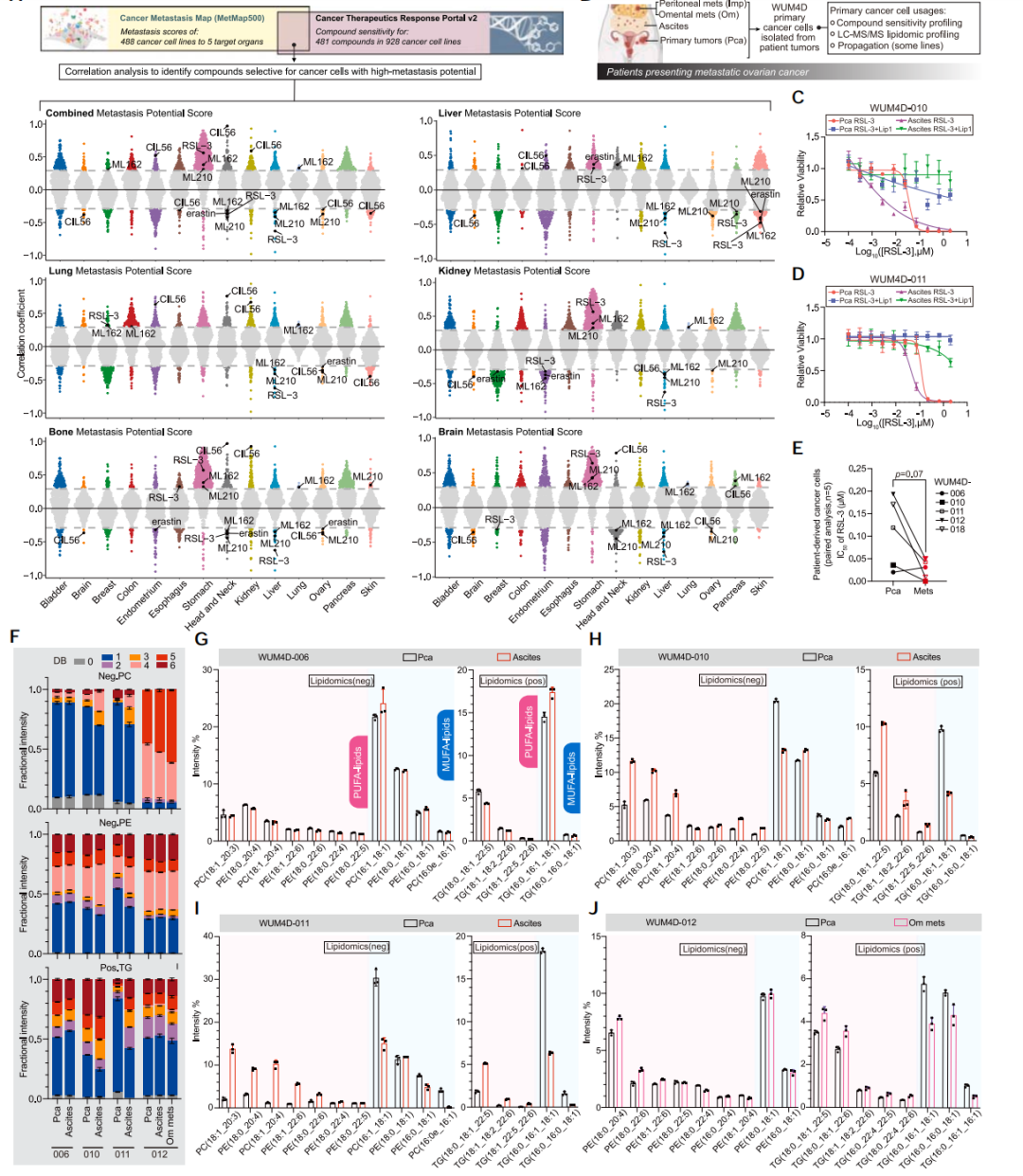
大数据分析
接下来,为了进一步观察脂质组成对卵巢癌转移的调控作用,研究人员将具有极高转移能力和铁死亡敏感性的人卵巢癌细胞系ES-2,进行两轮体内筛选,建立了两个高效卵巢癌转移小鼠模型(ES-2-MC2-Hep和ES-2-MC2-Lung,肝脏和肺部转移成功率达到100%),成功模拟了卵巢癌的腹腔转移和血行转移。
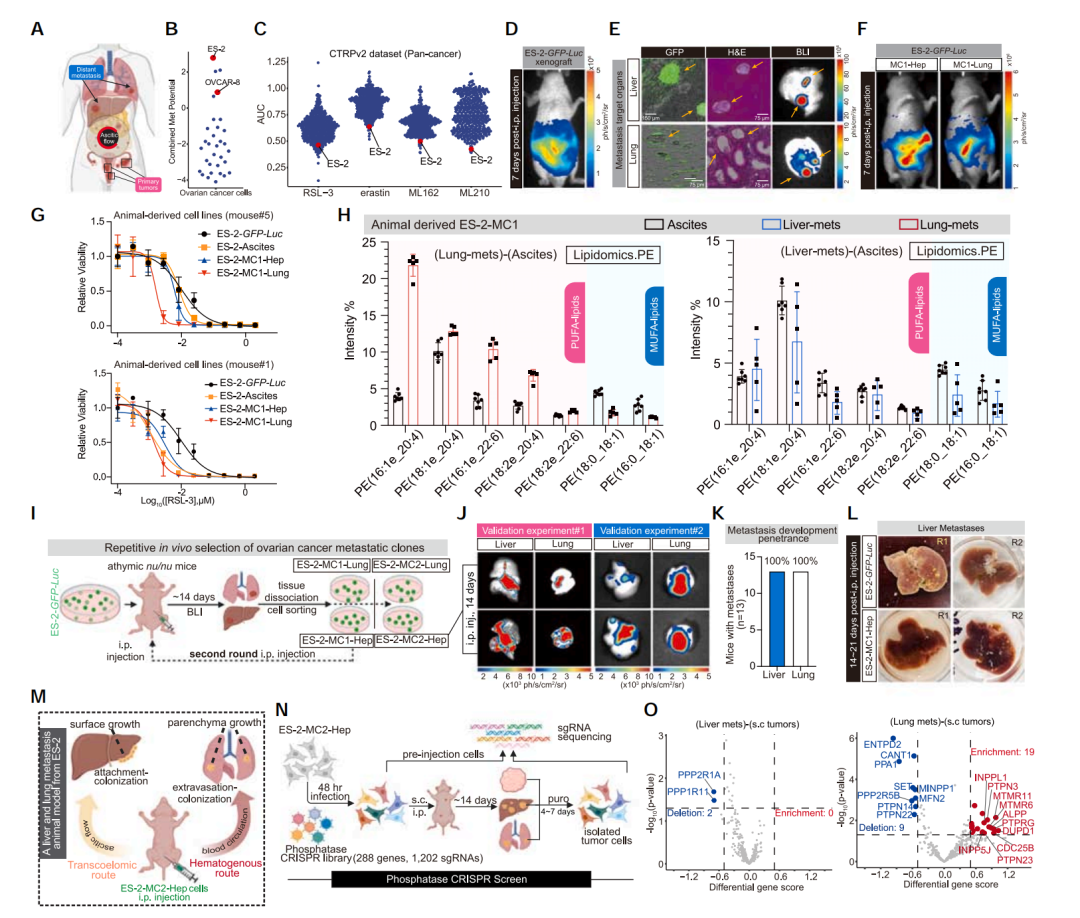
模型的建立
随后通过在卵巢癌转移小鼠模型中进行以代谢基因为重点的大规模CRISPR筛选后,研究人员识别出了多个与卵巢癌转移相关的重要基因。其中NMNAT1被鉴定为卵巢癌肝转移和肺转移的关键促进因子,而ACSL4(一种调控铁死亡和不饱和脂肪酸代谢的酶)则被鉴定为卵巢癌肺转移的关键促进因子。
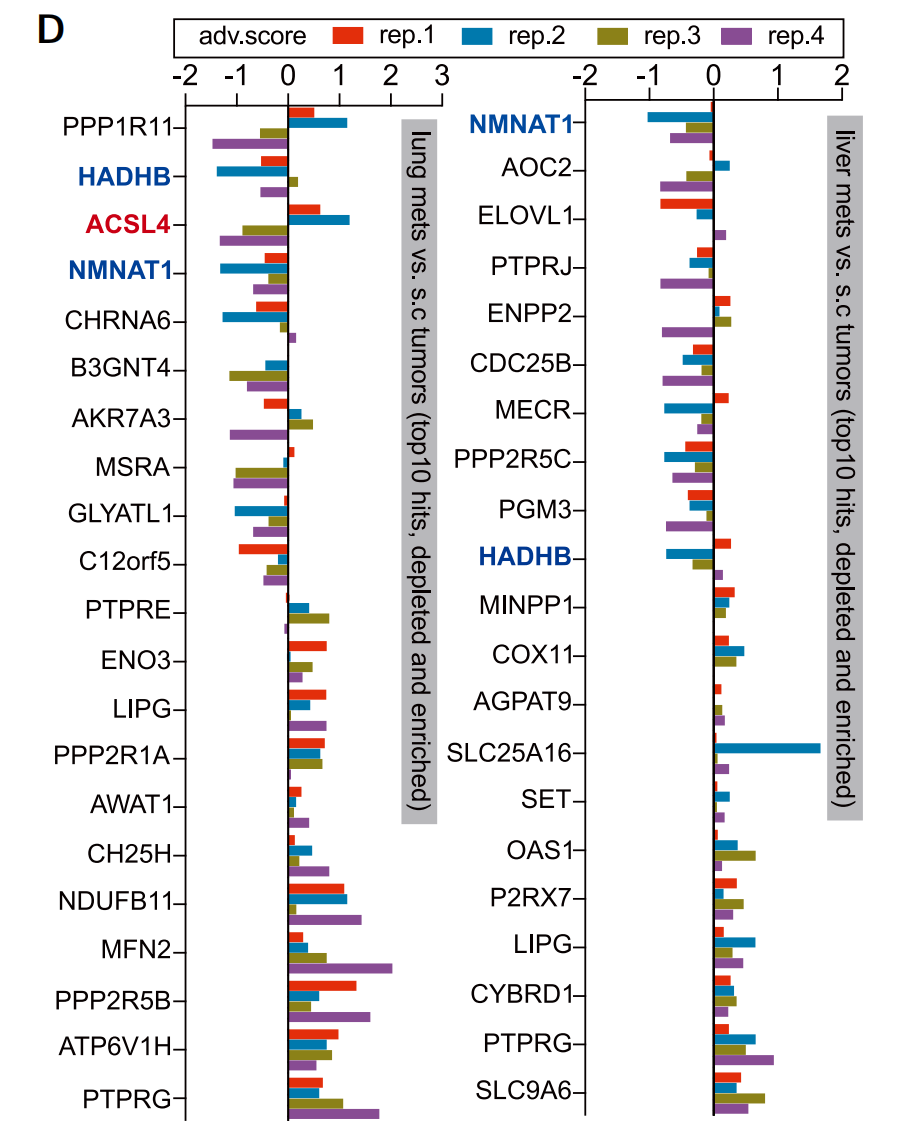
基因筛选
既往研究显示,ACSL4能特异性催化不饱和脂肪酸转化为脂酰辅酶A,参与细胞膜磷脂合成,以此提高细胞膜的流动性来实现许多细胞功能。因此,研究人员主要探讨了ACSL4调控卵巢癌肺转移的机制。
结果发现,ACSL4可通过调控PUFA代谢,来增强癌细胞的膜流动性和侵袭性,帮助癌细胞穿越血管壁(即促进癌细胞血管外渗),方便其在肺部定殖(这一步通过基因敲除和ACSL4抑制,以及外源性补充PUFA进行了验证)。
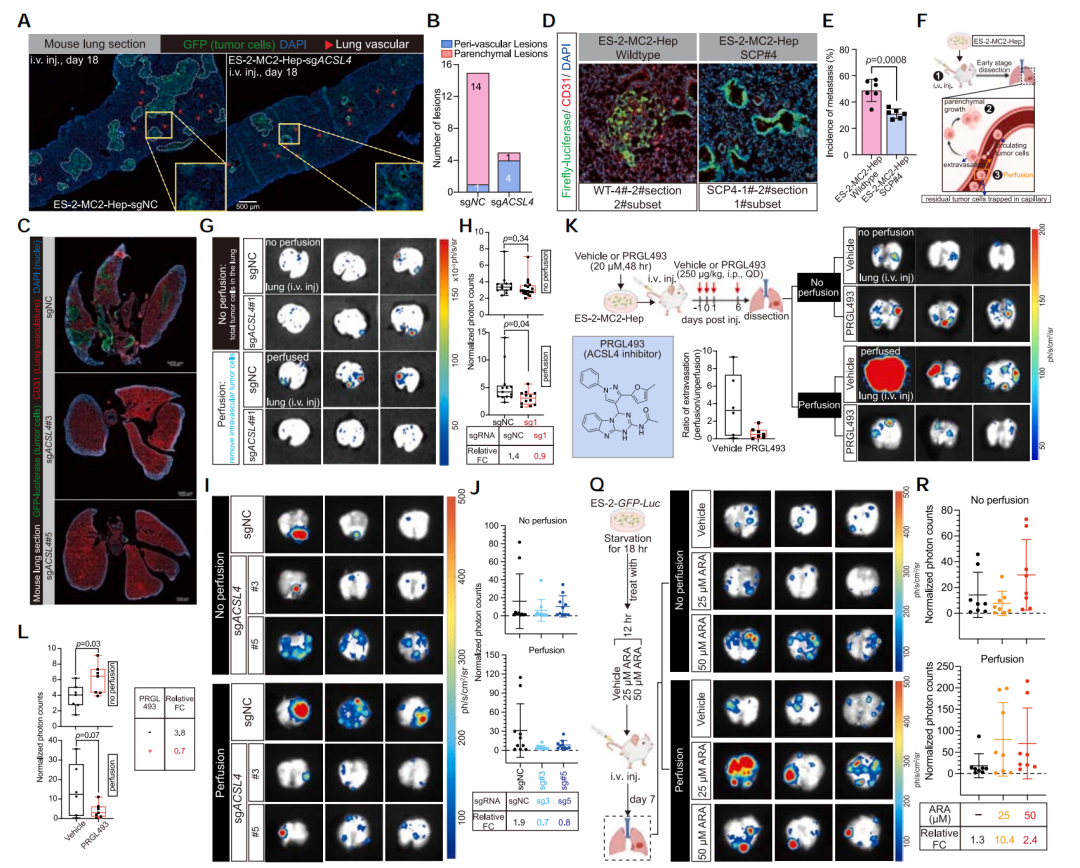
ACSL4调控PUFA磷脂合成促进卵巢癌肺转移的机制
更重要的是,研究人员发现,ACSL4的这种促进癌细胞血管外渗作用也可在SK-HEP-1肝癌和4T1乳腺癌模型中观察到。这提示,ACSL4的这种作用可能具有普适性。
鉴于癌细胞血行转移有两个关键步骤,一个是从血管中出来去要转移的器官驻扎(转移前期阶段),另一个就是驻扎后的生长(转移后期阶段)。但伴随着实验的进行,研究人员也发现了一个现象,就是ACSL4只能阻止癌细胞从血管里出来这步,因为敲除ACSL4对体外增殖肿瘤和皮下肿瘤生长没有影响。那么在转移后期阶段,又有哪些基因发挥了作用呢?
于是研究人员重新回看CRISPR遗传筛选的结果,并比较了转移前后肿瘤细胞中sgRNA丰度,结果发现,ABHD6、ECI1、ECH1和MDH1是癌细胞转移后期存活的关键基因,其中ECI1和ECH1对PUFA的氧化利用至关重要。
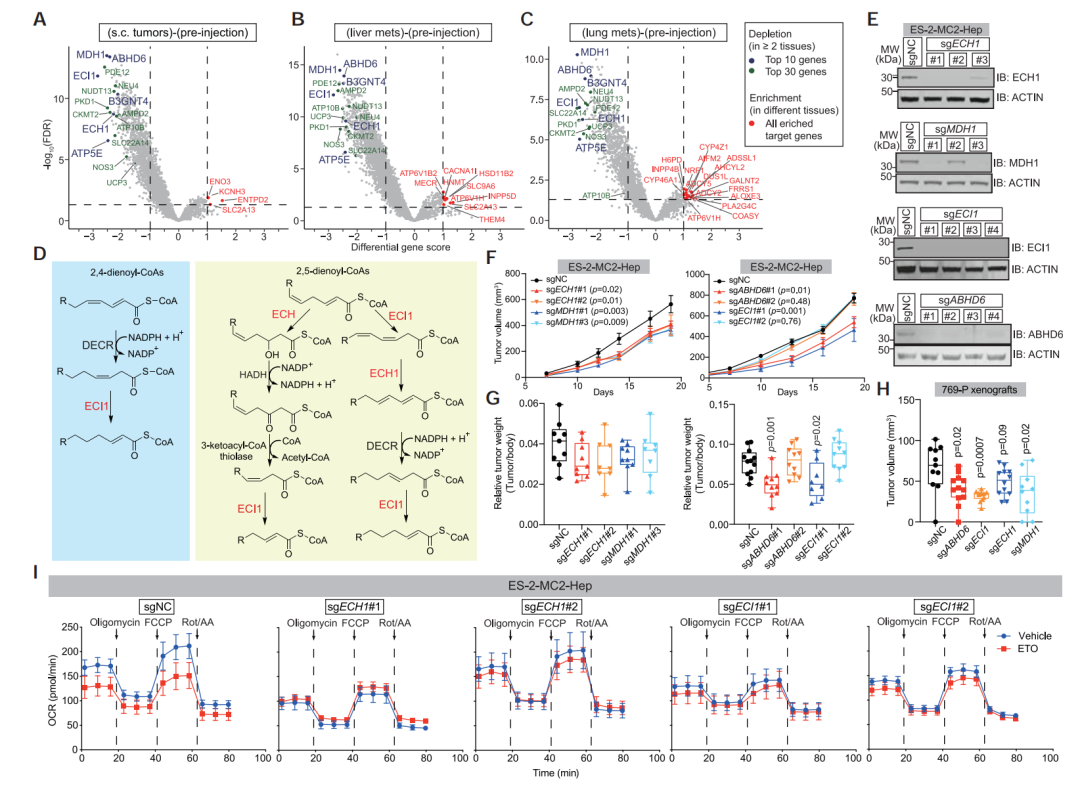
基因再筛选
通过进一步的代谢实验,研究人员也揭示了在转移的晚期阶段,高水平的PUFA会经由ECI1和ECH1基因介导的不饱和脂肪酸β-氧化通路,为癌细胞转移后生长提供能量。
以上结果表明,PUFA在肿瘤转移过程中发挥了双重作用。
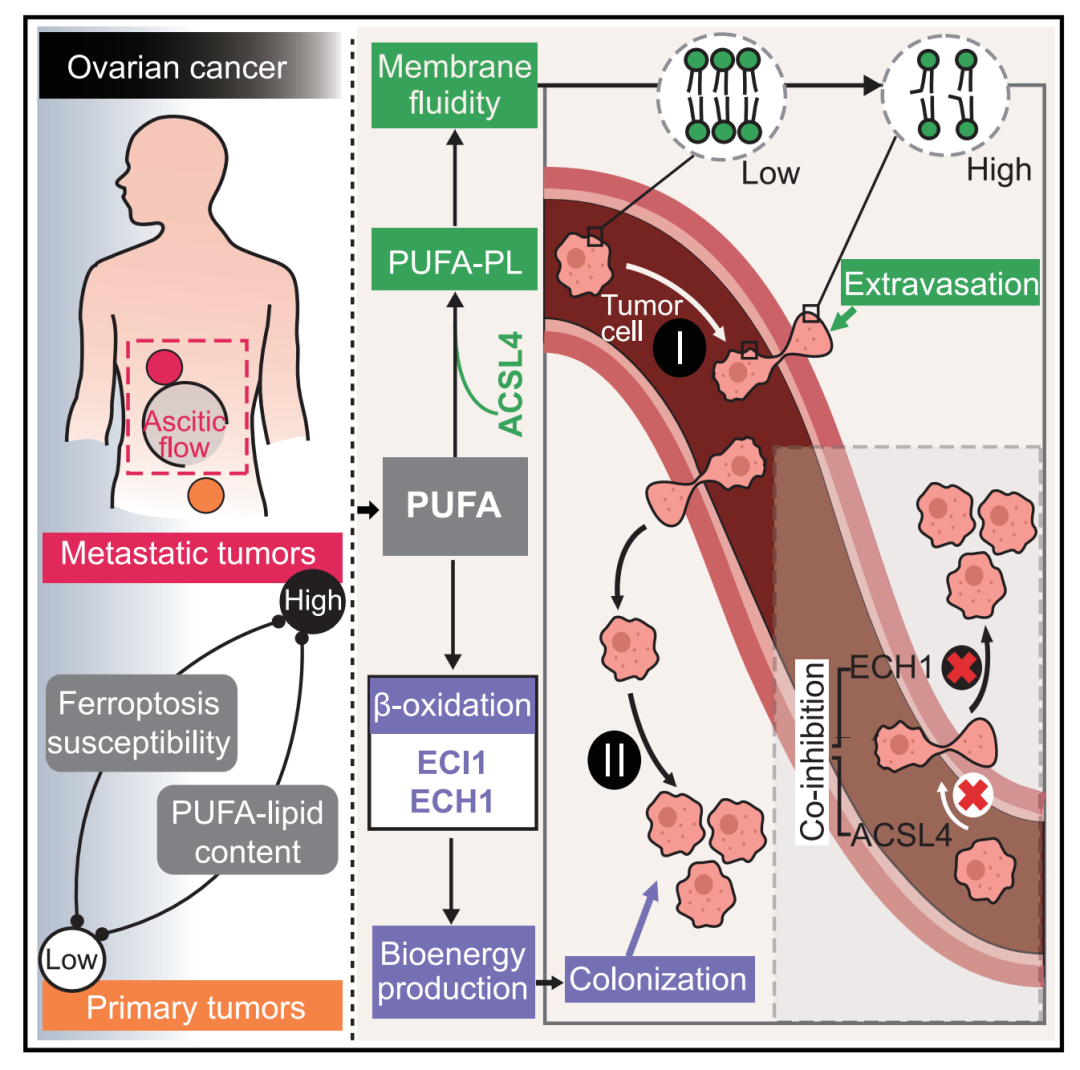
PUFA的双重作用
基于PUFA的双重作用,研究发现,在卵巢癌和黑色素瘤小鼠模型中,联合敲除ACSL4和ECH1,不仅可以有效抑制肿瘤细胞的远处转移,还成功控制了肿瘤细胞整体的血运转移负担。
总之该研究揭示了PUFA在癌症转移中有着支持癌细胞的迁移,又为其生长提供能量来源的双重作用。而针对脂质代谢的干预策略,也为开发转移性癌症治疗药物提供了新的思路。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


