Nature:解锁神经发育疾病的关键基因功能
来源:生物探索 2023-11-22 14:36
大脑的发育就像一场精心编排的舞蹈:神经元发展出具体的功能,并在大脑中小范围移动到达正确的位置,通过由此产生的化学信号使动物具备思考、感受、生存的功能。
大脑的发育就像一场精心编排的舞蹈:神经元发展出具体的功能,并在大脑中小范围移动到达正确的位置,通过由此产生的化学信号使动物具备思考、感受、生存的功能。
然而,在神经发育障碍(NDD)中,DNA中的数百个突变可能会中断这一过程,但科学家仍然不知道这些突变如何中断神经元的精确分化或迁移模式。实验设计方面,直接在胚胎或新生儿中研究这些缺陷太过危险,而使用其他动物模型又可能导致研究结果不够精准。
在《自然》杂志上发表的一项新研究中,斯坦福大学神经科学家Sergiu Paşca和他的团队将组装技术与CRISPR基因编辑相结合,以确定神经发育疾病基因在典型大脑发育过程中的作用,以及当它们缺失时随之而来的混乱1。

“我们终于得到了导致自闭症的一长串基因,”Paşca说:“问题是,我们如何理解它们的功能,特别是在人类大脑发育非常复杂的背景下。”
在过去的十年里,科学家们已经能够将干细胞转化为大脑类器官,这是一种三维细胞团,可以生长出与人脑相似的细胞类型和结构2。六年前,Paşca的团队将这项技术更进一步,融合了两个类器官,每个类器官代表不同的大脑区域3。这种被称为“组合体”的新模型使科学家能够人为模拟大脑内发生的相互作用。
这项新研究的重点是中间神经元,在大脑中携带关键的感知和运动信号。在发育过程中,这些神经元从前脑的一个位置迁移到另一位置,并调节其他神经元的过度放电,一些人认为这一过程在神经发育障碍中遭到破坏4。
Paşca的团队制作了1000多个类器官,模仿前脑中间神经元从大脑皮层下开始、到皮质结束的迁移过程。在每个大脑皮层下的类器官中,他们使用CRISPR基因编辑技术消除了研究人员筛选的425个神经发育障碍基因中的一个。然后,他们将基因编辑的皮质下类器官与皮质类器官融合并生成了组合体。通过以发出绿光的分子标记中间神经元,研究人员可以追踪中间神经元的生成以及它在大脑皮层和皮质之间的迁移。
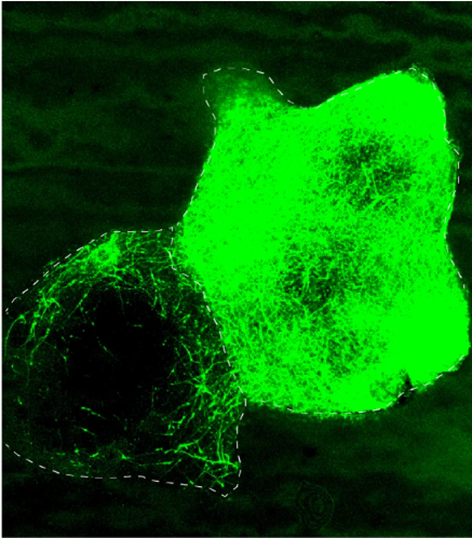
中间神经元(绿色)在整个组合体中迁移,其方式类似于它们在大脑发育过程中迁移到皮层(图源:Sergiu Paşca实验室)
研究人员发现,11%的神经发育障碍基因在中间神经元功能中发挥着重要作用。在缺乏某些基因的情况下,中间神经元根本无法形成。消除其他基因可以阻止中间神经元从大脑皮层下类器官移动到相邻的皮质类器官。对LNPK基因的深入研究表明,它破坏了中间神经元中亚细胞结构的运动,从而使细胞无法穿过大脑。
Paşca说:“我们现在已经可以获取数百个基因,并综合来看它们在人类大脑发育中的作用,这在以前是无法完成的。”他认为这种方法可以帮助识别新的致病基因。“一旦我们确定了干扰中间神经元迁移的所有基因,就可能发现我们之前不知道的致病基因,因为患者太罕见了。”
耶鲁大学遗传学家Kristen Brennand没有参与这项研究,她表示,与之前使用神经祖细胞的研究相比,这项研究提供了更具生理相关性的人脑背景。然而,她强调了使用更多样本重复研究的重要性。她指出:“三个不同的人可以继承相同的风险基因,但一个患有自闭症,一个患有精神分裂症,还有一个人不受影响。罕见的NDD基因不会孤立地发挥作用。”
Paşca认识到,中间神经元迁移可能只会导致一部分神经发育障碍病例,但他相信,研究这些关键的疾病过程有望带来潜在新药来治疗或修复缺陷。他的团队已经开始剖析这些基因如何影响中间神经元功能。
“我的实验室以开发工具而闻名,但这从来都不是真正的目标,”Paşca说:“我的目标是了解严重精神疾病背后的生物学原理。”
1.Meng X,et al.Assembloid CRISPR screens reveal impact of disease genes in human neurodevelopment.Nature.2023.
3.Birey F,et al.Assembly of functionally integrated human forebrain spheroids. Nature. 2017;545(7652):54-59.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


