2022 ASCO:DESTINY-Breast04重磅公布,耶鲁专家现场如何点评?
来源:医药魔方 2022-06-07 09:18
美国当地时间6月5日,来自纪念斯隆凯特琳肿瘤中心的Shanu Modi博士汇报了备受瞩目的DESTINY-Breast04最新数据。
美国当地时间6月5日,来自纪念斯隆凯特琳肿瘤中心的Shanu Modi博士汇报了备受瞩目的DESTINY-Breast04最新数据。

根据目前的评估模型,我们可以把转移性乳腺癌分为三类:HER+,HER2低表达,HER2-。针对HER2低表达患者,现有的HER2靶向药物未能显示出明显获益。DESTINY-Breast04研究结果显示,针对这部分患者,T-DXd显示出前所未有的(unprecedented)、具有临床意义的生存改善。在所有转移性乳腺癌患者中,HER2低表达者约占50%。
HER2低表达转移性乳腺癌存在巨大的、未被满足的临床需求。首先,HER2低表达是指免疫组化(IHC)评分1+或2+/原位杂交(ISH)-;其次,针对HER2低表达患者,既往治疗上等同于HER2阴性患者,后线选择有限;第三、针对HR+/HER2-患者,接受CDK4/6抑制剂后出现疾病进展,后续选择有限;第四、经过多线化疗后进展的患者,治疗获益也非常有限。
T-DXd的药物结构特征有7个——1、载荷为拓扑异构酶I抑制剂;2、载荷具有高效能;3、高药物-抗体比例(DAR=8);4、载荷的半衰期较短;5、连接子-载荷之间稳定;6、肿瘤选择性可切割型连接子;7、旁观者效应。T-DXd在早期临床研究中显示出理想的抗肿瘤活性。

DESTINY-Breast04研究是首个针对HER2低表达转移性乳腺癌患者的随机III期临床试验。纳入HER2低表达、不可切除、和/或转移性乳腺癌患者,转移性状态下既往接受过1~2线化疗;HR+者为内分泌难治性患者,按2:1随机分组,分为T-DXd组和医生选择治疗(TPC)组。主要终点为BICR(盲态独立中心评估)的PFS(HR+);次要终点包括:BICR的PFS(所有患者),OS(HR+患者,所有患者)。

统计学方面使用了多重检验,对主要终点和关键次要终点进行分层评估。在进入下一个终点评估前,每一个终点都需要有统计学显著性。最终共纳入557名患者,两组患者的基线特征相似,在转移性患者中,既往接受过≥3线治疗者超过了60%。
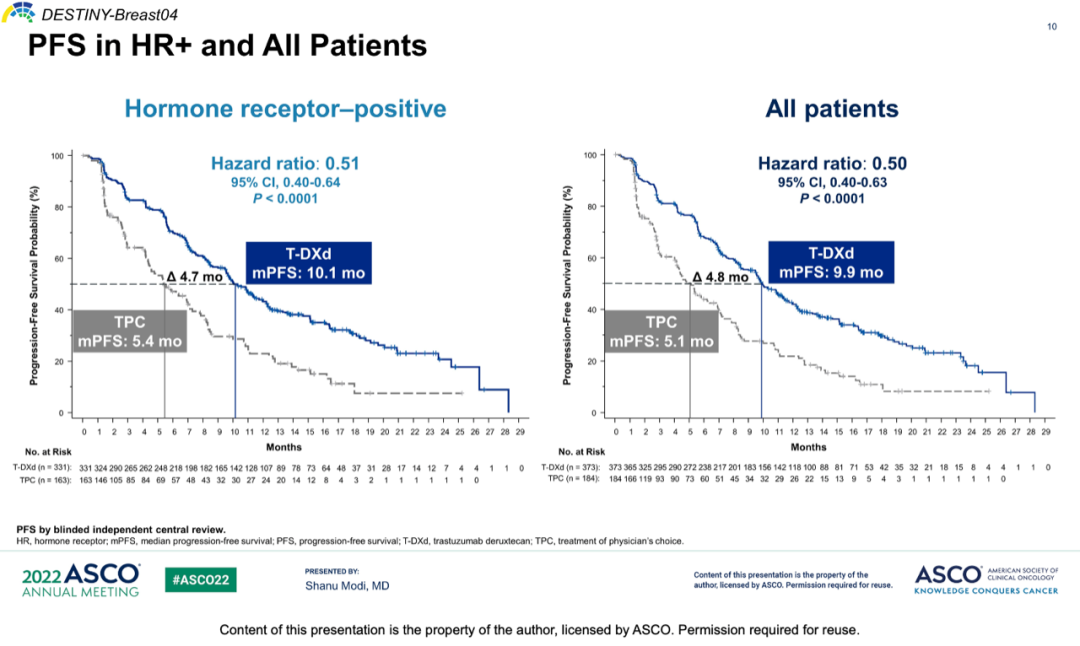
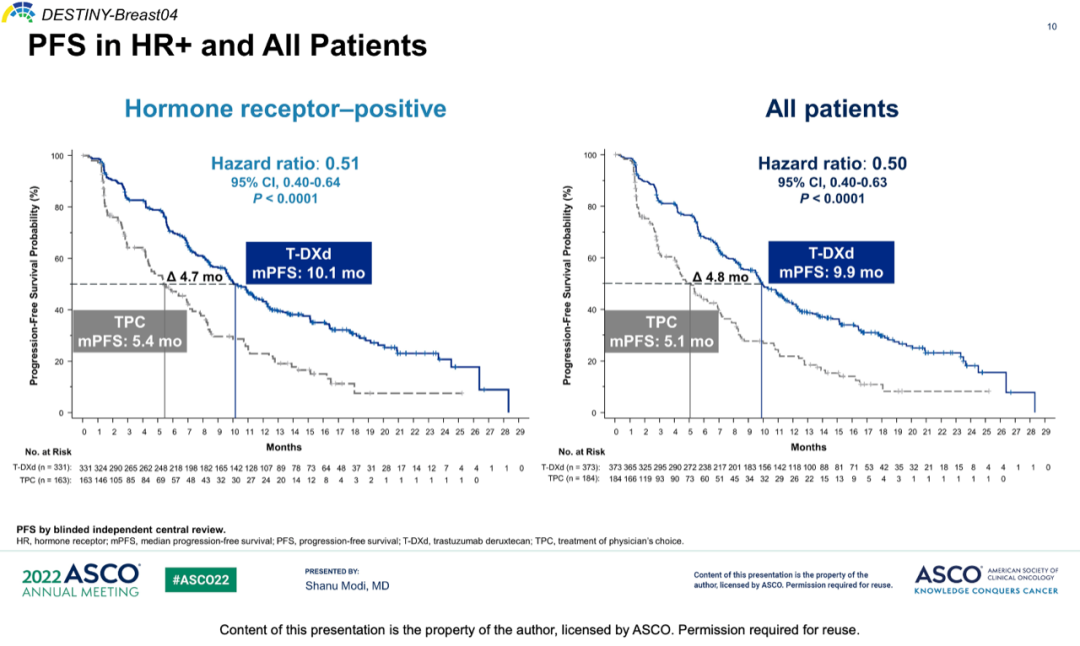
结果显示,HR+人群中,T-DXd组和TPC组的PFS分别为10.1个月和5.4个月(HR=0.51,P<0.0001);总人群中,T-DXd组和TPC组的PFS分别为9.9个月和5.1个月(HR=0.50,P<0.0001)。
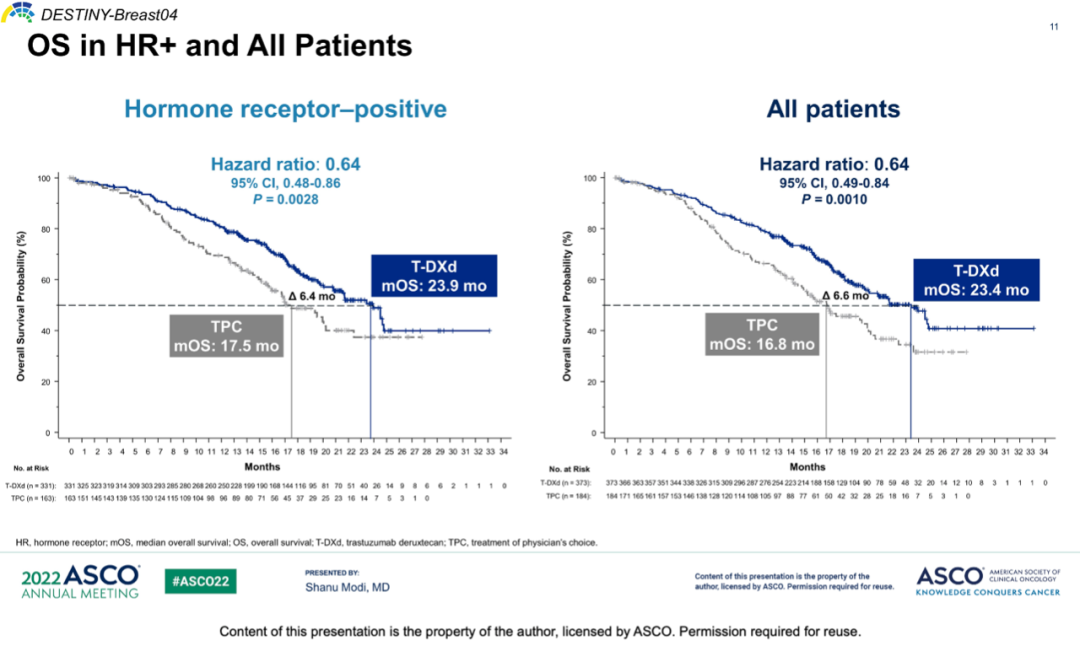
OS方面,HR+人群中,T-DXd组和TPC组的OS分别为23.9个月和17.5个月(HR=0.64,P=0.0028);总人群中,T-DXd组和TPC组的OS分别为23.4个月和16.8个月(HR=0.64,P=0.0010)。
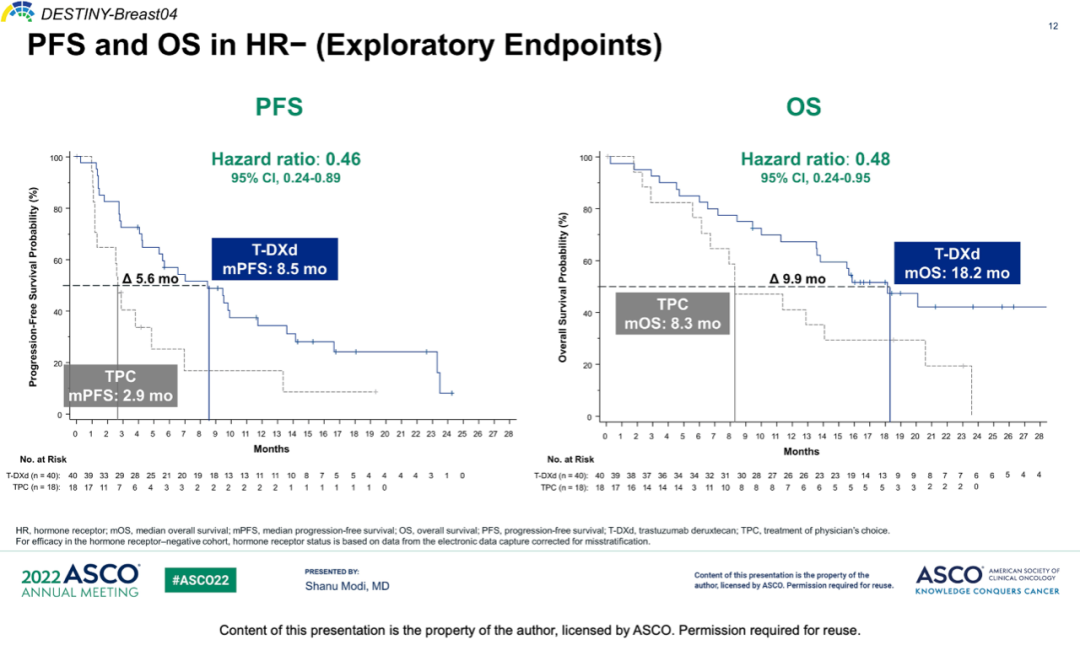
探索性终点方面,在HR-人群中,T-DXd组和TPC组的PFS分别为8.5个月和2.9个月(HR=0.46);T-DXd组和TPC组的OS分别为18.2个月和8.3个月(HR=0.48)。
HR+患者人群中,T-DXd组和TPC组的ORR分别为52.6%和16.3%;HR-患者人群中,T-DXd组和TPC组的ORR分别为50.0%和16.7%。

安全性方面,中位治疗持续时间,T-DXd组和TPC组分别为8.2个月和3.5个月;最常见的与治疗中止相关的不良事件,T-DXd组为ILD/肺炎(8.2%),TPC组为外周感觉性神经病变(2.3%);最常见的与剂量降低相关的不良事件,T-DXd组为恶心和疲乏(4.6%),TPC组为中性粒细胞减少症(14.0%)。

特殊药物相关不良反应——ILD/肺炎,T-DXd组和TPC组分别为12.1%和0.6%。左心室功能障碍,T-DXd组和TPC组分别为4.3%和0.5%。
总体来说,DESTINY-Breast04研究达到了主要和次要终点,所有亚组均能获益,包括HER2 IHC各水平组以及既往接受过CDK4/6组,没有发现新的安全性信号。

随后,来自耶鲁大学的Patricia LoRusso教授进行了精彩的讨论发言。讨论重点包括以下几个:1、T-DXd的药物特性;2、疗效的分析;3、HER2低表达乳腺癌的分类以及标志物挑战;4、其他肿瘤适应症;5、潜在的耐药机制;6、未来方向。
T-DXd的结构特征有7个(注:文章前半部分已有描述)。需要说明的是,T-DXd的载荷具有膜渗透性,可以对靶抗原阳性细胞周围的细胞产生杀伤作用。这种旁观者效应在HER2低表达,也就是异质性肿瘤中能发挥作用。
简
单重复一下疗效方面的数据。在HR+和HR-患者中,相较TPC组,T-DXd的OS生存获益~6个月。尽管HR-患者人数较少,但这部分患者的T-DXd生存获益达到~10个月。

上面是Tarantino教授于2020年提出的有关HER2低表达的定义标准。但是,面对这个新型的抗肿瘤药物以及理想的数据结果,我们必须重新思考,用更准确、更敏感性的方法去评估HER2状态,这对病理学提出了新的要求,我的同事们曾围绕这个问题发表了多篇相关论文。
T-DXd也在其他癌种中进行了临床试验,包括NSCLC、胃癌、结直肠癌等。这里有一项II期试验,纳入了非鳞、HER2突变的NSCLC患者,大部分患者都能产生应答,提示T-DXd可能对HER2突变性疾病均可产生活性。我了解过两项肺癌人群中的数据,应答率有所差异。遗憾的是,应答持久性尚不理想,即使在哪些应答水平较高的患者中。
目前,FDA尚没有批准针对HER2突变的泛癌种(pan tumor)治疗药物。T-DXd正在进行泛癌种的临床试验:DESTINY-PanTumor01和DESTINY-PanTumor02,纳入了胆管癌,膀胱癌,宫颈癌,子宫内膜癌,卵巢癌,胰腺癌以及罕见肿瘤等。
尽管T-DXd在转移性乳腺癌患者中有显著的、持久的应答,但是大部分患者不可避免会出现进展。在DAISY研究中,对继发性耐药进行了分析,疾病出现进展时,20名患者中有13名出现了HER2表达水平的下降。
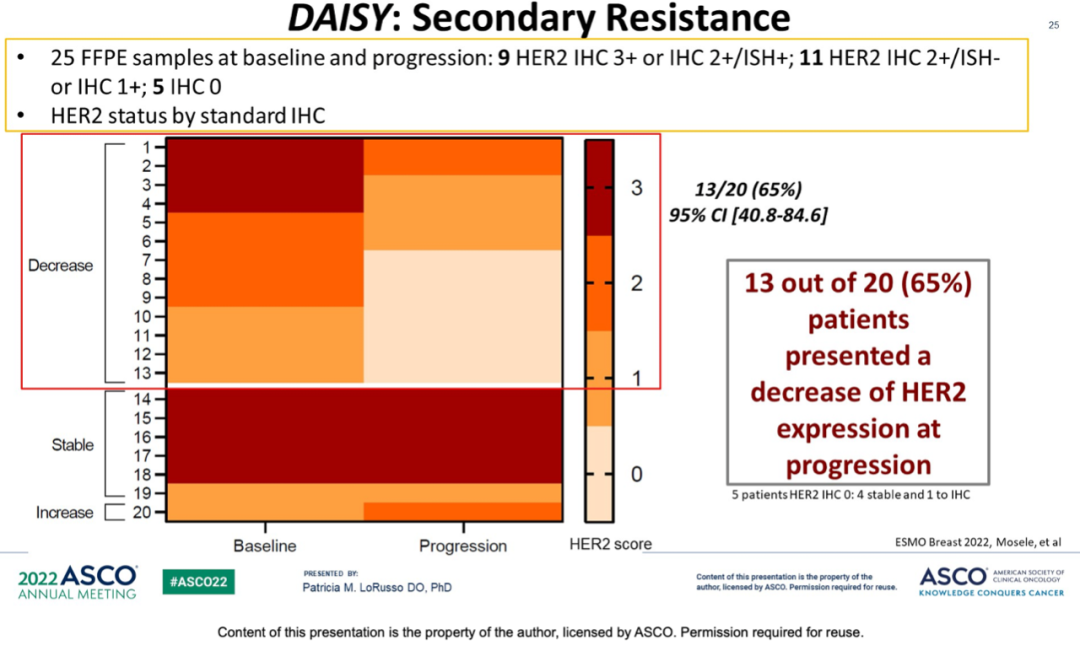
对于耐药的机制,我们目前尚不明确。HER2表达水平的降低,是否意味着旁观者效应的减弱?HER2+和HER2-肿瘤细胞之间的空间特征是否会影响疗效?对载荷Dxd产生了耐药性?是信号通路驱动,还是分子驱动?又或者是药物递送机制、降解机制出现了改变?另外,在不同的癌种中,耐药机制是否相同?载荷Dxd是否与其他拓扑异构酶I抑制剂的耐药机制相同?
同时,T-DXd还有很多问题值得我们解答:1、T-DXd对新一代ADCs的开发有哪些启示?2、在HER2+/突变肿瘤中,我们下一步做什么?辅助,新辅助还是联合方案的探索?3、肿瘤的耐药性如何处理?4、T-DXd发生ILD的机制是什么?如果在疾病较早期使用这个药物,会产生什么样的影响?我个人认为,如果将来在疾病较早期使用T-DXd和今天使用它,是会不一样的。到了那个时候,我们对它会有更多的了解,如何预防、早期诊断、并治疗相关的不良反应。最后,期望能给HER2低表达患者带来更好的治疗选择。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


