Cell Stem Cell | 北京大学席建忠/叶步青等合作构建非小细胞肺癌患者来源的肿瘤样细胞簇模型
来源:生物探索 2024-04-10 09:45
PTC模型作为一种全新、无基质胶、可再现肿瘤微环境的临床前模型,在临床肿瘤精准治疗方面表现出巨大潜力,目前已成功应用于胃癌、结直肠癌、乳腺癌、肺癌等患者的临床药物疗效预测。
北京大学席建忠、叶步青及上海交通大学姜丽岩共同通讯在Cell Stem Cell 在线发表题为“Patient-derived tumor-like cell clusters for personalized chemo- and immunotherapies in non-small cell lung cancer”的研究论文,该研究建立了283个非小细胞肺癌(NSCLC)患者来源的肿瘤样细胞簇(PTCs)模型,并以此模型为基础开展化疗药物及免疫药物敏感性检测,经临床双盲试验结果验证,PTCs预测药物疗效的准确率为89%以上。
该研究报告了非小细胞肺癌(NSCLC)患者源性肿瘤样细胞团(PTCs),能够在10天内进行100 - 5000次药物试验。建立了283个PTC模型,成功率为81%。PTCs含有与内源性间质细胞和免疫细胞自组装的原发肿瘤上皮,在表型和基因型特征上与原始肿瘤高度相似。利用标准化培养和药物反应评估方案,PTC药物检测分析显示,在前瞻性预测临床结果方面,总体一致性为89%,区分完全/部分缓解和进展性疾病的准确率为98.1%。值得注意的是,PTCs通过结合细胞活力和IFN-γ值评估,可以准确预测接受抗PD1治疗的患者的临床结果。这些发现表明,PTCs可作为一种有价值的临床前模型,用于非小细胞肺癌的个性化治疗和基础研究。

肺癌是最常见和最致命的癌症之一,每年在全世界造成160万人死于癌症。非小细胞肺癌(NSCLC)占肺癌的绝大多数(约85%),预计5年生存率仅为15.9% 2靶向治疗作用于驱动基因,主要是突变的表皮生长因子受体(EGFR),已经取得了令人印象深刻的反应。然而,并非所有的EGFR突变患者对酪氨酸激酶抑制剂(TKIs)有反应,大多数患者在几个月的有效治疗后复发。此外,大量分子和临床异质性的存在使得靶向治疗的选择更加复杂。例如,共同发生的基因组改变,特别是在TP53、BRAF或CDKN2A突变中,显著缩短EGFR TKIs治疗后的无进展生存期(PFS)。
精确肿瘤学旨在为每个癌症患者确定有效的治疗方法。到目前为止,有三种策略在促进药物选择方面显示出巨大的潜力:(1)DNA测序引导的药物选择有利于具有靶向基因组改变(如EGFR突变)的患者;(2)患者源性肿瘤异种移植物(PDXs)可以准确预测所测试的药物疗效,因为它们保留了个体患者不同肿瘤的特异性特征,但耗时(从PDX模型开发到药物评估约3个月)8-10;(3)从各种癌症中发展出来的患者来源的类器官(PDOs)。PDOs在时间和吞吐量方面比PDXs有优势。
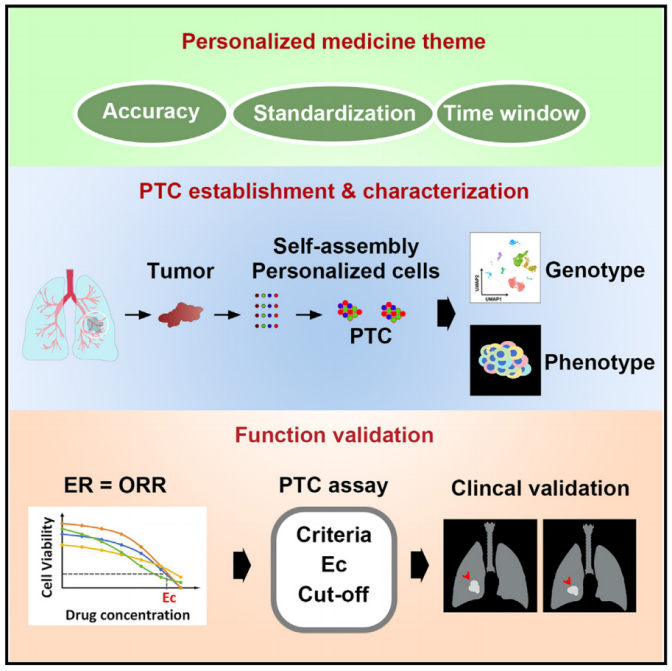
模式图(Credit: Cell Stem Cell )
截至目前,已有17项研究在临床中评估PDOs作为治疗反应预测生物标志物的临床有效性。培养基组成、培养技术、质量控制分析和实验设置(包括药物暴露时间、读数和体外反应判断)在这些研究中有所不同,并已得到充分记录。然而,两个最重要的参数,包括方法的标准化和预测的准确性,必须在临床实施PDOs指导的药物选择之前真正解决。基质或其他细胞外基质(ECM)替代品是PDO培养的重要组成部分,含有未定义的可能影响实验可重复性的外部因素。此外,PDOs预测化疗临床反应的准确性仍存在争议;Ooft等人进行了一项设计良好的前瞻性观察性研究,报道结直肠癌PDOs预测伊立替康的药物反应准确度较高,但无法预测一线5-氟尿嘧啶和奥沙利铂治疗患者的预后。
总体来讲,PTC模型作为一种全新、无基质胶、可再现肿瘤微环境的临床前模型,在临床肿瘤精准治疗方面表现出巨大潜力,目前已成功应用于胃癌、结直肠癌、乳腺癌、肺癌等患者的临床药物疗效预测,可准确、前瞻性地指导肿瘤患者的个体化治疗。作为一种有前景的肿瘤研究模型,PTC模型还可应用于肿瘤基础科学研究、新药研发等领域。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


