Science丨通过捕获新冠病毒刺突蛋白中间态,揭示广谱抗冠状病毒机制
来源:生物探索 2024-08-26 10:59
刺突蛋白的中间态结构表现出高度动态特性,尤其是stem-helix区域。因此,如何设计免疫原来刺激免疫系统产生针对这一保守区域的中和抗体,将成为开发泛冠状病毒疫苗的重要突破口。
来自耶鲁大学Walther Mothes团队的李文炜博士(主要联系人),以及博士生Michael Grunst(第一作者),秦专博士(第二作者)在Science杂志发表了题为Structure and inhibition of SARS-CoV-2 spike refolding in membranes的研究论文【1】。在这项研究中,研究团队利用冷冻电镜断层成像技术(cryo-electron tomography, cryo-ET)捕捉到了新冠病毒刺突蛋白与细胞受体ACE2在膜间结合的结构,以及其底端蛋白S2的下游构象变化,揭示了stem-helix区域结合类中和抗体的抗病毒机制。

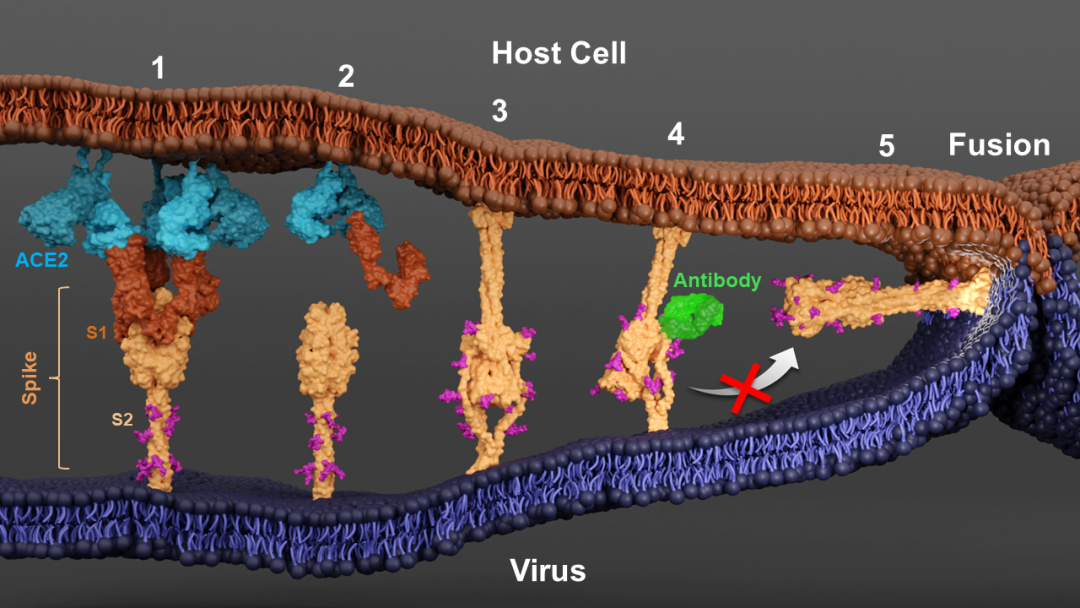
模式图(Credit: Science)
在融合前状态下(prefusion),刺突蛋白三聚体和ACE2受体二聚体相互交联,在膜间形成蛋白阵列,有助于病毒附着于宿主表面。刺突蛋白的三个单体可分别各结合1个ACE2受体二聚体,而受于结构构象的限制,绑定的二聚体ACE2蛋白无法同时结合来自于同一刺突蛋白三聚体的两个单体,但可以与来自相邻的刺突蛋白三聚体的单体结合,进而实现刺突蛋白的交联。这种交联机制在一定程度上增强了spike-ACE2结合的灵活性,为病毒在刺突蛋白上引入突变位点提供了适应性空间。
在热激活后, spike-ACE2复合体会发生构象变化,在病毒膜与宿主膜之间形成杆状结构。该杆状结构与之前发现的融合后状态(post-fusion)的刺突蛋白相似,但是其方向却完全相反——杆状结构从宿主膜延伸,而融合后状态的刺突蛋白则由病毒膜伸出。研究人员推测该杆状结构应该就是之前一直寻找的刺突蛋白的中间态(pre-hairpin intermediate),此时,底端蛋白S2已经将融合肽段插入宿主膜,形成螺旋杆状结构,S2的底部区域则表现出高度可变性,无法通过局部断层平均技术(subtomogram averaging)获得稳定结构。通过局部断层分类(subtomogram classification),研究团队获得到了在病毒膜上具有不同倾斜角度的刺突蛋白中间态,这些倾斜角度与膜间距离呈高度负相关,支持了刺突蛋白通过自身折叠的构象变化拉近病毒膜与宿主膜,最终促使双膜融合的研究模型。
在之前的研究中,研究团队分离出了一类中和抗体可以结合刺突蛋白底部的stem-helix区域【2】,由于该区域在冠状病毒间高度保守,这类抗体可对多种冠状病毒具有中和活性,为泛冠状病毒疫苗的设计提供了理论基础。然而,该类中和抗体的抗病毒机制尚未明了。在本研究中,研究团队证实了此类中和抗体能够结合到刺突蛋白底部的stem-helix区域,且在刺突蛋白发生构象变化后,仍能结合其中间态,但是病毒与宿主膜间距离不能进一步缩小,揭示其阻断了底端蛋白S2的自身折叠。
来自Northeastern University的Paul Whitford和Rice University的Jose Onuchic团队通过分子动力学模拟再现了刺突蛋白从融合前状态,到结合ACE2受体,激活S2构象变化形成中间态,最后自身折叠至融合后状态的过程。引入结合stem-helix区域的中和抗体后,抗体的结合会最终阻断底端蛋白S2的自身折叠。这些模拟结果与本研究中获得的cryo-ET结构高度契合。
刺突蛋白的中间态结构表现出高度动态特性,尤其是stem-helix区域。因此,如何设计免疫原来刺激免疫系统产生针对这一保守区域的中和抗体,将成为开发泛冠状病毒疫苗的重要突破口。
值得注意的是,来自Walther Mothes团队的李文炜,秦专博士去年通过冷冻电镜断层成像技术研究艾滋病毒入侵过程,也捕捉到了一些此前研究中未能观察到的结构【3】。病毒蛋白在原位膜上与受体结合,以及其后的构象变化远比之前的研究模型复杂。冷冻电镜断层成像技术为原位观察病毒膜蛋白活动提供了新的可能性,弥补了此前仅针对蛋白外膜部分的结构研究的不足。
参考文献:
1. Grunst, M. W., Z. Qin, E. Dodero-Rojas, S. Ding, J. Prévost, Y. Chen, Y. Hu, M. Pazgier, S. Wu, X. Xie, A. Finzi, J. N. Onuchic, P. C. Whitford, W. Mothes and W. Li (2024). "Structure and inhibition of SARS-CoV-2 spike refolding in membranes." Science 385(6710): 757-765. (https://www.science.org/doi/10.1126/science.adn5658)
2. Li, W., Y. Chen, J. Prévost, I. Ullah, M. Lu, S. Y. Gong, A. Tauzin, R. Gasser, D. Vézina, S. P. Anand, G. Goyette, D. Chaterjee, S. Ding, W. D. Tolbert, M. W. Grunst, Y. Bo, S. Zhang, J. Richard, F. Zhou, R. K. Huang, L. Esser, A. Zeher, M. Côté, P. Kumar, J. Sodroski, D. Xia, P. D. Uchil, M. Pazgier, A. Finzi and W. Mothes (2022). "Structural basis and mode of action for two broadly neutralizing antibodies against SARS-CoV-2 emerging variants of concern." Cell Reports 38(2): 110210. (https://doi.org/10.1016/j.celrep.2021.110210)
3. Li, W., Z. Qin, E. Nand, M. W. Grunst, J. R. Grover, J. W. Bess, J. D. Lifson, M. B. Zwick, H. D. Tagare, P. D. Uchil and W. Mothes (2023). "HIV-1 Env trimers asymmetrically engage CD4 receptors in membranes." Nature 623(7989): 1026-1033. (https://doi.org/10.1038/s41586-023-06762-6)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


