Science:“相爱相杀”——天然化学合成家如何同昆虫博弈
来源:微植有道 2022-03-08 11:41
不同于动物,植物在面临天敌威胁时,无法主动逃跑来规避危害,因此,在漫长的自然驯化选择中,植物开发出了一套专属的抵御“敌人”的手段—产生次生代谢物,不同类别的化合物能排斥不同种昆虫/吸引昆虫天敌靠近,从而使自身免于大规模昆虫造成的伤害,这也使得植物被人们誉为“天然的化学合成家”。这其中,植物释放的用来趋避非寄主昆虫的化学分子却一直没有被
不同于动物,植物在面临天敌威胁时,无法主动逃跑来规避危害,因此,在漫长的自然驯化选择中,植物开发出了一套专属的抵御“敌人”的手段—产生次生代谢物,不同类别的化合物能排斥不同种昆虫/吸引昆虫天敌靠近,从而使自身免于大规模昆虫造成的伤害,这也使得植物被人们誉为“天然的化学合成家”。这其中,植物释放的用来趋避非寄主昆虫的化学分子却一直没有被人们发现和鉴定到。
抗虫激素减少害虫伤害
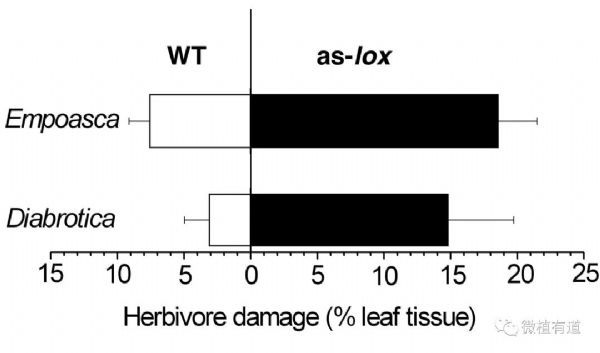
叶蝉是一类在世界范围内造成巨大农业经济损失的害虫,因危害范围广且能传播植物病毒和细菌等病原物而臭名昭着。目前叶蝉科昆虫全世界共有1万多种,中国已发现1000多种。早在2004年,来自德国马普化学生态研究所的Baldwin教授团队就发现,自然状态下,一种叶蝉科Empoasca的小叶蝉不会取食其非寄主植物渐狭叶野生烟草(Nicotiana attenuata),但当用分子生物学方法降低了烟草中抗虫激素茉莉酸后(右),小叶蝉就能产生对烟草极大的破坏性。
这表明,茉莉酸及其调控的代谢物合成通路很可能是植物抵抗非寄主昆虫的手段。Baldwin团队经过了10余年的探索,终于发现隐藏在背后的玄机。
抗虫相关基因和代谢物的发现
为了还原自然界中小叶蝉取食的真实情况,该团队首先在美国亚利桑那州的野外进行大田实验,种植了来源26个不同亲本杂交产生的650个遗传背景各不相同重组自交系群,发现不能合成茉莉酸的一些株系会招致小叶蝉的伤害,这与他们上述的结果相吻合。
接下来,团队利用此庞大的田间数据进行分析,发现茉莉酸合成及调控通路上的许多基因和代谢物同小叶蝉破坏程度成负相关(右图蓝色方块),表明它们都可能增强了植物对小叶蝉的抗性。随之,团队便认为CP、CoP和FP这三个植物合成的化学分子(右图红框)就是植物抗非寄主昆虫的关键代谢物。
然而,用这三种化合物单独饲喂昆虫发现,它们并不能够吸引昆虫取食抑或是造成后者死亡率升高,说明这其中还有着其他更加重要的未知化合物在发挥作用。
抗虫杀手锏—CPH
为了探究这一未知化合物的真实面貌,作者利用先前团队搭建好的串联质谱平台,挑选了15个已知能够大量产生抗虫化合物的株系进行分析,寻找到上述化合物之一CP来源的一个未知化合物,其m/z 347.19。较CP相比,该未知化合物多出一个绿叶挥发物性质的化学基团,而绿叶挥发物通常被认为具有广泛地驱虫性,这初步表露出该化合物的抗虫特性。于是,作者将目光锁定在这一化合物,并根据来源及构成把它命名为CPH。
那么CPH到底是不是发挥着植物抗虫性的那个“它?为此,作者开展了一系列的相关性分析及分子实验,结果发现,CPH同小叶蝉破坏呈负相关,但与茉莉酸及其活性形式呈正相关;同样的饲喂实验发现,不同于CP,CPH能够引起叶蝉大量死亡,这些令人欣喜的结果终于揭开了植物杀手锏的神秘面纱。
那么设想,如果可以人工合成该化合物并用于大规模的农业害虫防治,就可以制成纯天然高效的植物源农药,广谱地减少害虫的威胁。于是,作者团队试图利用合成生物学的手段在体外重构该化合物。
体内外合成抗虫良物CPH
一个化合物的合成过程往往需要各式的底物及酶才能够实现,CPH的一部分来源于CP,另一部分来源于绿叶挥发物,那么只需要确定酶的种类,便能够重构该化合物。于是,团队利用mQTL和DNA芯片技术,寻找到一系列在抗虫合成通路相关的酶。在底物和酶的参与下,作者在体外成功合成了CPH这一重要化合物。
但有趣的是,当在异源植物番茄和蚕豆体内表达合成CPH时,若没有小檗碱桥酶BBL2的参与,CPH便无法被检测到;而在体外合成过程却并不需要BBL2地参与。这一有趣的现象目前无以得解,但有研究表明BBL2在尼古丁的合成过程中帮助介质从线粒体转移到胞质,是否BBL2在此也扮演着类似的角色值得未来的进一步探究与发现。
至此,团队成功发现并合成了植物对抗非寄主昆虫的关键化合物,为作物抗虫研究提供了一个很好的应用出口。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。