AI造物里程碑:人类首次从头设计全新荧光素酶,转化公司已完成2500万美元融资
来源:生物世界 2023-02-27 11:35
这项研究开发了一种基于深度学习的人工智能算法——Family-wide Hallucination,可以从头设计出具有高催化活性、高底物特异性、结构紧凑和耐热性好的人造荧光素酶,这或将成为深度学习算法
最近,人工智能聊天软件ChatGPT火爆全网,在全世界范围内持续引发热议。作为一种人工智能技术驱动的自然语言处理工具,ChatGPT能够学习和理解人类的语言,并像人类一样来聊天交流,甚至能撰写文案、代码、翻译,甚至能写出以假乱真的论文。
实际上,人工智能(Artificial Intelligence,AI)已经在多个领域大放异彩并深入到我们的日常生活中。从围棋领域的AlphaGo到预测蛋白结构的AlphaFold,从去年的AI绘画再到如今的ChatGPT,人工智能作为一种新兴的颠覆性技术,正在逐步释放科技革命和产业变革积蓄的巨大能量,并深刻改变了人类的生活和思维方式。这不禁让我们感慨AI的无限可能。
2023年2月22日,著名蛋白质设计专家、华盛顿大学医学院 David Baker 教授团队在国际顶尖学术期刊 Nature 上发表了题为:De novo design of luciferases using deep learning 的研究论文。
该研究开发了可以从头设计人造荧光素酶的深度学习算法——Family-wide Hallucination,并通过实验室测试证实,这些自然界中不存在的人造酶可以非常有效地催化荧光素底物发光。这是科学界首次基于深度学习的人工智能来创造全新的酶。

生物体是杰出的化学家,细胞无时无刻不在进行复杂而繁多的生物化学反应,但与现实中的化工厂不同,细胞中的生化反应不依赖有毒化合物或极端高温、高压条件,而是在一个温和的环境下有条不紊地进行,要做到这一点,酶是最大的功臣。
如果我们能创造出新的酶,可再生化学品和生物燃料将变得触手可及。遗憾的是,自然界中的生物酶都是经过漫长的进化才逐渐演化而来,想要无中生有地设计出一种全新的酶是十分困难的,而且有限的算力很难预测酶的活性位点和底物结合结构域。
为了创造出新的酶,David Baker 团队开发了一种具有深度学习能力的AI算法——Family-wide Hallucination。研究团队首先选定一些荧光素底物,然后使用算法生成数千种可能与这些荧光素发生反应的蛋白质结构。
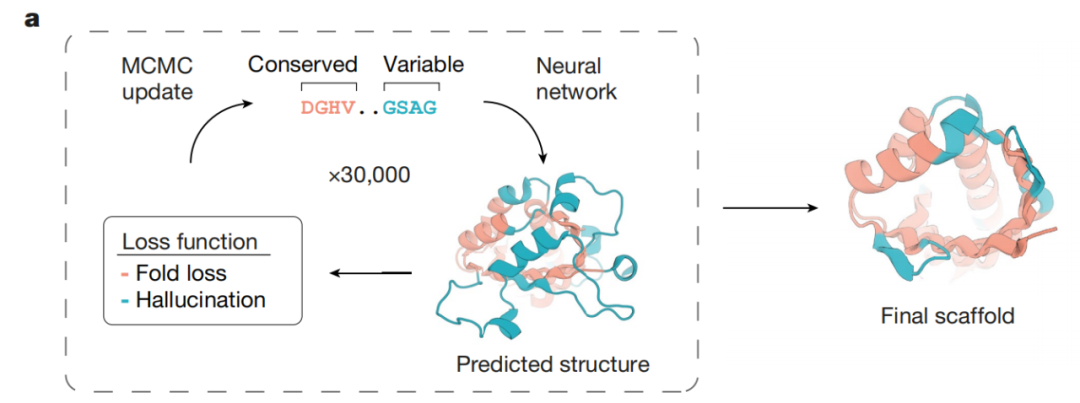
Family-wide Hallucination算法的运作模式图
具体来说,这种深度学习算法可以生成大量包含不同活性催化位点(就像一个口袋可以容纳底物)的理想蛋白质结构支架,并设计出编码他们的氨基酸序列。然后,研究团队再以这些支架为核心进一步设计出人造荧光素酶。
通过这种AI辅助设计的方式,研究团队获得了具有高特异性的人造荧光素酶,它们可以选择性地催化合成荧光素底物diphenylterazine(DTZ)和2-deoxycoelenterazine(h-CTZ)的氧化化学发光。
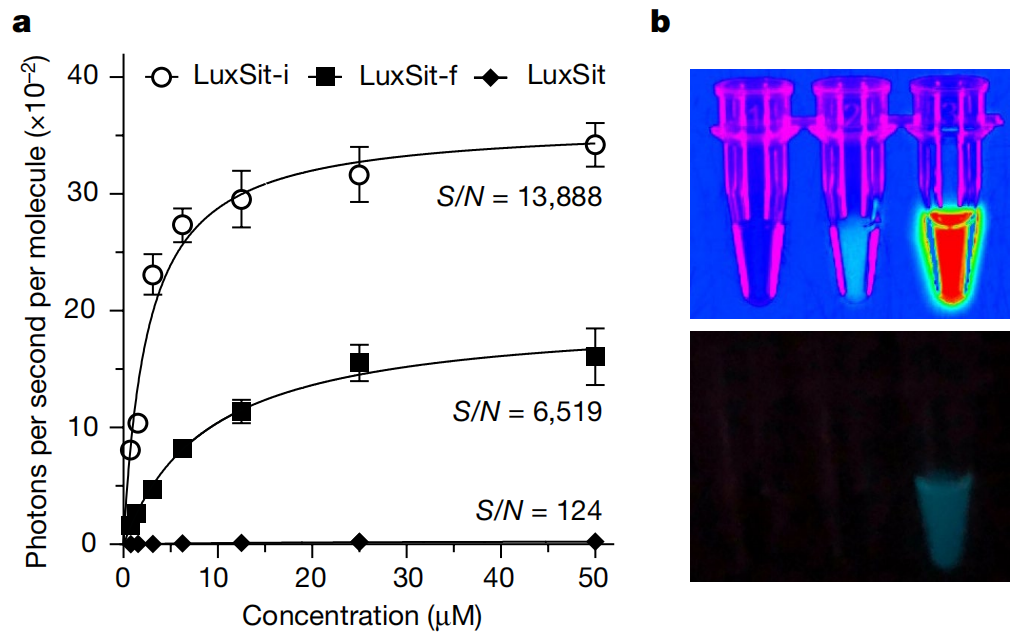
人造荧光素酶特异性识别、结合荧光素底物并使其发光
进一步结构分析显示,该研究所设计的人造荧光素酶的活性催化位点将精氨酸胍基(带正电)定位于酶促反应过程中形成的、具有高度形状互补性的结合结构域中的阴离子(带负电)附近,两者通过静电相互作用结合到一起。
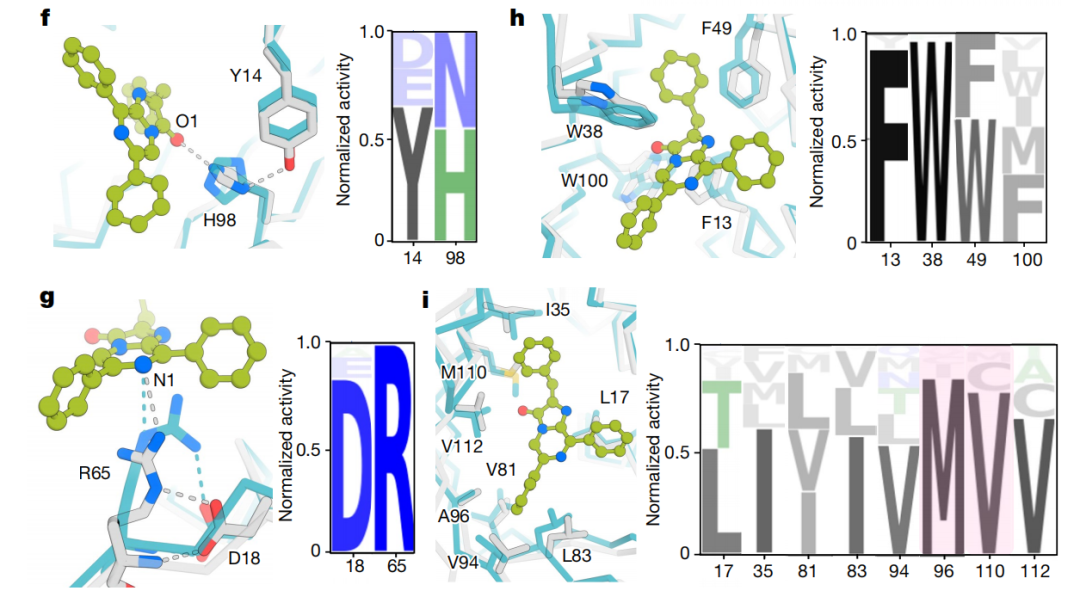
人造荧光素酶的活性催化位点和底物结合结构域
更重要的是,相比于天然荧光素酶,其中一种人造荧光素酶具有多种优势,例如分子量更小(13.9kDa)、耐热性更好(失活温度高于95°C)、底物特异性更高。与此同时,这种人造荧光素酶对diphenylterazine的催化效率与天然荧光素酶相当。
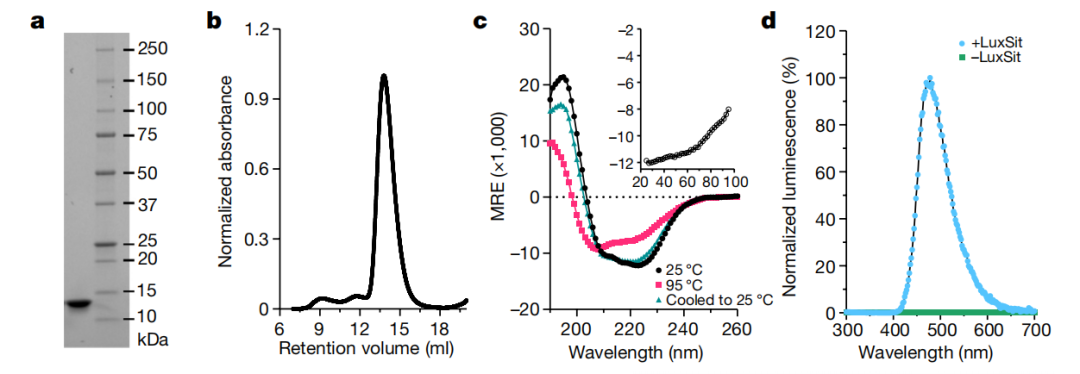
人造荧光素酶具有分子量小、耐热性好、底物特异性高和催化活性强等优点
值得一提的是,David Baker 教授在研究领域内素有“蛋白质折叠之父”之称,曾获2021年度科学突破奖·生命科学奖。

David Baker 教授
值得一提的是,David Baker 教授基于这项研究成果创立了一家名为 Monod Bio 的公司,这也是首个将蛋白质从头设计用于生物传感器和医疗诊断的公司,该公司具有包括LucCage生物传感器平台和LuxSit从头设计光素酶平台等核心技术。该公司于2022年8月完成2500万美元种子轮融资。

该论文的第一作者、Monod Bio 公司的科学联合创始人 Andy Hsien-Wei Yeh 博士表示,如今我们能够在电脑上从头开始设计非常高效的酶,而不再依赖于自然界中发现的酶。这一突破意味着,原则上可以为几乎任何化学反应设计定制酶。
总而言之,这项研究开发了一种基于深度学习的人工智能算法——Family-wide Hallucination,可以从头设计出具有高催化活性、高底物特异性、结构紧凑和耐热性好的人造荧光素酶,这或将成为深度学习算法辅助设计人造酶的关键里程碑。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


