两篇Nature论文发现了一种新的CRISPR-Cas剪刀---CRISPR–Cas12a2
来源:生物谷原创 2023-01-10 10:42
两篇Nature论文描述了一种新发现的CRISPR-Cas免疫系统的结构和功能,与更知名的让外来基因灭活来保护细胞的CRISPR-Cas系统不同,这种新的系统关闭受感染的细胞来阻挡感染。
像人类一样,细菌和古生菌也会受到病毒的攻击。这些微生物已进化出自己的免疫防御策略,以对抗它们的病原体。细菌防御系统,如CRISPR-Cas系统,具有多样化的蛋白和功能,帮助细菌保护自己免受外来入侵者入侵。
这种免疫防御基于一个共同的机制:CRISPR核糖核酸(CRISPR ribonucleic acid, crRNA)作为“向导RNA(gRNA)”,帮助检测外来基因组(比如病毒DNA)的区域,以便进行靶向切割。由crRNA指导的CRISPR相关(Cas)核酸酶可以像一把剪刀一样切割它的靶标:这是人类在许多技术中利用的一种自然策略。

美国犹他州立大学的生物化学学者Thomson Hallmark和Ryan Jackson与他们的合作者一起,发表了两篇具有开创性的论文。他们的研究结果描述了一种新发现的CRISPR-Cas免疫系统的结构和功能,与更知名的让外来基因灭活来保护细胞的CRISPR-Cas系统不同,这种新的系统关闭受感染的细胞来阻挡感染。相关研究结果于2023年1月4日在线发表在Nature期刊上,论文标题分别为“Cas12a2 elicits abortive infection through RNA-triggered destruction of dsDNA”和“RNA targeting unleashes indiscriminate nuclease activity of CRISPR–Cas12a2”。

Jackson说,“通过这种称为CRISPR-Cas12a2的新系统,我们观察到了它的结构和功能与迄今为止在CRISPR-Cas系统中观察到的结构和功能都不同。”
作为第一篇论文第一作者的Oleg Dmytrenko博士说,“我们正在探索最初与Cas12a归类在一起的CRISPR核酸酶,这类核酸酶通过识别和切割侵入性DNA来保护细菌。一旦我们发现了更多的它们,我们就意识到它们与Cas12a有足够的不同,可以进行更深入的研究。这种探索使我们发现这些我们称之为Cas12a2的核酸酶,它们不仅与Cas12a有很大的不同,而且与任何其他已知的CRISPR核酸酶也有很大的不同。”
关键的区别在于它们的防御行动机制。当Cas12a2识别入侵的RNA时,该核酸酶会对它进行切割,但也能破坏细胞内的其他RNA和DNA,破坏该细胞的生长并限制感染的扩散。Dmytrenko说,“一般来说,这种称为顿挫性感染的防御策略在细菌中已经被发现。其他一些CRISPR-Cas系统以这种方式工作。然而,一种基于CRISPR的防御机制,依靠单一的核酸酶来识别入侵者并降解细胞DNA和RNA,以前还没有被观察到。”
Cas12a2的蛋白序列和结构将这种核酸酶与Cas12a区分开来。在一种前间隔序列侧翼位点(protospacer-flanking sequence, PFS)的激活下,Cas12a2能识别与它的gRNA互补的靶RNA。靶向靶RNA会引发附带的核酸裂解,降解RNA、单链DNA和双链DNA。这种活性导致细胞停滞,可能是通过破坏细胞中的DNA和RNA,从而损害生长。Cas12a2可用于分子诊断和RNA生物标记物的直接检测,这已得到原理证明。
Jackson和Hallmark是正在破译CRISPR-Cas系统的基本结构,以及是什么让它们运作的全球研究人员中的一员。Jackson说,“我们在这两篇论文中报道的研究结果几乎是在六年内完成的。”
在过去五年中被确认为一种独特的免疫系统,CRISPR-Cas12a2在某种程度上类似于更知名的CRISPR-Cas9,后者与目靶DNA结合并像分子剪刀一样切割它,从而有效地关闭靶基因。但是CRISPR-Cas12a2与CRISPR-Cas9结合的靶标不同,而且这种结合具有非常不同的效果。
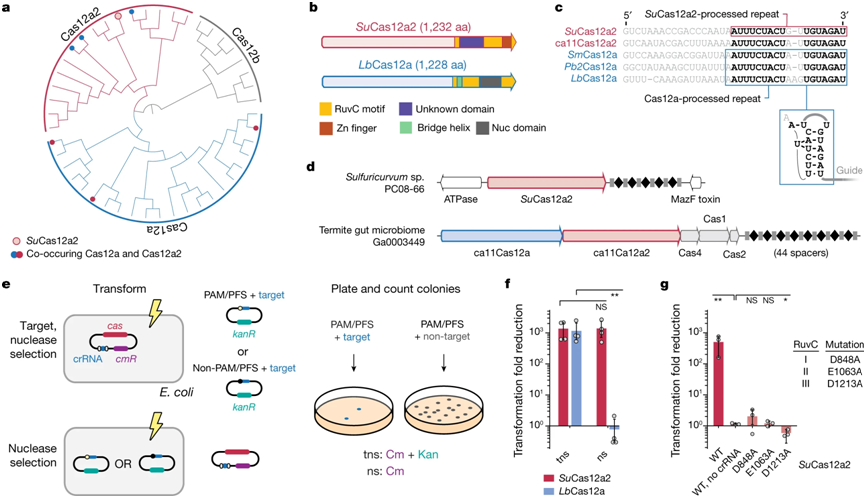
Cas12a2核酸酶在V型Cas12核酸酶中形成了一个独特的分支。图片来自Nature, 2023, doi:10.1038/s41586-022-05559-3。
Jackson说,“Cas12a2蛋白在与RNA结合时发生了重大的构象变化,为DNA的破坏打开了一个不加区分的活性位点。Cas12a2破坏了靶细胞中的DNA和RNA,导致它们衰老。”
通过使用低温电镜(cryo-electron microscopy, cryo-EM),这些作者展示了CRISPR-Cas12a2的这一独特方面,包括它的RNA触发的单链RNA、单链DNA和双链DNA的降解,从而导致一种自然发生的防御策略,即顿挫性感染(abortive infection,也译为流产性感染)。
Hallmark说,“顿挫性感染是细菌和古生菌用来限制病毒和其他病原体传播的一种天然噬菌体抵抗策略。比如,顿挫性感染可以阻止已感染了宿主细胞的病毒成分进行复制。”
Jackson说,该团队在Cas12a2切割双链DNA的过程中捕捉到了它的结构。他说,“令人难以置信的是,Cas12a2核酸酶将通常笔直的一段双螺旋DNA弯曲了90度,以迫使这段双螺旋DNA的骨架进入这种核酸酶的活性位点,并在那里遭受切割。这是一种结构上的变化,观察起来很不寻常---这种现象引起了科学家同行的惊呼。”
在进一步结构分析中,他们发现Cas12a在免疫反应的不同阶段与它的靶RNA结合后会发生重大结构变化。这反过来又导致核酸酶出现一个暴露的裂缝,可以粉碎它遇到的任何核酸--无论是RNA、单链DNA还是双链DNA。他们还发现了一种让Cas12a2发生突变以改变它在识别它的RNA靶标后降解的核酸的方法。这些具体细节为未来开辟了潜在的广泛技术应用。
Jackson说,健康细胞和恶性细胞或被感染的细胞之间存在遗传上的区别。他说,“如果可以利用Cas12a2在遗传水平上识别、靶向和摧毁细胞,那么它的潜在治疗应用意义重大。”
此外,这两篇论文中描述的CRISPR-Cas12a2的RNA诊断能力,可能推动阻止一些遗传性疾病影响的努力。
Jackson说,“我们只是触及表面,但我们相信CRISPR-Cas12a2可能导致改进其他CRISPR-Cas技术,这将大大有利于社会。” (生物谷 Bioon.com)
参考资料:
1. Oleg Dmytrenko et al. Cas12a2 Elicits Abortive Infection via RNA-triggered Destruction of dsDNA. Nature, 2023, doi:10.1038/s41586-022-05559-3.
2. Jack P. K. Bravo et al. RNA Targeting Unleashes Indiscriminate Nuclease Activity of CRISPR-Cas12a2. Nature, 2023, doi:10.1038/s41586-022-05560-w.
3. Biochemists describe structure and function of newly discovered CRISPR immune system
https://phys.org/news/2022-12-biochemists-function-newly-crispr-immune.html
4. Researchers discover new type of CRISPR gene scissors
https://medicalxpress.com/news/2023-01-crispr-gene-scissors.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


