研究解析人类高原低氧适应的调控机制
来源:昆明动物所 2020-10-12 19:20
高原低氧环境适应的分子机制是进化和遗传领域的重要科学问题,长期以来受到广泛关注。近十年来,中国科学院昆明动物研究所研究员宿兵团队与西藏大学教授崔超英合作,通过分析大规模的高原藏族人群样本和比较基因组学数据,发现包括EPAS1和EGLN1在内的一系列与藏族高原适应相关的候选基因(Peng et al. Mol. Biol. Evol. 2011;Xiang e
高原低氧环境适应的分子机制是进化和遗传领域的重要科学问题,长期以来受到广泛关注。近十年来,中国科学院昆明动物研究所研究员宿兵团队与西藏大学教授崔超英合作,通过分析大规模的高原藏族人群样本和比较基因组学数据,发现包括EPAS1和EGLN1在内的一系列与藏族高原适应相关的候选基因(Peng et al. Mol. Biol. Evol. 2011;Xiang et al. Mol. Biol. Evol. 2013;Yang, et al. Hum. Mut. 2016;Zheng et al. Zool. Res. 2017;Guo et al. Zoo. Res. 2017;Ouzhuluobu et al. Nat. Sci. Rev. 2020),进一步利用功能组学分析,证实了这些基因参与藏族人群的高原适应(Peng et al. Mol. Biol. Evol. 2017; He et al. Nat. Sci. Rev. 2018)。然而,鉴于已发现的大部分在藏族人群中富集的适应性突变都发生在非编码区域,为系统破译这些位点的分子调控机制和功能效应带来挑战。
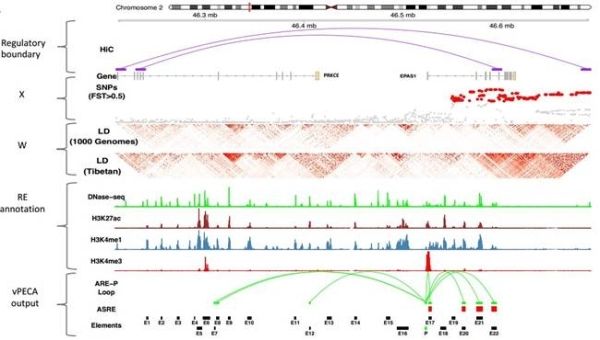
近年来,随着多组学技术尤其是表观染色质状态和三维结构测序技术的发展和广泛应用,为解析这些非编码区域变异的调控机制带来契机。为系统解析藏族人群适应高原低氧的分子调控机制,宿兵团队与中科院数学与系统科学研究院研究员王勇团队、斯坦福大学和西藏大学合作,设计实验采集、测量、比较藏族适应型和汉族野生型两种脐带内皮细胞(HUVEC)在低氧和常氧条件下及不同时间节点上的多组学数据,包括基因组、转录组、染色质可及性(ATAC-seq)和染色质空间构象(Hi-C)数据,进一步发展出新的方法论框架——vPECA (Variants interpretation model by Paired Expression and Chromatin Accessibility data),整合基因组-表观组-转录组-表型层面的数据,构建以受选择调控元件为核心的基因调控网络模型,系统分析藏族高原低氧适应的调控机制。该模型可检测位于非编码区变异位点是否在群体中受到选择,同时位于具有调控活性的调控元件上,并在调控网络中影响下游基因表达水平。研究团队利用该模型,揭示EPAS1基因表达由受选择和不受选择两类调控元件组合调控,发现3个位于增强子区域的功能位点,这3个位点通过削弱所在区域的染色质开放程度(可及性),进而下调EPAS1的表达,从而避免藏族人群在高原低氧环境过高表达EPAS1带来的负效应(如红细胞过度增生)。此外,研究人员还构建EPAS1基因的下游调控网络,解析下游受选择靶基因的调控机制,在网络中探索高原适应相关表型的联系。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


