Cell Rep Med:免疫靶向作用癌症融合蛋白或有望治疗罕见的人类肝癌
来源:生物谷原创 2024-04-02 14:41
本文研究结果为揭示人类新抗原特异性谱的片段特性提供了新的见解,并为在临床上开发针对人类FLC的成功免疫疗法证明了方向。
纤维板层肝细胞癌(FLC,fibrolamellar carcinoma)是一种罕见的肝癌,如果不及时尽早手术治疗的话,患者的预后将会很差,这种疾病是由能产生一种融合蛋白的单一遗传突变所引起的,近日,一篇发表在国际杂志Cell Reports Medicine上题为“DNAJB1-PRKACA fusion neoantigens elicit rare endogenous T cell responses that potentiate cell therapy for fibrolamellar carcinoma”的研究报告中,来自美国圣犹大儿童研究医院等机构的科学家们通过研究发现了一种特殊的免疫细胞蛋白,其或能靶向作用FLC并引起其破坏。
如今科学家们发现,FLC患者中天然产生的T细胞能独特识别融合蛋白,这些细胞或许为科学家们开发治疗FLC的新型免疫疗法奠定了一定的基础。融合蛋白是由DNA损伤将两种不同的基因连接在一起所产生的,有时这种杂交的基因会产生一种融合蛋白并帮助细胞癌变,所有的FLC肿瘤都是由DNAJB1和PRKACA基因的融合所驱动的,其通常会在超过90%的FLC患者的基因组的同一位置发生。
由于这种融合蛋白并不存在于正常细胞中,因此宿主机体的免疫系统应该能够找到这种融合蛋白并摧毁携带其的癌细胞,然而,这一概念依赖于T细胞对融合蛋白的识别和反应,研究人员表示,他们发现了两种罕见的T细胞或许就能做到这一点,而这一研究发现也阐明了一种新型疗法的概念。Allison Kirk教授说道,我们利用患者机体的T细胞受体,其能引导T细胞杀灭携带融合蛋白的肿瘤细胞,这一方法在小鼠模型中效果非常好。
T细胞是一种特殊的白细胞,其能寻找并杀灭机体中被感染或癌变的细胞,这些免疫细胞能利用T细胞受体来寻找其靶点,而T细胞受体则能将细胞引导到肿瘤上的特定蛋白中,这类似于执法部门利用面部识别来寻找最烦,这种引起FLC的融合蛋白在体内能作为一种难以识别的危险逃亡物。
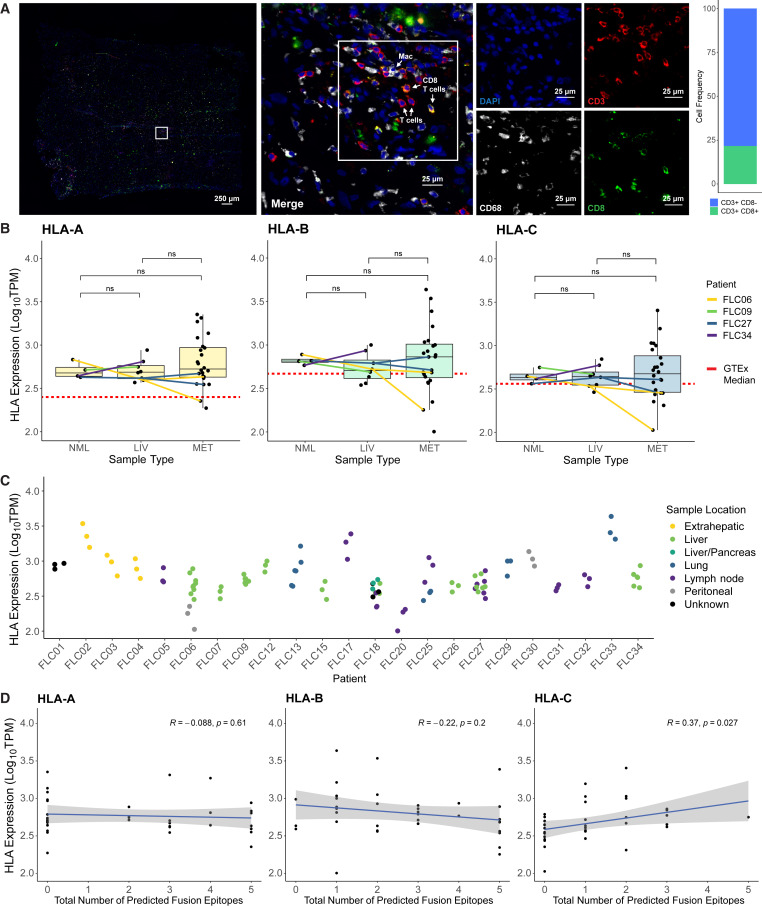
免疫靶向作用癌症融合蛋白或有望治疗罕见的人类肝癌
图片来源:Cell Reports Medicine (2024). DOI:10.1016/j.xcrm.2024.101469
在60%-80%的病例中,FLC肿瘤并不能通过手术切除,即使经过治疗,患者的疾病也会复发且会在10年内死亡,除了手术外,目前并没有有效的治疗方法,这就促使科学家们开始寻找新的方法,当科学家们将能识别融合蛋白的T细胞受体加入到携带FLC样肿瘤的小鼠机体中数百万个T细胞中时,他们发现肿瘤尺寸显著下降了,且能表达融合蛋白的所有癌细胞都被消除了。从本质上来讲,研究人员在肿瘤中注入了免疫“执法者”,而且这是事先准备好的,这往往离不开融合蛋白。
在人类机体中,一种称之为T细胞受体转基因(TCR-T)免疫疗法的类似手段则能将患者自身的T细胞加入到融合蛋白特异性T细胞受体中,这种经过修饰的T细胞随后就会被输注到患者体内并开始寻找摧毁肿瘤。本文研究还证实了,机体对融合蛋白所产生的天然免疫反应或许是可能的,即使这种情况非常少见,实际上,科学家们仅发现了两种针对融合的天然体细胞反应,当面对这种罕见的情况时,研究人员尝试利用这两种受体来推断出其它受体的样子。
研究者Paul Thomas说道,一旦我们看到了一些T细胞受体观察到抗原的例子,我们通常就能进行相关预测,而且我们还发现这两种受体看起来一点都不像,也不像我们在患者身上观察到的那样,因此其或许都是独一无二的。如此罕见的研究结果表明,科学家们或许不太可能找到针对先前存在的肿瘤所产生的另一种天然反应,于是他们测试了很多其它患者,仅发现了两种T细胞反应,其都来自于单一的患者,这或许是一种非常罕见的反应,而研究人员很幸运地发现了它。
目前研究人员仍然并不清楚针对FLC最有效的疗法到底是什么,但相关研究发现表明,携带能对融合蛋白产生反应的T细胞的单一个体或许就为开发新型疗法提供了一定的机会。最后研究人员只发现了一个对FLC融合蛋白能产生免疫反应的患者,但这就足以推动他们进行下一步研究来开发更为有效的FLC新型疗法了。综上,本文研究结果为揭示人类新抗原特异性谱的片段特性提供了新的见解,并为在临床上开发针对人类FLC的成功免疫疗法证明了方向。(生物谷Bioon.com)
参考文献:
Allison M. Kirk,Jeremy Chase Crawford,Ching-Heng Chou,et al. DNAJB1-PRKACA fusion neoantigens elicit rare endogenous T cell responses that potentiate cell therapy for fibrolamellar carcinoma, Cell Reports Medicine (2024). DOI:10.1016/j.xcrm.2024.101469
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


