2022年1月Science期刊不得不看的亮点研究
来源:本站原创 2022-01-31 23:59
2022年1月31日讯/生物谷BIOON/---2022年1月31日讯/生物谷BIOON/---2022年1月份即将结束了,1月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Science:利用人类大脑类器官,揭示结节性硬化症的起源doi:10.1126/science.abf5546在一项新的研究中,在大脑类器官的帮助
2022年1月31日讯/生物谷BIOON/---2022年1月31日讯/生物谷BIOON/---2022年1月份即将结束了,1月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Science:利用人类大脑类器官,揭示结节性硬化症的起源
doi:10.1126/science.abf5546
在一项新的研究中,在大脑类器官的帮助下,来自奥地利科学院和维也纳医科大学等研究机构的研究人员能够确定结节性硬化症(tuberous sclerosis complex, TSC)是一种罕见的神经发育遗传性疾病,它是在发育过程中产生的,而不仅仅是在遗传上。通过这些来自患者的人类大脑实验室模型,他们将这种疾病的起源确定为人类特有的尾侧晚期中间神经元祖细胞(caudal late interneuron progenitor, CLIP)。这些研究结果进一步表明,只有使用人类衍生的大脑类器官模型才能很好地理解影响人类大脑的疾病的病理。相关研究结果发表在2022年1月28日的Science期刊上,论文标题为“Amplification of human interneuron progenitors promotes brain tumors and neurological defects”。
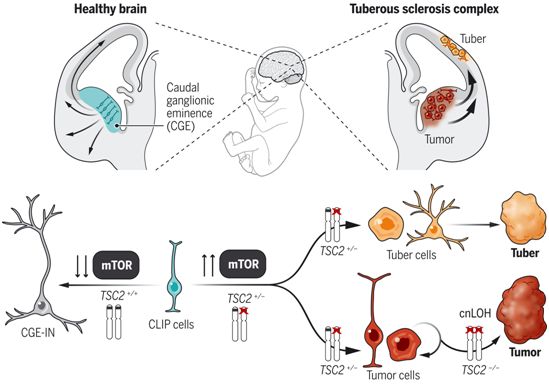
在妊娠中期,尾侧神经节隆起中的CLIP细胞产生迁移到皮层的中间神经元。图片来自Science, 2022, doi:10.1126/science.abf5546。
2.Science:我国科学家开发出麦角酸二乙基酰胺和裸盖菇素的非致幻类似物,有望治疗精神疾病
doi:10.1126/science.abl8615
在一项新的研究中,来自中国科学院生物化学与细胞生物学研究所、上海科技大学和苏州大学的研究人员开发出麦角酸二乙基酰胺(LSD)和裸盖菇素(psilocybin)的非致幻类似物,有可能用于治疗精神疾病。相关研究结果发表在2022年1月28日的Science期刊上,论文标题为“Structure-based discovery of nonhallucinogenic psychedelic analogs”。在这篇论文中,他们描述了他们构建出的类似物以及它们在小鼠身上的表现。
在这项新的研究中,这些作者使用X射线晶体学仔细观察了LSD和裸盖菇素,并能够确定它们与神经受体5-HT2AR结合时的构象。他们发现这两种分子都能以两种方式与5-HT2AR结合,从而形成独特的构象。他们随后构建出能以他们发现的第二种结合方式与5-HT2AR结合的化合物。
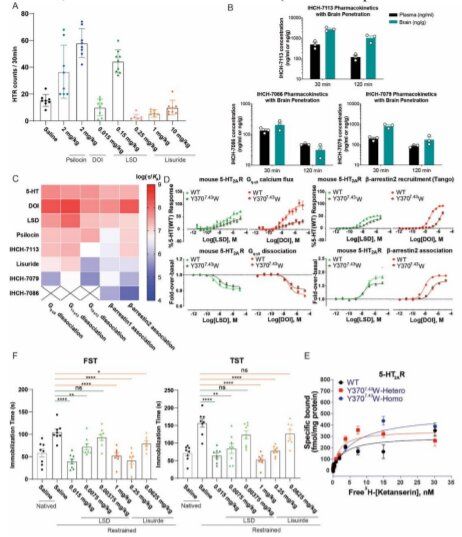
迷幻剂对幻觉和抑郁相关动物行为的影响,图片来自Science, 2022, doi:10.1126/science.abl8615。
3.Science:构建出血液蛋白形态图谱,鉴定出有潜力预测肝脏移植排斥的生物标志物
doi:10.1126/science.aaz5284
在一项新的研究中,来自美国西北大学等研究机构的研究人员发现体内的蛋白家族有可能预测哪些患者有可能会排斥新移植的器官,从而帮助患者做出治疗决定。这一进展标志着对特定细胞中的蛋白进行更精确研究的新时代的开始。相关研究结果发表在2022年1月28日的Science期刊上,论文标题为“The Blood Proteoform Atlas: A reference map of proteoforms in human hematopoietic cells”。
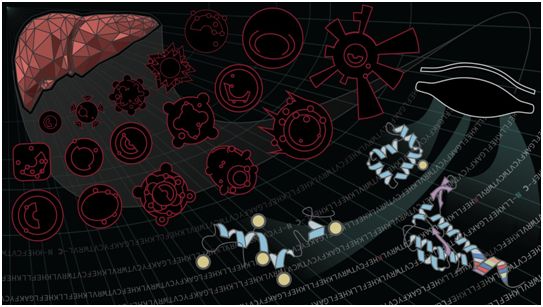
血液蛋白形态图谱(BPA)汇集了从21种人类细胞类型和血浆中鉴定出的约56000种蛋白形态。图片来自Kelleher and Levitsky labs at Northwestern University。
这种BPA图谱概述了超过56000种确切的蛋白分子(称为蛋白形态),因为它们出现在21种不同的细胞类型中---这些结构比以前类似的研究中出现的几乎多10倍。
4.Science:挑战常规!揭示DNA结合蛋白高效结合DNA靶序列的新机制
doi:10.1126/science.abg7427
在一项新的研究中,来自瑞典乌普萨拉大学的研究人员展示了DNA结合蛋白如何在不受到阻碍的情况下在整个基因组中搜索它的靶序列。这一结果与我们目前对基因调控的理解------遗传密码影响DNA结合蛋白的结合频率,但不影响它的结合时间---相矛盾。相关研究结果发表在2022年1月28日的Science期刊上,论文标题为“Sequence specificity in DNA binding is mainly governed by association”。
当DNA结合蛋白在遗传密码中寻找它们的靶序列时,它们沿着DNA螺旋滑动以加快这一过程。当它们最终找到正确的位置时,它们停留在那里;与“正确的”靶序列的相互作用阻止了它们的滑行。这一机制已被广泛接受来描述这一搜索过程。这确是一个吸引人的假说,但它提出了一个恼人的问题---DNA代码中充满了许多“几乎正确”的序列。如果DNA结合蛋白在特定的DNA基序上停留的时间是由序列决定的,那么执行搜索任务的DNA结合蛋白将不断地在与它们的靶序列相似的序列上逗留。
论文第一作者、乌普萨拉大学的Emil Marklund说,“如果教科书上的解释是正确的,那么DNA结合蛋白会一直停留在靶序列之外。基因调控将非常无效,但我们从以前的研究中知道,情况并非如此。我们最熟悉的DNA结合蛋白LacI在几分钟内就能在460万个碱基对中找到它的靶序列。”
为了解决这一悖论,这些作者让DNA结合蛋白LacI在安装在一个微芯片上的数千个不同的DNA序列上来回滑动。一种荧光分子附着在LacI蛋白上,使得测量LacI附着在不同DNA序列上的速度以及它从中释放下来的速度成为可能。所获得的结果是令人吃惊的。与之前的假设相反,DNA序列对LacI与DNA结合的时间几乎没有影响。然而,当遇到的DNA序列与靶序列相似时,滑动的LacI更有可能短暂地停留下来。换句话说,DNA结合蛋白经常也会离开它们要调节的序列,但是在靶位点,它们总是在找到它们的路径之前进行非常短的旅程。在宏观的时间尺度上,这看起来是一种稳定的相互作用。
5.Science:通过数学建模揭示细胞如何选择自身命运
doi:10.1126/science.abg9765
多稳定性(multistability)允许基因相同的细胞存在数千种分子不同和有丝分裂稳定的状态。构建合成的多稳定回路可以深入了解足以实现多稳定性的最小回路,并为在工程化细胞疗法
中利用多细胞性建立基础。然而,针对哺乳动物细胞的研究工作仅限于双状态系统,或使用了不能轻易扩展的架构。除了产生长期的多稳定性,一种理想的合成架构还应重现天然细胞命运
控制系统的关键特性,包括用瞬时的外部输入让细胞在不同状态之间切换的能力、控制特定状态的稳定性的能力,以及产生不可逆的状态转换的能力。尽管在确定许多天然细胞命运控制系
统中的关键基因和调节相互作用方面开展了大量研究工作,但是仍不清楚哪些回路架构可以提供这些能力。
天然细胞命运控制系统表现出两种普遍的特征:积极的自动调节和组合性的蛋白-蛋白相互作用。在一项新的研究中,来自美国加州理工学院的研究人员根据类似的原则设计出一种称为
MultiFate的最小回路架构,在这种架构中,一组转录因子竞争性地形成同源二聚体和异源二聚体,只有同源二聚体才能激活它们自身基因的表达。相关研究结果发表在2022年1月21日的
Science期刊上,论文标题为“Synthetic multistability in mammalian cells”。

MultiFate支持长期、可控和可扩展的多稳定性,图片来自Science, 2022, doi:10.1126/science.abg9765。
6.Science:新研究揭示EBV感染可能是导致多发性硬化症的主要原因
doi:10.1126/science.abj8222
多发性硬化症(MS)是一种影响全球280万人的渐进性疾病,目前尚无明确的治疗方法。在一项新的研究中,来自美国哈佛大学陈曾熙公共卫生学院的研究人员发现多发性硬化症可能是由
爱泼斯坦-巴尔病毒(EBV, 也称为EB病毒)感染引起的。他们的研究结果于2022年1月12日在线发表在Science期刊上,论文标题为“Longitudinal analysis reveals high prevalence
of Epstein-Barr virus associated with multiple sclerosis”。
论文通讯作者、哈佛大学陈曾熙公共卫生学院流行病学与营养学教授Alberto Ascherio说,“我们团队和其他人对EBV导致多发性硬化症的假设已经研究了好几年,但这是第一个提供令人
信服的因果关系证据的研究。这是一大进展,因为它表明大多数多发性硬化症病例可以通过阻止EBV感染来预防,并且靶向EBV可能导致发现治愈多发性硬化症的方法。”

多发性硬化症导致神经元脱髓鞘。CD68染色组织显示病变区域有多个巨噬细胞。图片来自Marvin 101/Wikipedia。
7.Science:流式细胞仪技术取得里程碑式进展
doi:10.1126/science.abj3013
作为一家全球医疗技术公司,BD公司(Becton, Dickinson and Company)宣布,与欧洲分子生物学实验室(EMBL)合作进行的一项研究,作Science期刊最新一期的封面故事发表,介绍
了BD公司在流式细胞仪方面的一项新创新,它增加了荧光成像和基于图像的决策,根据每个细胞的视觉细节而不是仅仅根据存在的生物标志物的类型或数量,以极高的速度对单个细胞进行
分类。这项新技术有可能改变免疫学、细胞生物学和基因组学研究,并实现新的基于细胞的治疗发现。相关研究结果发表在2022年1月21日的Science期刊上,论文标题为“High-speed
fluorescence image–enabled cell sorting”。
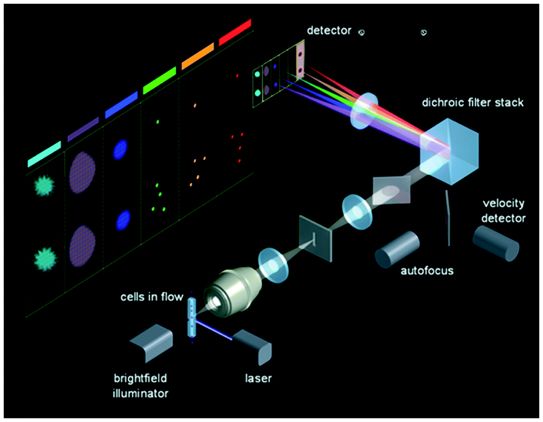
ImageStream的光学器件,图片来自Lab on a Chip, 2016, doi:10.1039/C6LC01063F。
通过在传统的生物标志物识别和定量确定中加入成像技术,这种新技术不仅能识别细胞中是否存在某种生物标志物以及存在多少,还能识别其位置或在细胞中的分布情况。通过用这种技术 对生物标志物的分布进行成像,这些作者获得了以前在传统流式细胞仪实验中看不到的关于细胞的详细信息,这使他们能够回答复杂的生物学问题,如细胞如何生长、发挥功能和相互作用 ,或研究病毒或蛋白在细胞内的确切位置,所有这些都是以高度加快的速度进行的。
8.Science:揭示辛醛促进动脉粥样硬化机制
doi:10.1126/science.abg3067
在一项新的研究中,来自美国拉霍亚免疫学研究所的研究人员发现动脉中的免疫细胞可以“嗅”出它们周围的环境并引起炎症。相关研究结果发表在2022年1月14日的Science期刊上,论文
标题为“Olfactory receptor 2 in vascular macrophages drives atherosclerosis by NLRP3-dependent IL-1 production”。
这项新的研究表明这种炎症会导致小鼠的心血管疾病和动脉粥样硬化。这些作者通过阻断称为巨噬细胞的免疫细胞对一种叫做辛醛(octanal)的化合物的感应来逆转这种炎症。
每个人的血液中都有少量的辛醛,但是这些作者发现具有心血管疾病标志物(比如较高的LDL胆固醇)的人也有较高的辛醛水平。这种额外的辛醛可能由于饮食或细胞中一种叫做氧化应激
的现象而最终进入血液。
9.Science:人类免疫系统用来促进细胞焦亡的gasdermin蛋白家族竟起源于细菌
doi:10.1126/science.abj8432
在一项新的研究中,来自美国丹娜法伯癌症研究院和以色列魏茨曼科学研究所的研究人员发现人类的免疫系统具有惊人的复杂性、微妙性和精密性,它包括一个有10亿年历史的细菌用来保
护自己免受病毒侵袭的蛋白家族。相关研究结果发表在2022年1月14日的Science期刊上,论文标题为“Bacterial gasdermins reveal an ancient mechanism of cell death”。
图片来自CC0 Public Domain。
论文共同通讯作者、丹娜法伯癌症研究院的Philip Kranzusch博士说,“世界各地的科学家们已经做了大量的研究工作来了解人类免疫系统的功能。人类免疫的关键部分在细菌中是共享的 ,这一发现为这个领域的研究提供了一个新的蓝图。”
10.Science:重大突破!注射脂质纳米颗粒封装的mRNA在体内产生CAR-T细胞,可显著逆转心脏纤维化
doi:10.1126/science.abm0594; doi:10.1126/science.abn0851
在一项新的研究中,来自美国宾夕法尼亚大学佩雷尔曼医学院的研究人员发现类似于基于信使RNA(mRNA)的COVID-19疫苗,一种实验性免疫疗法只需注射一次mRNA就能暂时重编程患者的免疫细胞以攻击特定靶标。相关研究结果发表在2022年1月7日的Science期刊上,论文标题为“CAR T cells produced in vivo to treat cardiac injury”。
这些作者证实这种新方法利用mRNA制剂重编程这种强大的称为T细胞的免疫细胞,经过重编程的T细胞可以攻击心脏成纤维细胞。心力衰竭通常部分上是由这些成纤维细胞驱动的,它们对心脏损伤和炎症作出的反应是长期过度地产生纤维物质,使心肌变硬,从而损害心脏功能---这种情况称为纤维化(fibrosis)。在模拟心力衰竭的小鼠实验中,这些经过重编程的T细胞引起的心脏成纤维细胞的减少导致了心脏纤维化的显著逆转。
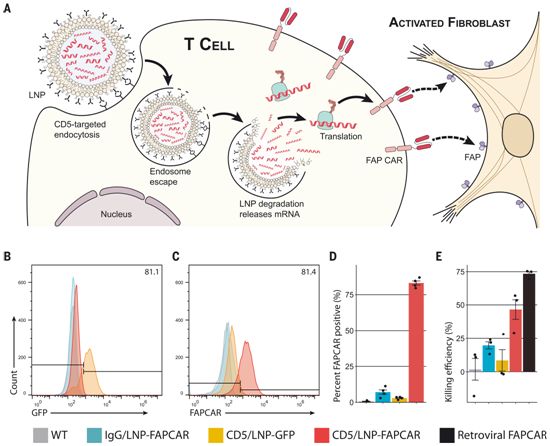
靶向CD5的脂质纳米颗粒在体外产生功能性的、基于mRNA的FAPCAR T细胞。图片来自Science, 2022, doi:10.1126/science.abm0594。
当注射到小鼠体内时,用脂质纳米颗粒封装的mRNA分子被T细胞摄取,并作为产生靶向成纤维细胞的T细胞受体的模板,从而有效地重编程T细胞以攻击活化的成纤维细胞。然而,这种重编程是非常短暂的。mRNA没有被整合到T细胞的DNA中,在T细胞内只存活了几天,之后T细胞恢复正常,不再靶向成纤维细胞。
这些作者发现,尽管发挥作用的时间短暂,但在心力衰竭模型的小鼠中注射mRNA,成功地重编程了大量的小鼠T细胞,使它们的心脏纤维化大大减少,并恢复了大部分正常的心脏大小和功能,而且治疗一周后没有证据表明它们的T细胞继续有抗纤维化的活性。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


