董一洲团队开发新型CAP-LNP,将mRNA递送到精母细胞,治疗男性不育症
来源:生物世界 2023-02-13 13:57
该研究开发的CAP-LNP可向精母细胞递送编码DNA减数分裂重组酶1(Dmc1)蛋白的传统mRNA以及自扩增RNA(saRNA),从而恢复Dmc1蛋白表达,治疗Dmc1基因突变引起的雄性不育症。
男性不育症是一种重要的生殖疾病,影响了全球至少7%的男性。目前,有些男性不育病例可以通过辅助生殖技术(ART)来治疗。然而,ART技术并不能解决因基因突变导致的男性不育问题。例如常见的导致男性不育的Sycp3基因突变和TEX11基因突变,这些基因突变通常与精母细胞蛋白功能异常、减数分裂阻滞和无精子症有关。不幸的是,目前临床上还没有有效的方法来恢复人类的这些遗传功能和生育能力。
为了解决男性不育症这一重要医疗需求,其中一个挑战是将治疗药物递送到患病细胞群(例如精母细胞)。脂质纳米颗粒(LNP)由于其低免疫原性和良好的递送效率,是目前应用最广泛的mRNA递送纳米材料之一。2020年,两款LNP递送的mRNA疫苗获批用于预防新冠病毒(SARS-CoV-2)感染。此外,还有许多研究在探索LNP-mRNA的各种治疗应用。
LNP能够有效递送到肝脏,一些新型LNP也实现了对肺、脾、心脏以及肿瘤组织的递送。但其在睾丸、特别是精母细胞中的有效递送仍然存在着巨大的挑战,这也是mRNA递送的一个有待开发的领域。
2023年2月7日,俄亥俄州立大学董一洲教授团队在 Advanced Science 期刊发表了题为:Cholesterol-Amino-Phosphate (CAP) Derived Lipid Nanoparticles for Delivery of Self-Amplifying RNA and Restoration of Spermatogenesis in Infertile Mice 的研究论文。
该研究开发了新型CAP-LNP载体,能够将mRNA高效递送至精母细胞,在DNA减数分裂重组酶1(Dmc1)基因敲除的无精子症小鼠模型中,CAP-LNP递送表达Dmc1蛋白的自扩增RNA(saRNA),能够长时间表达Dmc1蛋白,恢复无精子症小鼠模型的减数分裂和精子发生。
这项研究证明了通过LNP向精母细胞递送mRNA的可行性,据悉,这也是首次将saRNA应用于免疫治疗以外的遗传性疾病的治疗。这项研究为基因突变引起的男性不育症提供了一种新的潜在治疗方法。

董一洲,西奈山伊坎医学院终身教授。先后获得北京大学医学部药理学学士学位、上海有机化学研究所有机化学硕士学位及北卡罗来纳大学教堂山分校药学博士学位,在010-2014年,董一洲在纳米医学和mRNA先驱Robert Langer和Daniel Anderson教授实验室从事博士后研究工作。2014年,董一洲加入俄亥俄州立大学任助理教授,并于2018年晋升为副教授。2022年,董一洲作为终身教授加入西奈山伊坎医学院。董一洲是国际公认的LNP领域权威学者,他的实验室聚焦于设计和开发用于治疗癌症、遗传病和传染病的纳米颗粒递送系统及RNA疗法,发明了多种用于高效mRNA递送和基因组编辑的纳米载体,并全面改造了mRNA以改进了它们的蛋白质生产能力。

董一洲教授
为了促进mRNA向精母细胞的递送,研究团队关注了一些在生物膜和男性生殖系统中发挥重要作用的生物活性分子。例如,胆固醇是哺乳动物的细胞膜基本结构成分,之前有研究显示,精子发生过程中胆固醇水平升高,表明胆固醇代谢与生育能力之间存在密切关系。此外,磷酸基团是磷脂的极性部分,磷脂是生物膜的关键组成部分,参与细胞运输途径。最后,氨基可以被电离成带正电荷,这可以与带负电荷的mRNA相互作用。
除了生物活性外,可电离脂质的几何形状也可以极大地影响LNP的递送效率,几何形状可以用包封参数(P值)来描述,通常P值大的脂质有利于形成倒锥形,从而有利于有效载荷的内体逃逸。
在这项研究中,董一洲团队整合了上述三种生物活性成分,设计了一系列胆固醇-氨基-磷酸酯(CAP)脂质,然后配置为CAP-LNP,这些CAP脂质由两个刚性疏水尾部(胆固醇)、一个磷酸盐连接子和一个氨基头组成。这种结构组成有望促进相变、内体逃逸和有效载荷的释放。
接下来,研究团队使用这种合理设计的CAP-LNP载体向精母细胞递送编码正确蛋白的mRNA来恢复基因突变导致的精子发生障碍。研究团队选择了DNA减数分裂重组酶1(Dmc1)基因敲除小鼠作为模型,其表型与人类无精子症相似。
Dmc1基因突变会导致减数分裂停滞,因为Dmc1蛋白通过形成同源重组(HR)和修复DNA断裂,在减数分裂中发挥核心作用。恢复Dmc1基因敲除小鼠的精子发生,对于以减数分裂停滞为特征的人类无精子症的治疗具有强烈的临床意义。
研究团队使用CAP-LNP封装编码Dmc1蛋白的mRNA,这些mRNA是自扩增RNA(saRNA),在mRNA序列中加入了可复制序列,在进入细胞后可以像病毒一样,能够利用宿主细胞进行自我复制,从而在极低注射剂量的情况下实现蛋白的高表达。
然后,研究团队将这些CAP-LNP封装的Dmc1 saRNA微量注射到小鼠的生精小管中。随后,CAP-LNP可以向精母细胞的细胞质释放其中的mRNA,这些mRNA成功表达了Dmc1蛋白。最后,足够的Dmc1蛋白补充可以挽救精母细胞的染色体重组,从而恢复减数分裂和精子发生。
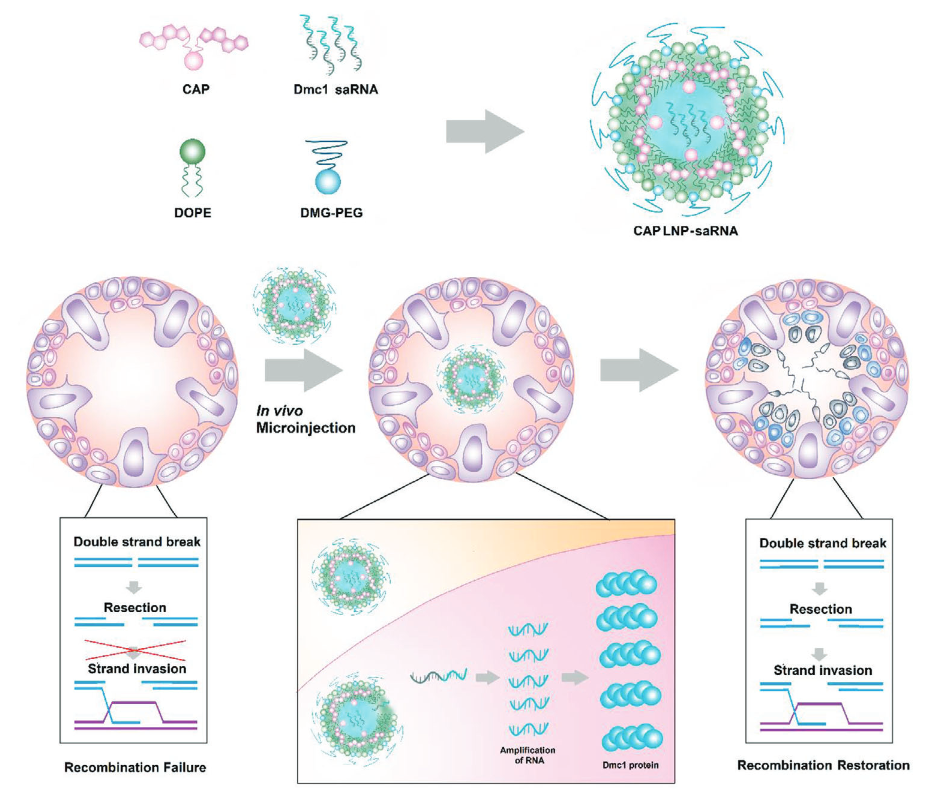
利用CAP-LNPs递送编码Dmc1的mRNA,将其注射到生精小管后,将Dmc1-mRNA递送至精原细胞,恢复其染色体重组和精子发生。
总的来说,该研究开发的CAP-LNP可向精母细胞递送编码DNA减数分裂重组酶1(Dmc1)蛋白的传统mRNA以及自扩增RNA(saRNA),从而恢复Dmc1蛋白表达,治疗Dmc1基因突变引起的雄性不育症。
值得注意的是,CAP-LNPs的递送效率明显高于MC3和ALC-0315 LNP。更重要的是,单次注射CAP-LNPs-saRNA可以长时间表达Dmc1蛋白,恢复Dmc1基因敲除小鼠模型的精子发生。
这项研究证明了通过LNP向精母细胞递送mRNA的可行性,据悉,这也是首次将saRNA应用于免疫治疗以外的遗传性疾病的治疗。这项研究为基因突变引起的男性不育症提供了一种新的潜在治疗方法。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


