种子轮融资2500万美元,波士顿初创瞄准「下一代」器官靶向性LNP,重点关注肺部疾病
来源:生辉 2023-06-19 10:59
近日,一家波士顿生物技术初创公司 Hopewell Therapeutics 宣布完成了 2500 万美元的种子轮融资,本轮融资的投资方包括 Mass Ave Capital、五源
近日,一家波士顿生物技术初创公司 Hopewell Therapeutics 宣布完成了 2500 万美元的种子轮融资,本轮融资的投资方包括 Mass Ave Capital、五源资本、山行资本、Forcefield Ventures(IMO Ventures)、BOPU Capital 和 WS Investments。
新闻稿中提到,本轮融资将用于搭建差异化器官靶向性脂质纳米微粒技术平台(ttLNP)、推进肺部疾病管线,以及开发突破心脑屏障的新一代脂质纳米微粒(LNP)。
(来源:公司官网)
这是一家成立于 2018 年的“新一代”基因治疗公司,由塔夫茨大学生物医学工程终身教授许巧兵博士创办,位于马萨诸塞州沃本市。该公司正在开发更高器官靶向性和更精准的 LNP,并基于此新型的递送载体开发“新一代”mRNA 基因治疗药物,重点方向瞄准了肺部疾病。完成本轮融资后,该公司预计在接下来 3-6 个月内启动新一轮融资,以用于重点项目的 IND 准备工作。
“公司独特的技术平台将重新定义基因药物的非病毒系统递送方式,实现对肝外组织的器官特异性靶向递送,并达到细胞层面的精准递送。正如公司的名字 Hopewell ,寓意着对新疗法的一种期盼以及为患者带来希望和明天。我们希望能通过新型高效的 LNP 开发基因治疗药物,从而缓解和消除病人的痛苦。”Hopewell Therapeutics 首席科学官张晓葵(Kate Zhang)博士告诉生辉。
▲图 | 张晓葵博士(来源:受访者提供)
张晓葵博士在酶替代物、单抗、小分子以及以基因编辑为基础的基因和细胞药物研发和管理方面拥有超 25 年的经验。她于 2022 年 8 月加入 Hopewell Therapeutics,致力于开发准确安全有效的递送方法,解决基因药物递送瓶颈,以推动“新一代”基因药物的广阔发展。此前,她在 Editas Medicine 担任负责生物基因药总开发副总裁,成功推进世界首例利用 CRISPR 技术 AAV 体内基因编辑治疗先天性失明 LCA10 的 IND、以及自体体外细胞 CRISPR 基因编辑治疗镰刀贫血和地中海贫血的 IND。她还领导开发临床前多重基因编辑的 iPSC 衍生自然杀伤细胞(iNK)用于液体和实体肿瘤适应症。张博士曾在健赞和赛诺菲长期任职,担任全球研发平台和全球药物开发高级总监,参与和领导不同阶段的 9 个从 IND 到 BLA 的生物药研发和商业化。还担任溶酶体贮积病诊断、筛查和监测的全球科学负责人。
许巧兵创办,底层技术已取得多个关键性突破
许巧兵在药物递送领域已经深耕近 16 年。他于 2007 年加入 MIT Robert Langer 实验室从事博士后研究工作,开始接触蛋白质和 mRNA 新型递送。2010 年,他加入塔夫茨大学生物医学工程系开展独立研究,研究方向是新型 LNP 的开发与应用。同年, Robert Langer 作为科学创始人联合创办 Moderna 公司。
“这一过程中,团队意识到,在基因治疗中,有效载荷一直在持续迭代和更新,也在越来越趋于复杂化,比方说,从基因片段、mRNA 到复杂的基因编辑和基因修正工具等等。这对药物递送工具的准确性包容性也提出了越来越高的要求,在此背景下,团队搭建了高价值的 ttLNP 技术平台,并将该平台推向工业化,在工业化制药的过程中进一步完善技术平台。”张晓葵说。
经过十几年的持续积累以及在 LNP 研究过程中不断取得重要进展,许巧兵团队日渐建立起了 LNP 体系,并获得了多项关键技术基础专利。
(来源:公司官网)
“这十几年来,科学创始人许巧兵团队引领了多个关键性的突破技术。一是,提出利用可电离脂质纳米微粒的结构,比如引进二硫键, 提高 LNP 的生物相容性,以进一步加大治疗指数提高药品安全性;二是,通过改变脂质纳米微粒本身分子结构的电分布达到准确递送到器官的靶向性,比如可靶向肺部,而无需加入第五个固定电荷的脂质纳米微粒;三是,进一步引领分子结构的设计和完善,达到细胞深度的靶向准确性, 比如靶向进入 T 细胞,肺泡 I 和 II 型细胞以及肺干细胞;四是,利用 LNP 递送不同的基因编辑工具,包括 Cas9、碱基编辑工具(base editor) 以及多种不同的 gene writer 技术;五是,搭建高通量 LNP 筛选平台,以达到根据不同的细胞挑选合适的 LNP。”
张晓葵进一步解释道,这些关键技术突破和进展为后续研发新型 LNP 开发了一片天地,能够丰富 LNP 的多样性、也可以扩展 LNP 的应用范围。
2018 年,许巧兵注册创办了 Hopewell Therapeutics 并担任首席技术官,着手转化这些研究成果。3 年后,许巧兵团队开始加速公司运营和转化工作,推进 ttLNP 技术平台的工业化。张晓葵坦言,这些研究成果和突破也是公司开发新型 LNP 递送载体以及“下一代”基因药物的底层技术。现阶段,相关技术专利也已经从塔夫茨大学通过授权许可方式引进到 Hopewell Therapeutics。
瞄准“下一代”组织靶向性 LNP,重点关注肺部疾病
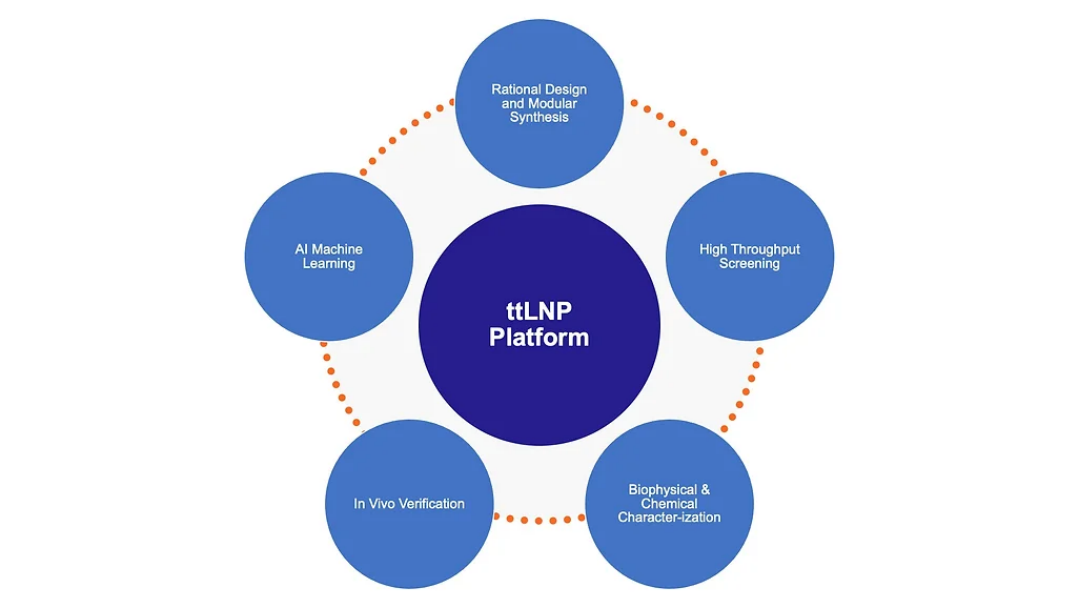
基于多年的研究,该公司搭建了 ttLNP 平台并不断优化和完善技术,推进发现、合成和研发“下一代”组织靶向性 LNP。目标是计划通过专有的平台技术克服当前 LNP 在器官和组织靶向、生物相容性和重复剂量持续表达方面的药物递送限制,开发出“下一代”基因治疗药物。
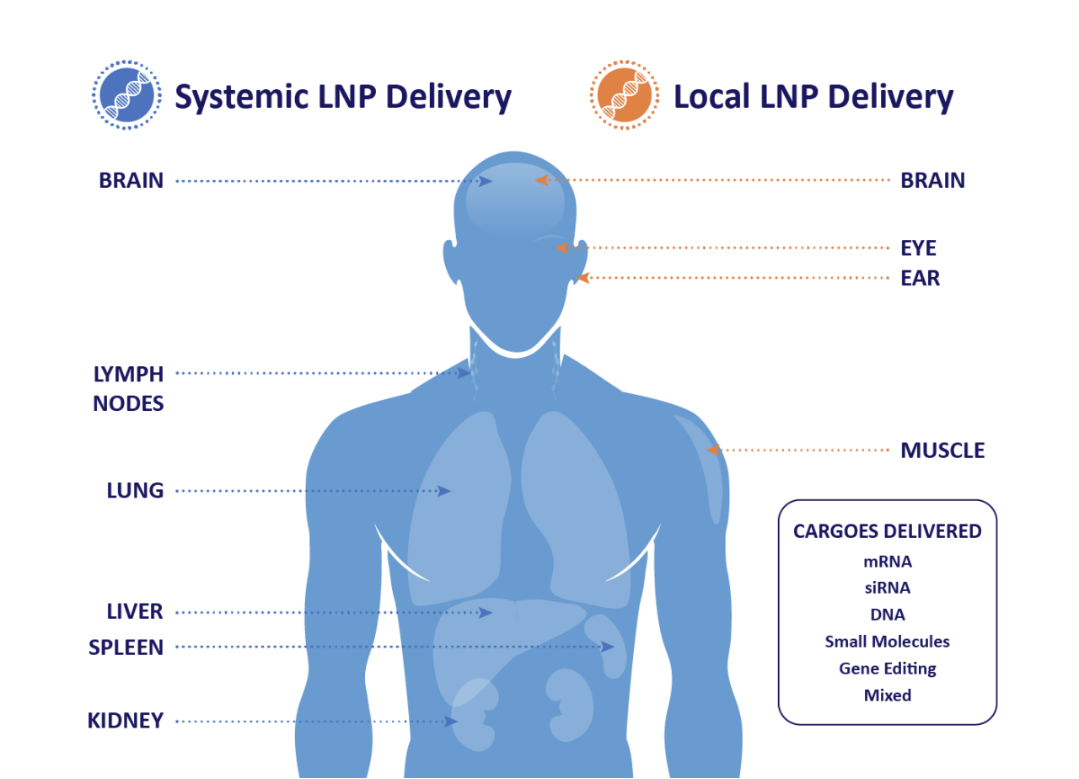
根据官网的介绍,该平台开发出的 LNP 已被证明能包裹多种基因荷载包括 mRNA、siRNA、DNA、基因编辑和基因编写工具,并将这些载荷递送到全身多个器官、组织和细胞,而不局限于肝部。
▲图 | ttLNP 平台(来源:公司官网)
“ 我们和合作伙伴已经在猴子试验中证明,系统性递送靶向组织在不同物种间具有很高的可转化性。这些进一步展示出,ttLNP 平台在生物医学多个领域的应用潜力。”张晓葵说。
公开资料显示,Hopewell Therapeutics 最初重点关注肺部疾病,开发出了 LNP-mRNA 管线,实现精确、靶向性肺细胞递送。后续也会持续筛选可突破血脑屏障的 LNP,将适应症扩展到神经系统疾病领域。“目前,公司已经针对靶向肺器官准确建立起结构和细胞之间的递送关系,开发出了 LNP 递送‘地图’,相当于拿到了靶向肺部递送的钥匙。”
张晓葵告诉生辉,多项研究结果已经显示,我们筛选出的 LNP 在多个物种中对不同肺部细胞类型具有高转染效率,能够递送基因药物到达肺部细胞,达到对多种细胞类型精准可调递送。这展现出系统性靶向肺部的 LNP 极具差异化和价值,对于治疗多种具有挑战性肺部疾病的潜力。
据悉,该公司开发的新型 LNP 在肿瘤等适应症中也表现出了一定的潜力。其淋巴器官特异性的 LNP 被视为开发下一代肿瘤免疫治疗和 mRNA 疫苗的关键。早期临床前数据显示,LNP-mRNA 能高效诱导 CD8+ T 细胞反应,在乳腺癌和黑色素瘤模型中展现出显著的预防和治疗效果。
(来源:公司官网)
“未来 3-5 年,Hopewell Therapeutics 将进一步开发肺部管线, 快速推进临床 POC,预计接下来 1-2 年内核心管线进入临床;同时公司也会通过和国际药企合作,在肿瘤、脑神经和传染病领域布局, 争取早日拿到早期临床数据。”
“LNP 会是未来基因药物发展的底层基础”
AAV、慢病毒等载体是基因治疗领域最常使用的病毒载体,应用潜力也已经得到了一定的验证。然而,现阶段的这些病毒还存在包裹有效载荷尺寸具有局限性,通常不超过 4.3 千碱基对,不能重复给药以及潜在免疫原性等问题。
“在有效载荷日趋复杂化的背景下,这些一定程度上影响了基因药物的开发。而 LNP 具有可重复给药、递送尺寸相对较大、安全性更高等优势,我认为 LNP 会是未来基因药物发展一个不可或缺的底层基础。”张晓葵说。
LNP 是一种由合成脂质和其他分子(胆固醇、磷脂等)组装而成的微小脂质囊泡。这是一种核酸药物最常用的非病毒载体,已被广泛用于 siRNA、mRNA 等药物的递送。采用 LNP,尤其是阳离子脂质纳米微粒进行药物递送的相关研究已有 30 余年的历史。
公开资料显示,当前,临床上进度较快或者已经获批的 mRNA 疗法几乎均选择了 LNP,当下以及未来很长一段时间,LNP 仍然是一个主流递送工具。
(来源:CAS)
不过,正如硬币的正反面,LNP 也存在局限性。张晓葵坦言,虽然 COVID-19 疫苗的广泛应用为 LNP 发展带来了可遇不可求的临床数据,一定程度上展现出了 LNP 的生物相容性以及成药可行性,但是也为 LNP 从疫苗走向基因药物应用提出了关键的问题, 肝外器官靶向性、安全性、重复给药性、复杂多样的大分子的封装、稳定性。
“因此,通过多种技术解决这些问题会进一步推动 LNP 的成药性,尤其是,如果能够实现肝外器官精确靶向性,这会是 LNP 走向成功的一个关键里程碑。我们认为,随着技术的不断完善和优化,LNP 会成为引领‘下一代’基因药物发展的推动器,进一步拓展基因药物的适应症,治疗多种难治性疾病。”对于 LNP 带动的新一代基因药物发展,张晓葵充满信心。
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->