Nature子刊:曾朝阳/熊炜/龚朝建团队揭示HPV病毒编码circRNA,促进头颈鳞癌免疫逃逸
来源:生物世界 2024-10-14 09:27
该研究拓展了HPV在头颈鳞癌发病机制,特别是免疫逃逸分子机制的理解,并为头颈鳞癌的免疫治疗提供了新的靶点和潜在治疗方案。
近日,中南大学基础医学院肿瘤研究所曾朝阳、熊炜联合湘雅二医院口腔医学中心龚朝建,在 Nature Communications 期刊发表了题为:Human papillomavirus-encoded circular RNA circE7 promotes immune evasion in head and neck squamous cell carcinoma (人乳头瘤病毒编码的环状RNA circE7促进头颈鳞癌免疫逃逸)的研究论文。
该研究发现人HPV病毒通过编码环状RNA——circE7,下调免疫检查点分子Galectin-9的表达,从而促进头颈部鳞状细胞癌(HNSCC)免疫逃逸,并基于该发现提出了TIM-3(Galectin-9在T细胞上的受体)单抗与现有PD-1单抗联合使用提高头颈鳞癌免疫治疗效果的新思路。

circE7是目前唯一被鉴定的由HPV编码的环状RNA(circRNA),且仅由高危型HPV16编码,其生物学功能还很不明确。

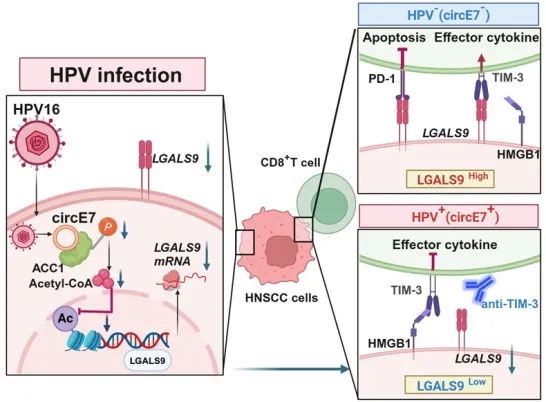
研究团队通过整合头颈部鳞状细胞癌(HNSCC)患者临床样本,结合细胞和动物实验,发现circE7可下调LGALS9基因(编码Galectin-9蛋白)的表达,抑制杀伤性T细胞功能,进而促进肿瘤免疫逃逸。进一步分析发现,Galectin-9通过竞争性结合T细胞表面的TIM-3,促进CD8+ T细胞分泌杀伤性细胞因子,Galectin-9还可以结合T细胞表面PD-1抑制T细胞凋亡;circE7下调Galectin-9,导致CD8+T功能和活性受到抑制;circE7下调LGALS9表达的具体分子机制是,circE7结合并抑制乙酰辅酶A羧化酶1(acetyl-CoA carboxylase 1,ACC1)的磷酸化和激活,降低细胞内乙酰辅酶A水平,导致LGALS9基因的启动子区域H3K27乙酰化水平降低,通过表观遗传调控抑制LGALS9的表达。
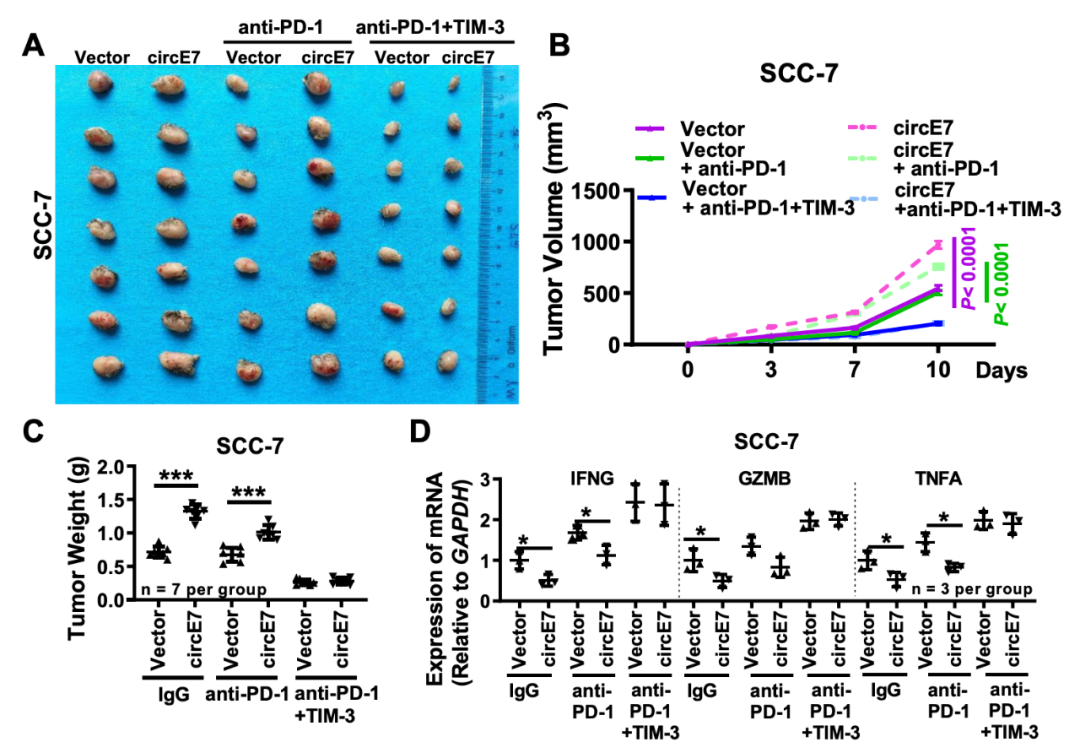
最后,研究团队通过体内外模型证实,联合使用TIM-3与PD-1单克隆抗体能显著提高HNSCC的免疫治疗效果。
总的来说,该研究拓展了HPV在头颈鳞癌发病机制,特别是免疫逃逸分子机制的理解,并为头颈鳞癌的免疫治疗提供了新的靶点和潜在治疗方案。
曾朝阳、熊炜、龚朝建为论文共同通讯作者,博士后葛军尚、博士生孟依、硕士生郭佳玥为并列第一作者。该研究得到了国家自然科学基金区域创新联合基金重点项目、国家自然科学基金面上项目及湖南省重点研发计划项目等资助。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


