TN:科学家首次发现,Tau蛋白会促进自身通过外囊泡扩散,并找到可抑制这一过程的药物
来源:奇点糕 2023-12-08 10:05
在走向临床试验之前,仍需要对PDDC的耐受性进行进一步评估。不过,根据当前的数据, PDDC或可作为一种有前途的治疗新策略,通过减少过度磷酸化Tau的扩散来减缓AD的进展。
近日,美国约翰霍普金斯大学医学院的Norman J. Haughey、Dimitrios Kapogiannis和Barbara S. Slusher等人,在Translational Neurodegeneration期刊上发表最新研究。他们发现,长期给药一种抑制Tau蛋白扩散的小分子口服抑制剂,能够有效减缓阿尔茨海默病(AD)小鼠的Tau蛋白传播,并改善神经炎症等其它AD病理。

论文首页截图
中性鞘磷脂酶2(nSMase2)是协助细胞制备细胞外囊泡的关键酶。nSMase2能够将细胞膜中的鞘磷脂裂解成神经酰胺,富集的神经酰胺改变细胞膜物理特性,导致细胞外囊泡出芽。抑制nSMase2的活性,可以改变细胞的囊泡运输机制。
PDDC是由美国约翰霍普金斯大学医学院的研究人员开发的首个具有高度选择性、脑渗透性的nSMase2抑制剂口服药物。在这项研究中,Barbara S. Slusher等人利用Tau病理的AD小鼠模型(P19)探索PDDC的效果。
结果显示,AD小鼠从4个月龄起每周5天口服PDDC(约3mg/天),治疗5个月后,体重变化与常规饲料喂养的AD小鼠相近,没有引起行为异常或肝肾功能的不良影响。
在进行体外实验时,研究者们有个前所未有的发现。他们观察到,转染突变pTau蛋白(人类Tau蛋白)后,大鼠海马神经元的nSMase2活性显著增强,神经酰胺水平明显提高。
与体外实验结果一致,与野生型小鼠相比,AD小鼠的海马神经元nSMase2活性更高、11种神经酰胺水平提高。但是经PDDC治疗的AD小鼠,nSMase2活性和神经酰胺水平的异常升高完全正常化,与野生型小鼠相近。
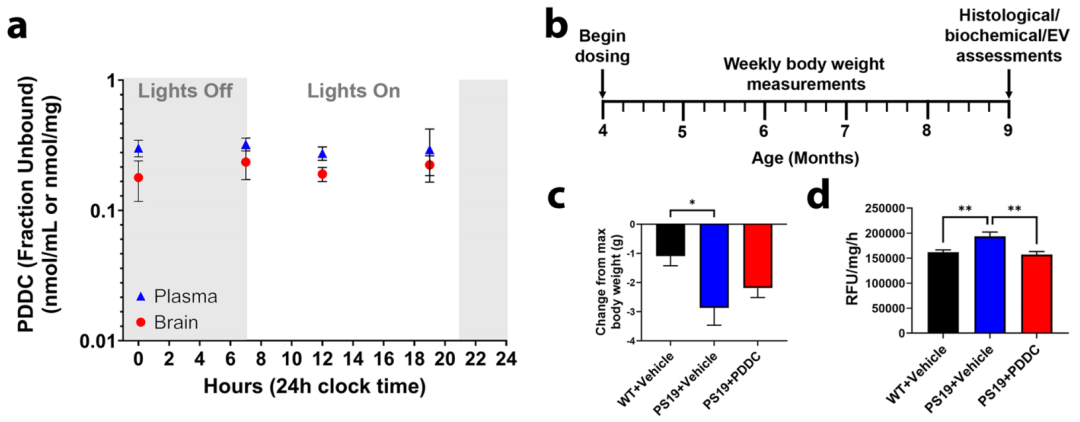
PDDC治疗对体重和nSMase2活性的影响
进一步研究表明,PDDC治疗不会改善AD小鼠的Tau蛋白过度磷酸化,但可以降低总Tau蛋白水平(P=0.0041)。另外检测到,PDDC能够有效抑制神经元和小胶质细胞产生细胞外囊泡,降低血液和大脑中的细胞外囊泡数量。
研究者们还利用Tau蛋白快速传播的小鼠模型证明,PDDC治疗显著减少Tau蛋白到大脑对侧部分的传播。
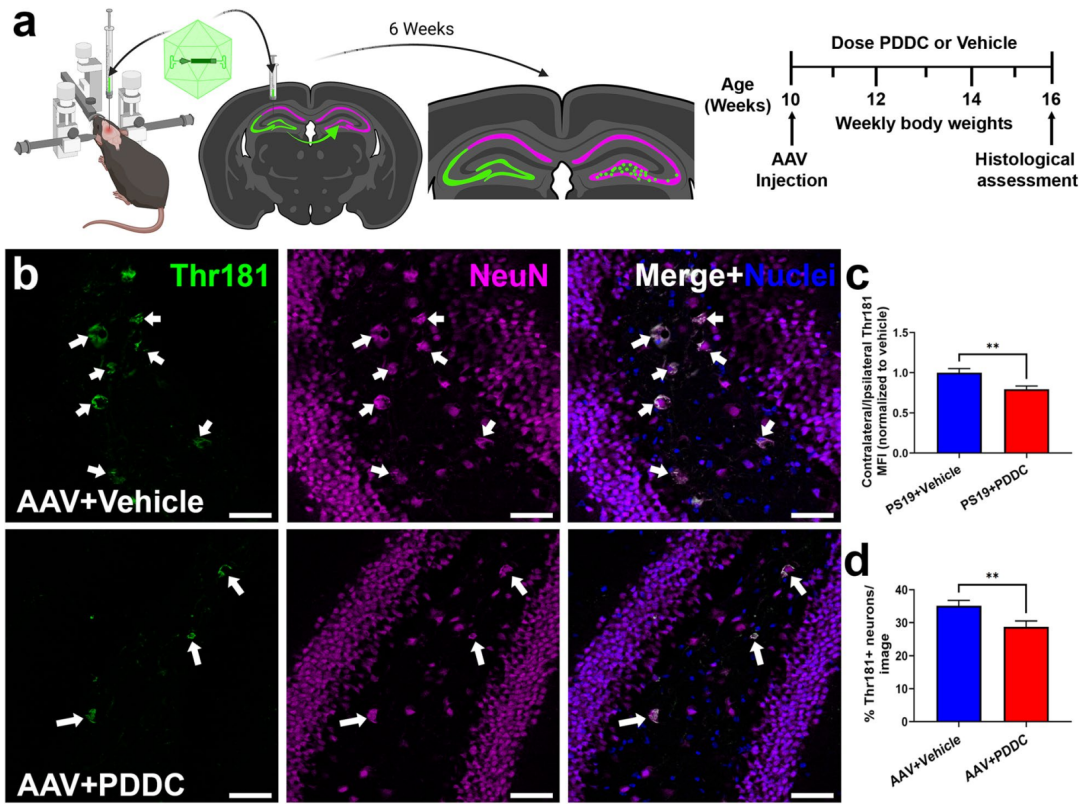
PDDC治疗减少Tau蛋白扩散
PDDC的作用不局限于抑制Tau蛋白扩散。AD小鼠实验结果表明,PDDC治疗对保护神经结构和功能具有积极作用,可以减少海马损伤和突触损失。同时,PDDC治疗减少AD小鼠大脑中小胶质细胞和星形胶质细胞的活化,这对于减轻AD的炎症相关病理具有潜在帮助。
总而言之,这项研究首次发现,异常Tau蛋白可以提高海马神经元的nSMase2活性和神经酰胺水平。当异常Tau蛋白表达增加时,nSMase2活性增强、神经酰胺水平升高,促进细胞外囊泡的形成以及异常Tau蛋白的释放和传播,导致更多健康的神经元遭受异常Tau蛋白的迫害。
约翰霍普金斯大学医学院的研究人员开发的口服药物PDDC,可以破解异常Tau蛋白的这一计谋。通过抑制nSMase2活性,PDDC不仅可以直接减少Tau的传播,还可以缓解其它AD病理,比如减少神经炎症和突触损失,使大脑神经酰胺水平正常化。
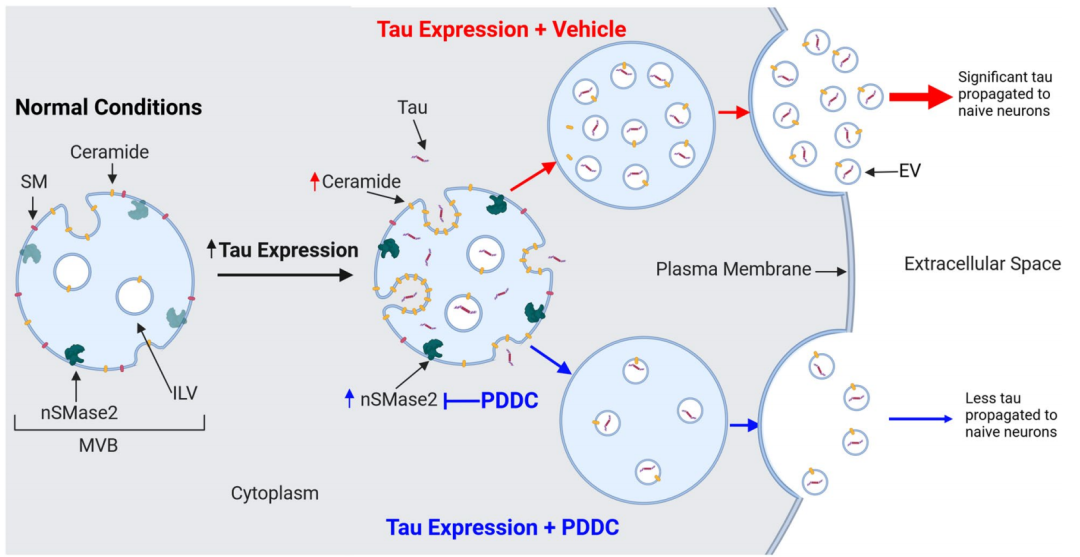
机制图
在走向临床试验之前,仍需要对PDDC的耐受性进行进一步评估。不过,根据当前的数据, PDDC或可作为一种有前途的治疗新策略,通过减少过度磷酸化Tau的扩散来减缓AD的进展。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


