Nature 子刊:mTORC1-4EBP1/2轴触发了葡萄糖饥饿期间生存所必需的代谢开关
来源:生物谷原创 2024-06-18 13:41
该研究揭示了MTORC1通过4EBP1/2介导的脂肪酸代谢翻译重编程调节葡萄糖饥饿下的细胞存活。
葡萄糖是最重要的营养物质之一,生物体内葡萄糖的缺乏是一种重要的生理应激。的确,缺糖迫使细胞进化分子机制来调节新陈代谢和维持生存。这些机制对于实体瘤内的细胞尤其关键,因为这些组织由于血管形成缺陷而遭受葡萄糖剥夺。对葡萄糖饥饿的代谢适应是通过阻断合成代谢过程,同时激活分解代谢过程来实现的,这些过程共同保存细胞能量和氧化还原平衡。
这些反应是由高度保守的能量传感器和信号中枢协调的,如amp激活的蛋白激酶(AMPK)5,6和雷帕霉素复合物1的机制靶标(mTORC1),两者都是决定葡萄糖剥夺条件下细胞命运的必要条件。
AMPK在直接感觉到AMP/ATP和ADP/ATP比值增加以及果糖-1,6-二磷酸消耗后被葡萄糖剥夺激活。激活后,AMPK将几种定义明确的底物磷酸化,以增加细胞能量生产和降低能量消耗,以及重新编程新陈代谢。
具体地说,在葡萄糖饥饿期间,AMPK磷酸化并抑制脂肪酸合成途径的限速酶--乙酰辅酶A羧基酶1(ACC1),以减少脂肪酸的合成。由于这一代谢过程是细胞中消耗NADPH最多的过程,AMPK介导的ACC1阻断能够维持NADPH的动态平衡,抑制活性氧(ROS),并促进细胞在缺糖条件下的存活。

图片来源:https://doi.org/10.1038/s41467-024-48386-y
近日,来自内盖夫本-古里安大学的研究者们在nature communications 杂志上发表了题为“mTORC1 regulates cell survival under glucose starvation through 4EBP1/2-mediated translational reprogramming of fatty acid metabolism”的文章,该研究揭示了MTORC1通过4EBP1/2介导的脂肪酸代谢翻译重编程调节葡萄糖饥饿下的细胞存活。
能量压力迫使细胞进化出适应机制来调整其新陈代谢。抑制mTOR激酶复合体1(MTORC1)对于葡萄糖饥饿时的细胞生存是必不可少的。在葡萄糖饥饿期间,mTORC1是如何控制细胞活性的还不是很清楚。
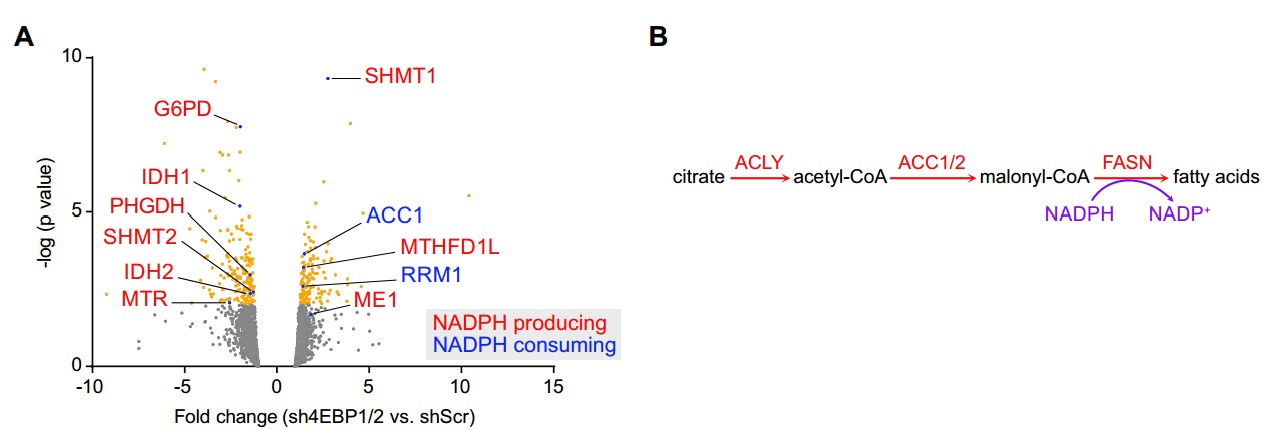
4EBP1/2调控葡萄糖饥饿时的脂肪酸合成活性,以维持氧化还原平衡,保护细胞
图片来源:https://doi.org/10.1038/s41467-024-48386-y
在本研究中,研究者证明了mTORC1效应物真核启动因子4E结合蛋白1/2(4EBP1/2)为葡萄糖饥饿下的哺乳动物细胞和萌芽酵母提供了保护。在机制上,4EBP1/2通过翻译抑制乙酰辅酶A羧基酶1(ACC1)来阻止NADPH消耗脂肪酸的合成,从而促进NADPH的动态平衡,从而减轻氧化应激。
这与癌症有重要的关系,因为癌基因转化细胞和胶质瘤细胞利用4EBP1/2调节ACC1的表达和氧化还原平衡来对抗能量应激,从而支持体外和体内的转化和致瘤性。临床上,EIF4EBP1的高表达与几种癌症类型的预后不良有关。本研究数据显示,mTORC1-4EBP1/2轴触发了葡萄糖饥饿期间生存所必需的代谢开关,转化细胞和肿瘤细胞利用了这一开关。
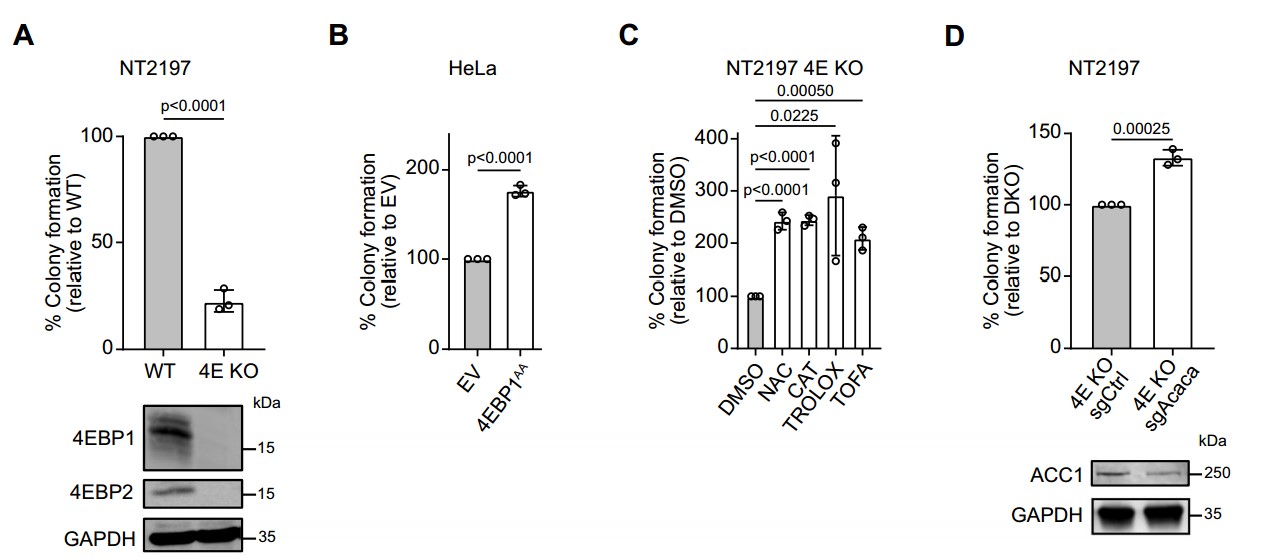
4EBP1支持体外和体内的致癌转化
图片来源:https://doi.org/10.1038/s41467-024-48386-y
总之,本研究发现表明,4EBP1可能是代谢挑战肿瘤类型的治疗靶点,同时值得谨慎使用mTOR抑制剂治疗这些癌症。此外,本研究发现显示,mTORC1-4EBP1/2轴在葡萄糖饥饿期间抑制脂肪酸的合成,并且这一特殊功能被肿瘤细胞利用以获得其自身的选择优势。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


