Molecular Therapy: Nucleic Acids非编码RNA:DGUOK-AS1通过调节miR-204-5p/IL-11轴发挥促癌作用
来源:本站原创 2021-12-31 11:29
乳腺癌是女性致死率最高的恶性肿瘤之一,然而,乳腺癌进展和转移的潜在分子机制尚不清楚。
乳腺癌是女性致死率最高的恶性肿瘤之一,然而,乳腺癌进展和转移的潜在分子机制尚不清楚。大量研究证实,长非编码RNA在乳腺癌中异常表达,在细胞增殖和转移中发挥重要作用。在这项研究中,作者评估了DGUOK-AS1在乳腺癌进展和转移中的功能作用和详细机制。
图片来源: https://doi.org/10.1016/j.omtn.2021.10.018
尽管目前在诊断和治疗方面有所创新,但乳腺癌的预后仍然不令人满意。因此,需要更多的研究来进一步探讨乳腺癌进展的机制,提供新的治疗靶点。近年来,多项研究证实lncRNAs在人类生理和病理生理过程中发挥着重要作用。此外,lncrna的异常调节与乳腺癌的发生、进展和耐药密切相关。
LncRNA HUMT过表达与乳腺癌患者预后不良有关,可能通过激活FOXK1转录促进淋巴结转移,进而调节VEGFC的表达。LncRNA HOST2在TNBC细胞和组织中表达上调,并通过诱骗let-7b促进STAT3介导的TNBC细胞增殖和迁移能力。既往研究表明DGUOK-AS1在乳腺癌组织中表达上调,并与乳腺癌患者的不良预后相关,提示DGUOK-AS可能是一种有前途的预后预测指标和治疗靶点。
此外,已有研究报道DGUOK-AS1可能通过调节miR-653-5p/EMSY通路促进宫颈癌细胞增殖。然而,DGUOK-AS1在乳腺癌中的作用尚未完全阐明。在本研究中,作者通过体外和活体实验研究了DGUOK-AS1的功能和分子机制。
作为非编码RNA,lncRNAs主要通过调控癌基因或抑癌基因的表达,包括染色质重塑调控、转录或转录后调控、翻译调控等对肿瘤细胞发挥作用。其中,焦点主要集中在CELNA机制上。例如,lncRNA UCA1充当miR-182-5p的miRNA海绵,最终促进肾癌的恶性进展。LncRNA CDKN2BAS与肝细胞car- cinoma患者预后不良相关,并通过调节miR-153-5p/ARHGAP18轴促进肿瘤转移。
在本研究中,作者发现DGUOK-AS主要定位于细胞质中,并通过对miR-204-5P的海绵作用发挥其致癌作用。先前的研究报道miR-204-5p在多种癌症中发挥肿瘤抑制作用,包括头颈部鳞状细胞癌、胃癌和乳腺癌。虽然miR-204-5p的异常表达在细胞增殖、迁移和侵袭中具有潜在的重要作用,但DGUOK-AS1是否通过与miR-204-5p的直接相互作用影响乳腺癌的进展仍有待探讨。
荧光素酶报告实验和RIP实验结果表明,DGUOK-AS通过与miR-204-5p结合,作为miRNA海绵发挥调节作用。此外,功能分析进一步证明miR-204-5p过表达减轻了DGUOK-AS1过表达对细胞增殖、迁移和侵袭的促进作用。
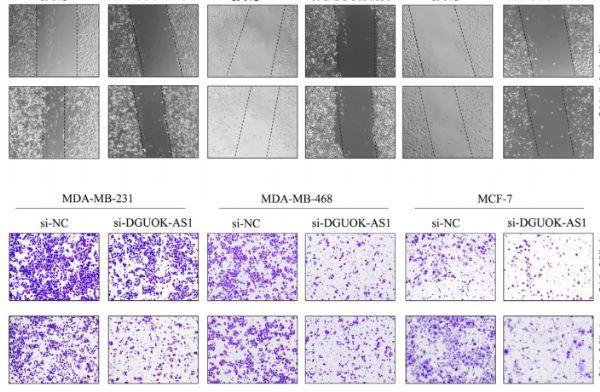
DGUOK-AS1基因敲除抑制乳腺癌细胞的迁移和侵袭
图片来源: https://doi.org/10.1016/j.omtn.2021.10.018
综上所述,作者的研究表明DGUOK-AS1作为癌基因通过调节miR-204-5p/IL-11轴促进乳腺癌细胞的增殖、迁移和侵袭。这些结果表明,DGUOK-AS1是乳腺癌进展的关键分子,可能成为一种新的生物标志物和潜在的治疗靶点。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。