Adv Sci:黄锦海/周行涛团队使用AAV介导的CRISPR基因编辑治疗角膜新生血管
来源:生物世界 2024-04-15 10:20
该研究使用CRISPR-Cas9基因编辑系统敲除VEGFA基因来治疗小鼠缝线诱导的角膜新生血管。据悉,这是第一项利用AAV介导的CRISPR-Cas9基因编辑系统在体内治疗角膜新生血管的研究。
近日,复旦大学附属眼耳鼻喉科医院黄锦海/周行涛团队与暨南大学附属深圳眼科医院雷和田教授团队、温州医科大学附属眼视光医院王勤美教授团队合作,在 Advanced Science 期刊发表了题为:Genome Editing VEGFA Prevents Corneal Neovascularization In Vivo(体内基因组编辑VEGFA阻止角膜新生血管生成)的研究论文。
该研究首次利用腺相关病毒(AAV)介导的CRISPR-Cas9基因编辑VEGFA在体内治疗角膜新生血,为利用CRISPR基因编辑策略治疗此类眼部疾病奠定了基础。

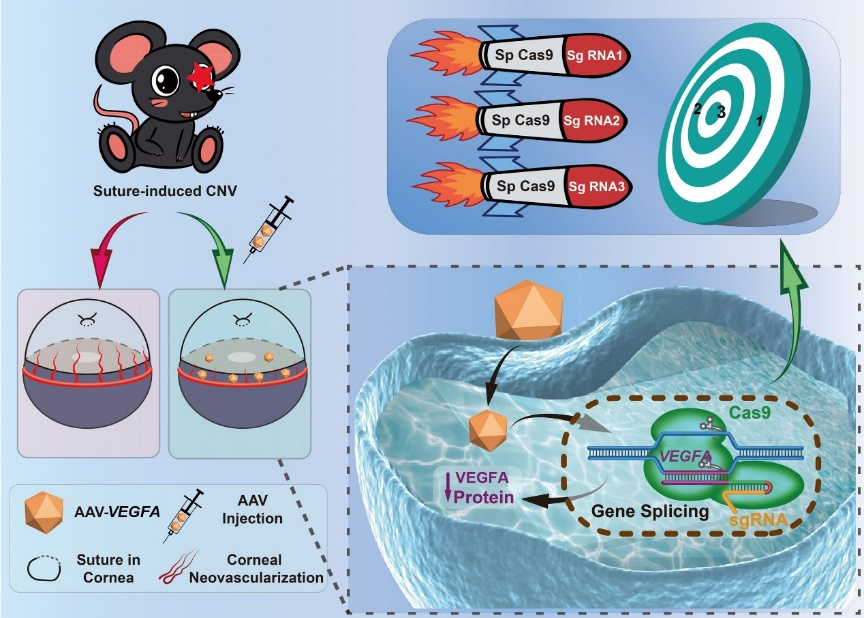
CRISPR-Cas9基因编辑技术为治疗人类疾病提供了新机会,美国FDA以批准了一款CRISPR-Cas9基因编辑疗法用于治疗β-地中海贫血和镰状细胞病。
在这项研究中,研究团队探索了在小鼠中使用CRISPR-Cas9基因编辑技术来抑制VEGFA的表达,从而抑制小鼠角膜新生血管的形成。
该研究显示,使用CRISPR-Cas9基因编辑系统靶向敲除VEGFA,可以在体外抑制人脐静脉内皮细胞(HUVEC)的增殖、迁移和血管形成。更重要的是,结膜下注射双AAV病毒载体递送的SpCas9/sgRNA-VEGFA系统,可以阻断角膜缝线诱导的VEGFA、CD31和α-平滑肌肌动蛋白的表达,以及小鼠角膜新生血管的形成。这项研究首次为通过基因编辑方法治疗角膜新生血管奠定了坚实基础。
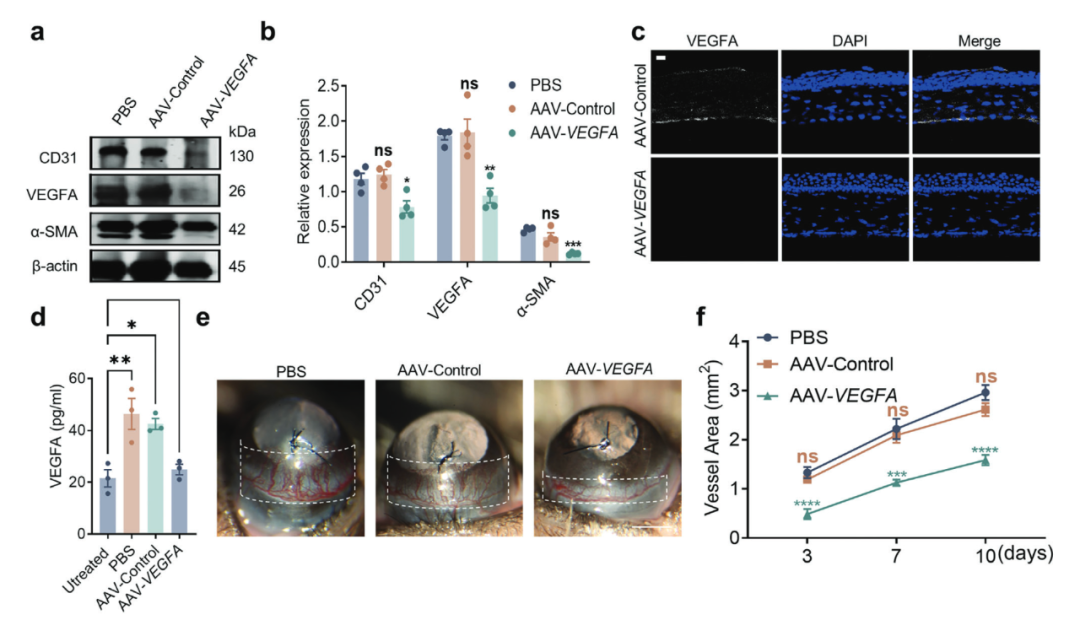
该研究进一步表明,通过CRISPR-Cas9基因编辑来抑制眼组织中的VEGFA表达,不会影响视网膜功能,且并未影响身体的各个器官,这些结果证实了结膜下注射靶向VEGFA的双AAV病毒载体递送的CRISPR-Cas9系统后没有可检测到的毒性作用。
总的来说,该研究使用CRISPR-Cas9基因编辑系统敲除VEGFA基因来治疗小鼠缝线诱导的角膜新生血管。据悉,这是第一项利用AAV介导的CRISPR-Cas9基因编辑系统在体内治疗角膜新生血管的研究,为利用CRISPR基因编辑策略治疗此类眼部疾病奠定了基础。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


