《神经病学》:阿尔茨海默病治疗新时代已至,但临床准备好迎接它了吗?
来源:奇点糕 2023-08-02 14:29
AD治疗已经进入了一个拥有疾病修饰疗法的新时代,不断完善实践中的不足,不断创新,是确保AD患者接受治疗后获得最佳临床结果的必经之路。
自2021年,抗β-淀粉样蛋白(Aβ)单抗aducanumab获得FDA加速审批上市,正式推开了阿尔茨海默病(AD)抗Aβ单抗治疗的大门。不久前,另外两款单抗lecanemab和donanemab又传来了好消息,一个正式获得了FDA批准,一个III期临床试验阳性结果登顶JAMA,迎来了一波小爆发。难道,抗Aβ单抗疗法真的是AD治疗的“天降紫微星”?
不过话说回来,抗Aβ单抗药物有着完全不同于传统AD药物的治疗风险和治疗负担,它们在真实世界中的临床应用和相应的不良事件管理对现有疾病管理流程和基础设施来说产生了很大挑战。
为此,美国神经病学学会携多个医学机构的神经病学专家撰写了一篇综述文章,为广大神经病学临床医生提供了关于新兴的抗Aβ单抗的介绍和治疗决策的实用指导。文章发表于美国神经病学学会官方期刊《神经病学》。

抗Aβ单抗作为AD治疗药物的表现
从临床角度来看,AD包含一系列的综合征表现,而从生物学角度来看,AD是由Aβ斑块和神经原纤维tau沉积定义的。纵向衰老研究和遗传学研究均显示,异常脑淀粉样病变是AD级联中的早期事件,奠定了Aβ靶向治疗的基础。
第一款aducanumab尽管获得了FDA的加速批准,但存在许多争议,尤其是两项设计相同的III期临床试验EMERGE和ENGAGE产生了相互矛盾的结果,提前终止,尽管未能达到主要终点,不过值得注意的是,与安慰剂组相比,高剂量试验组参与者的临床痴呆评定量表(CDR-SB)评分有一定的下降。
获得FDA正式批准的lecanemab的III期临床试验CLARITY-AD则向前迈了一步,18个月的治疗使得患早期AD的参与者由CDR-SB评估的认知和功能下降有显著减缓,相当于疾病进展延缓4-5个月。
Lecanemab治疗除注射反应外的最常见不良事件为淀粉样相关成像异常(ARIA),总发生率为21.3%,但其中近80%是无症状的,低于aducanumab的III期临床试验中最高剂量组的41%。
由此,抗Aβ单抗药物确实可以减缓早期AD的疾病发展,但风险超出目前的AD治疗药物。
患者选择与共同决策
目前,临床试验的结果仅支持抗Aβ单抗用于治疗轻度认知障碍(MCI)或AD相关轻度痴呆症,患者想要接受治疗需进行简易精神状态检查(MMSE)等量表的评估,对治疗效果的评估以来CDR-SB或神经心理评估,可能需要额外的培训或医疗资源,无法适用于所有医疗环境。因此,临床医生需要考虑如何系统性识别哪些患者最有可能从治疗中获益。
在启动治疗前,也需要存在异常脑淀粉样病变的证据,可以通过淀粉样蛋白PET或脑脊液生物标志物来确定,前者对设备、试剂和专业知识要求较高,且未被保险覆盖,后者更容易获取,但需有创操作,且在临床中的应用尚未取得共识。
除此之外,治疗前评估还应包括不良事件风险评估,例如脑MRI确定脑血管疾病和其他相关结构异常的程度,微出血和浅表铁质沉着与ARIA高风险有关,脑大出血、大面积缺血性卒中、多腔隙卒中病史,或MRI显示严重小血管缺血性疾病均与不良事件风险升高有关,在CLARITY-AD试验中,相关参与者被排除。
类似的考虑点还包括合并用药和基因型,抗凝药物不可与抗Aβ单抗联用,CLARITY-AD试验中,1例参与者因急性缺血性卒中接受组织纤溶酶原激活剂后死于广泛多灶性脑出血,开放标签阶段的2例死亡中也至少有1例涉及抗凝药物暴露。APOEε4也与高ARIA发生率有关,尤其是APOEε4纯合子。其他潜在影响因素包括癫痫、癌症、血液或免疫合并症等。
在治疗过程中,临床医生、患者和照护人员之间需要有共同的、一致的治疗获益、风险和照护目标,因为抗Aβ单抗疗法仍在探索阶段,存在一定不确定性,以及相对较高的金钱和时间成本,合理的、一致的目标有助于疾病管理。
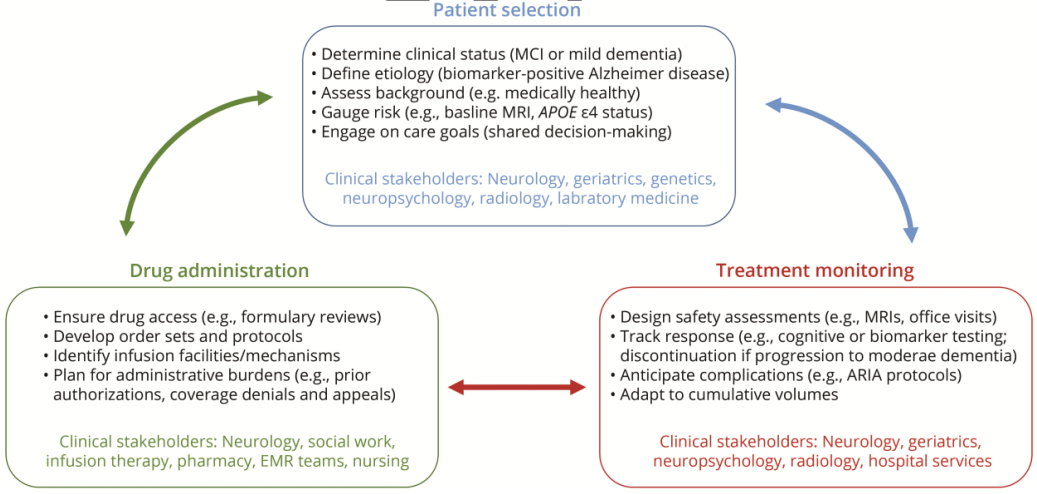
治疗管理和临床实践基础设施
目前的AD照护框架包括相对不频繁的办公室随访和先进的诊断测试,以lecanemab为例,lecanemab需要每2周输注一次,需要大约1小时,除了筛选患者和安排定期输注外,临床医生还需要为ARIA和其他潜在不良事件的发生做好应对准备,例如出现症状时的紧急评估和多学科处置。
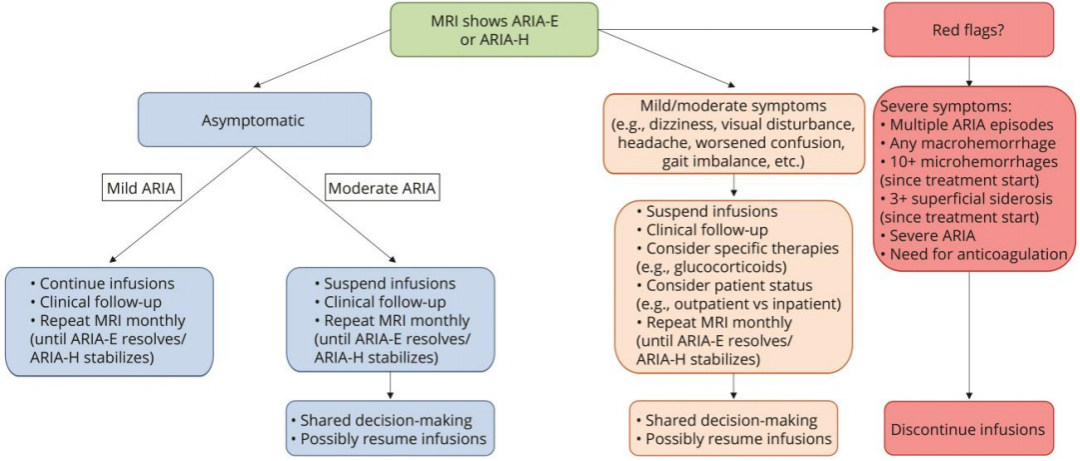
ARIA的常见症状包括头晕、头痛、视力障碍和精神错乱增加,但大多数经放射学检测发现的ARIA是无症状的,因此,如果缺少充分监测,可能存在恶化风险,FDA规定,在第5次、第7次和14次lecanemab输注前,应进行MRI,这与CLARITY-AD试验中,ARIA在治疗的前4个月内最为常见的结果有关,ARIA风险较高者还需要额外的MRI。
对于有症状的或MRI显示严重的ARIA患者,需要考虑类固醇治疗和可能的合并症常规治疗。这意味着,抗Aβ单抗治疗的提供方需要确保有足够的普通和/或重症监护病房、MRI和脑电图设备,以及其它配套医疗资源。
对于大多数社区人口来说,接受社区医院非专科医生的初步评估是更实际的,对非专科医生的概念和技能培训可以帮助他们成为“社区前线”,进一步,识别高风险和/或复杂性患者的分诊也可能对专科医生预约,以及医生和患者体验产生重要影响。
随着治疗应用的扩大,可以预期的是,需要为患者和照护人员提供疾病/治疗信息的需求会增加,除了社区医生的培训,还可以通过开发患者教育网站,提供对常见问题的模板回答。
抗Aβ单抗的未来进展
目前,抗Aβ单抗的临床试验入组的均为散发性、有典型临床表现的AD患者,未来,如何扩展到非典型临床表现的患者中将成为新的挑战。
药物特异性特征可能成为另一个挑战,现有的抗Aβ单抗靶向Aβ级联中的多个导致斑块沉积的步骤,但微妙的药物机制和药代动力学差异可能影响疗效、不良反应和最佳使用群体,这一点在其他疾病中也有观察到,例如多发性硬化症的新一代治疗方法,而且Aβ斑块减少的幅度和速度也可能会对下游病理生理学变化的调节产生不同的影响,继而影响临床治疗结局,从而影响患者的在临床试验中的候选资格和药物选择。
与安慰剂相比,几种抗Aβ单抗治疗都与较低的脑容量有关,这还需要进一步的研究来确定其中的机制和长期影响。
此外,对于抗Aβ单抗治疗的最佳持续时间还没有达成共识,需要确定一个合适的治疗结束时机,至一段固定时间内发展为中度痴呆或达到淀粉样蛋白PET阴性,对于患者的生理和经济负担来说是完全不同的。
类似的,还有启动治疗的时机,在认知未受损时是否能够延缓AD发生和进展?以及,如何更加合理地设置研究终点,既能够达到临床试验的合理预期,又能够被患者和照护者认为是有意义的改变,在AD早期阶段,CDR-SB量表中0.5分的差异就可以体现出日常生活能力的实质性变化,但在长期治疗过程中,评分的逐渐下降对于患者和照护者来说可能并不明显,是一种非线性获益。
除此之外,扩大临床试验和真实世界研究中接受治疗的患者的种族/民族多样性,以确保研究结果具有代表性,增加具有行为神经病学和神经精神病学专业知识的专科医生的数量也很重要。
总的来说,AD治疗已经进入了一个拥有疾病修饰疗法的新时代,不断完善实践中的不足,不断创新,是确保AD患者接受治疗后获得最佳临床结果的必经之路。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


