《自然·生物技术》:植入脂肪,“饿死”肿瘤!科学家发明“脂肪操纵疗法”,改造出可竞争代谢营养物抑癌的脂肪类器官
来源:奇点糕 2025-02-06 13:54
将脂肪类器官植入到四类不同肿瘤模型小鼠的肿瘤旁,就使肿瘤体积相比对照组缩小了50%以上,且癌细胞不仅增殖速率下降,凋亡速率也显著上升,同时肿瘤微血管密度明显下降。

看到今天《自然·生物技术》发表的这篇最新研究论文,奇点糕第一时间想到的,还真就是“驱虎吞狼”四个字:把癌症和脂肪比作虎狼,不是很合适吗?而加州大学旧金山分校(UCSF)研究者们提出的最新抗癌策略——“脂肪操纵疗法”(AMT),就是通过基因编辑改造肥胖元凶白色脂肪,让它们变成可植入患者体内、通过竞争营养物质抑癌的有效疗法。
具体来说,这套疗法首先从患者体内抽取白色脂肪,再用CRISPR技术上调UCP1等关键转录因子/酶表达,即可使白色脂肪转变到与人体内有益健康的棕色脂肪类似的状态(“棕色脂肪样组织”),再将它们植入到患者体内,在肿瘤旁甚至是在远处时,经改造的脂肪都能从癌细胞手中抢走葡萄糖和脂肪酸两大关键代谢物质,显著抑制肿瘤生长。而且,这套策略也可稍加调整后用于依赖其它营养和代谢物质的肿瘤,潜在的治疗应用场景或将十分广泛[1]。

为了给不断分裂增殖和侵袭供给能量,癌细胞在争抢营养物质方面有多么不择手段凶残狡诈,相信也不用奇点糕多介绍了,但这世上往往强中更有强中手,2022年瑞典卡罗林斯卡学院发表在《自然》上的研究成果就揭示,以冷暴露方式激活棕色脂肪,可有效抑制癌细胞摄取葡萄糖并经糖酵解将其代谢的能力,带来抑癌效果,且UCP1正是其中的关键调控因子[2]。
但在临床治疗时,癌症患者的身体恐怕承受不住冷暴露,照搬这种方式复现激活棕色脂肪的效果显然不现实,所以UCSF团队才把思考转到了“白色脂肪棕色化”[3]的方向,实验的第一步就用CRISPR上调人体白色脂肪细胞的UCP1及PPARGC1A、PRDM16等关键转录因子/酶表达水平,使它们成功棕色化,具有更强的摄取葡萄糖/脂肪酸能力。
接下来的细胞共培养实验证实,只要上调UCP1、PPARGC1A、PRDM16三个关键基因之一,白色脂肪细胞就可在共培养时将癌细胞增殖速率降至原本的1/5-1/3,上调UCP1收效最好;各项检验也证实,共培养使癌细胞糖酵解和脂肪酸氧化速率显著下降。

经CRISPR改造“棕色化”的脂肪细胞,可在共培养实验中有效抑癌
不过研究者们认为,相比单纯植入CRISPR改造后的白色脂肪细胞,改造出“脂肪类器官”(adipose organoid)可能更有优势,接下来的小鼠实验就改用脂肪类器官(仅上调UCP1表达)进行:将脂肪类器官植入到四类不同肿瘤模型小鼠的肿瘤旁,就使肿瘤体积相比对照组缩小了50%以上,且癌细胞不仅增殖速率下降,凋亡速率也显著上升,同时肿瘤微血管密度明显下降,意味着癌细胞经微血管远处转移也将更困难。
而与此前的细胞共培养试验类似,脂肪类器官也是通过抢走葡萄糖和脂肪酸实现抑癌,向小鼠喂食高脂饮食或高浓度糖水则可抵消抑癌效果。对乳腺癌模型小鼠进行的实验还显示,脂肪类器官被植入到距离肿瘤较远的部位也可有效抑癌,即其激活的抑癌作用是系统性的;从切除乳腺中分离的脂肪细胞,经改造后也可让AMT疗法实现“自体移植”,这对降低潜在的排异风险很有帮助。
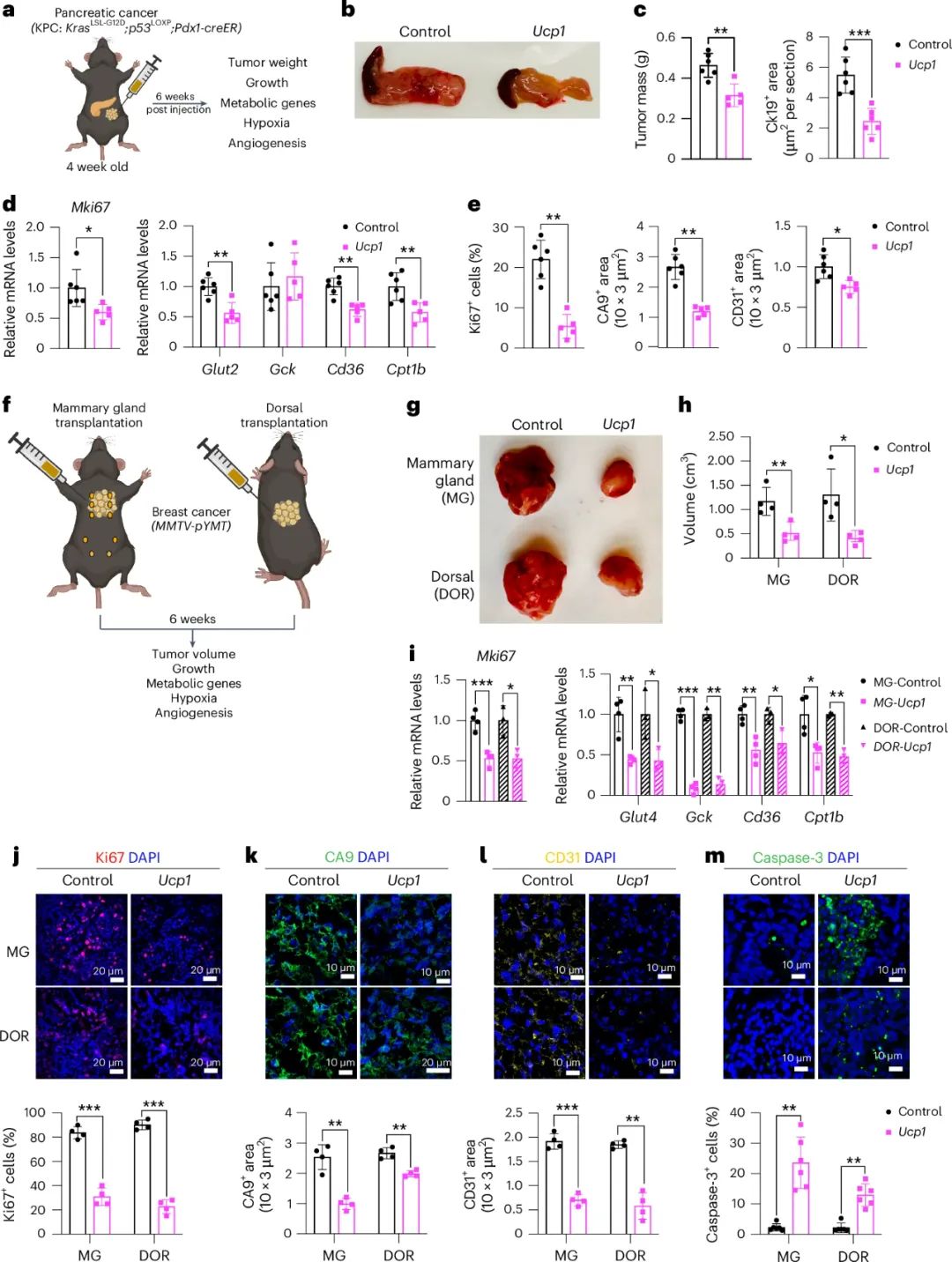
即使在远离肿瘤的部位植入脂肪类器官,也有明确抑癌作用
说到这里,“植入脂肪抑癌”思维的天马行空和疗法的使用潜力就已经很让人惊喜了,但研究者们还找到了AMT疗法更多可能得应用场景,首先是对携带BRCA1/2突变的乳腺癌发病高危人群,AMT疗法也在实验中被证实可减少癌前细胞数量,有望用于预防性治疗;其次,将CRISPR上调的关键基因换为尿苷代谢酶UPP1,AMT疗法就能有效抑制缺少葡萄糖时可代谢尿苷替代供能的胰腺癌生长,类似的策略当然也可以外推到更多癌症中嘛。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


