多篇文章聚焦科学家们在表观遗传学研究领域取得的新进展!
来源:本站原创 2021-08-27 16:52
近年来科学家们在表观遗传学研究领域投入了大量的精力,取得了多项重要成果,本文中,小编就对相关研究成果进行整理,分享给大家!
表观遗传学是研究基因的核苷酸序列不发生改变的情况下,基因表达了可遗传的变化的一门遗传学分支学科。近年来科学家们在表观遗传学研究领域投入了大量的精力,也取得了多项重要成果,本文中,小编就对相关研究成果进行整理,分享给大家!
表皮观遗传学代码或能重塑成体小鼠肝脏中的染色质状态。
图片来源:Zhang, C., et al. Nat Commun 12, 4110 (2021). doi:10.1038/s41467-021-24466-1
【1】Nat Commun:表观遗传学代码重塑的染色质状态或能赋予小鼠肝脏一定的再生潜能
doi:10.1038/s41467-021-24466-1
研究人员推测,对肝脏再生至关重要的基因表达的高度控制模式是由静止的肝脏细胞中的表观遗传学代码所编码的;近日,一篇发表在国际杂志Nature Communications上题为“Chromatin states shaped by an epigenetic code confer regenerative potential to the mouse liver”的研究报告中,来自纽约大学阿布扎比分校等机构的科学家们通过研究发现了一种特殊代码,其或能设置肝脏的基因组来解释肝脏惊人的再生能力。这一研究结果或能帮助阐明在机体被切除部分肝脏时,促进肝脏再生的特定基因被激活的分子机制,同时还有望帮助改善新形式再生医学疗法的发展,并帮助非再生器官在小鼠和人类机体中再生并生长。
尽管其它动物都能够再生大多数器官,但人类、小鼠和其它哺乳动物则仅能再生肝脏来应对损伤或被移除的结局;研究人员假设,驱动肝脏再生的基因或能被一种特殊的代码所控制,而这种代码还能促进其在应对损伤或切除时被激活,随后研究人员重点对表观基因组进行了相关研究,即通过对DNA进行修饰来改变基因的表达,而并非改变遗传代码本身。
利用小鼠模型进行研究,研究人员在静息的肝脏细胞中识别出了存在的表观遗传代码元件,静息的肝脏细胞并不能复制但却拥有在合适条件下增殖的能力,这些表观遗传代码元件或能激活特殊的基因进行器官再生。参与肝细胞增殖的基因在不进行再生再生的肝脏中处于沉默状态,但令研究人员惊讶的是,这些基因存在于大多数基因活跃的基因组部分;而且这些促再生的基因往往被被标记一种名为H3K27me3的特定修饰,在肝脏再生期间,H3K27me3能被从基因中剔除,从而使得基因能够进行动态表达并驱动增殖过程。
【2】Nat Commun:揭秘表观遗传修饰驱动B细胞命运的分子机理
doi:10.1038/s41467-021-22458-9
B细胞的B1和B2谱系会以不同的方式来保护机体抵御病原体的侵袭,目前研究人员并不清楚DNA CpG的甲基化组在指定上述两种B细胞命运上所扮演的重要角色;近日,一篇发表在国际杂志Nature Communications上题为“B1a and B2 cells are characterized by distinct CpG modification states at DNMT3A-maintained enhancers”的研究报告中,来自麻省总医院等机构的科学家们通过研究揭示了表观遗传学改变驱动机体B细胞命运的分子机制。
B细胞是一种负责产生抗体的机体免疫细胞,大多数的B细胞(B2细胞)都能产生抗体来对病原体或疫苗产生反应,从而产生抵御感染的免疫防御和免疫力。但名为B1细胞的一类长寿的B细胞则与寿命较短的B2细胞有着很大不同,其并不会产生抗体来对外来入侵者产生反应,而是会自发地制造抗体来执行重要的内务管理功能,比如从血液中移除诸如氧化的LDL胆固醇等废弃物。
与机体中所有细胞一样,B1和B2细胞有着相同的DNA,因此其拥有相同的起始指令;这是通过表观遗传学修饰来实现的,这种修饰能够开启或关闭基因组中阅读遗传指令的特殊区域,而同一基因组则能被用来为每一种细胞类型创建独特的指令;理解不同的表观遗传蓝图(指令的改变)是如何使得相似的细胞产生这些差异的,既是免疫学研究中一个重要的基本问题,也能够更好地帮助科学家们理解与B细胞功能失常相关的疾病。
文章中,研究人员研究了在机体发育不同阶段B1和B2细胞中存在的DNA修饰特征,旨在识别出一种表观遗传特征来确定是否细胞会转变成为B1细胞或B2细胞。医学博士Vinay Mahajan表示,通过我们的分析,我们发现,B细胞的命运是由蛋白质DNMT3A所驱动的表观遗传学修饰所决定的。而进行人类遗传研究就能将携带这些标志物的基因组区域与多种免疫介导的疾病相联系起来。
【3】Science:间歇性“休整”通过表观遗传学重塑过程恢复CAR-T细胞功能
doi:10.1126/science.aba1786
嵌合抗原受体T细胞疗法(简称 “CAR-T”)正越来越多地被应用于肿瘤患者的治疗。 CAR-T细胞疗法在血液系统癌症患者中显示出令人鼓舞的结果,但其抗癌活性可能受到CAR-T细胞功能有效性的限制。 在最近一项研究中,来自斯坦福大学医学院的Crystal L. Mackall教授课题组表征了连续活动引起的CAR-T细胞衰竭相关的表型和表观基因组变化,以及短暂休息对于恢复其功能的有益作用。作者测试了不同类型的“间歇性休息”处理,例如使用药物dasatinib暂时抑制T细胞活性,这有助于防止CAR-T细胞衰竭并能够有效改善小鼠模型中的CAR-T细胞抗肿瘤活性。相关结果发表在最近的Science杂志上。
接受嵌合抗原受体(CAR)-T细胞治疗的B细胞恶性肿瘤的患者中,有50%以上仍然会出现癌症的进一步发展,并且该疗法尚未显示出对实体瘤的稳定效果。 CAR-T细胞的功效通常受到T细胞衰竭的限制,其转录和表观遗传学方面的改变会驱动免疫抑制蛋白的过表达并降低T细胞的功能。目前针对T细胞衰竭的治疗方法,包括免疫检查点抑制剂,并未影响相关的表观遗传学变化趋势。
先前研究已经证明,认为提高CAR信号活性可以诱导和维持人T细胞的功能,因此作者假设抑制CAR信号或强制性“休整”可以预防甚至可能逆转CAR-T细胞群体的衰竭。dasatinib(一种临床上使用的酪氨酸激酶抑制剂,可以可逆性地抑制CAR信号下游激酶活性)来抑制CAR-T细胞活性。基于上述结果,作者希望能够对CAR-T细胞衰竭前后的表型,功能性,转录组和表观遗传学标等进行全面分析,以了解“间歇性休整”对CAR-T细胞功能的影响。
【4】Nature子刊深度解析!科学家发现或会促进机体终生压力易感性的表观遗传学机制!
doi:10.1038/s41593-021-00814-8
近日,一篇刊登在国际杂志Nature Neuroscience上题为“Long-term behavioral and cell-type-specific molecular effects of early life stress are mediated by H3K79me2 dynamics in medium spiny neurons”的研究报告中,来自西奈山医院等机构的科学家们通过研究发现,大脑奖惩回路中主要细胞类型所发生的表观遗传学修饰或能控制生命早期的机体压力如何增加成年后机体对额外压力的易感性;研究人员报告指出,一种负责这种修饰的酶类小分子抑制剂目前正在作为一种抗癌药物进行研发,其或有望逆转动物模型对终生压力易感性水平的增加。
研究者Hope Kronman博士表示,长期以来我们一直都知道,整个生命阶段压力的暴露或能控制机体对后续压力的终生易感性,这篇研究报告中我们发现了一种关键的分子机制,其能介导机体对压力的持久效应,基于本研究,研究人员发现了一种易于进行操作的生物学靶点,其或有望帮助治疗早期生活压力所诱导的机体易感性,这或为科学家们开发新型疗法并寻找新型药理学靶点来控制压力相关的抑郁症行为提供了新的线索和思路。
终生的压力史是人类已知的最强的抑郁症风险因素,此前研究结果表明,早期的生活压力或将成年人抑郁症的风险增加三倍,而这取决于时间、强度和具体的特征;众所周知,早年间的压力会增加日后机体对压力的行为易感性的可能性,并会对大脑奖惩系统中的主要组成部分—伏隔核(nucleus accumbens)产生重要的影响。这篇文章中,研究人员重点对细胞内的表观遗传修饰进行研究,这些表观遗传学修饰是基因活性的化学改变,但并非是由我们所遗传的DNA代码所触发的,而是由调节机体的遗传物质在何时、何地以及在何种程度上被激活的分子所诱发的。研究人员识别出了一种此前未知的表观遗传学机制,其能介导机体对早期压力的长效效应,即伏隔核中名为H3K79me2 (组蛋白H3的79位赖氨酸的去甲基化,demethylation of Lysine 79 of Histone H3)的机制;早年间的压力会选择性地在伏隔核中D2型多刺神经元中诱导这一机制的发生,从而就会重编程细胞来增加成年时机体对二次压力的易感性。
图片来源:Molecular Cell , 2021, doi:10.1016/j.molcel.2021.01.038。
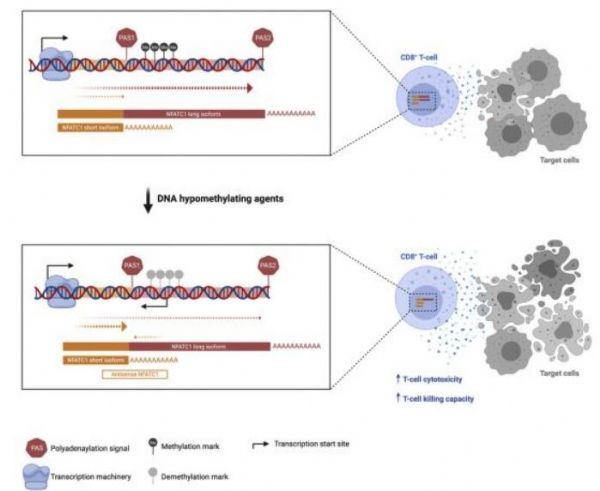
【5】Cell子刊:表观遗传学疗法可以将杀伤性T细胞变成杀死癌细胞的高手
doi:10.1016/j.molcel.2021.01.038
在一项新的研究中,来自加拿大大学医疗网络玛嘉烈公主癌症中心和多伦多大学的研究人员通过开展一系列优雅的实验,构建出特定白细胞的“超级士兵”来提高抗肿瘤反应。具体而言,他们描述了一种修饰DNA的表观遗传学疗法,可以通过增强杀伤性T细胞杀死癌细胞的能力,将它们转化为“超级士兵”。相关研究结果于2021年2月19日在线发表在Molecular Cell期刊上,论文标题为“DNA hypomethylating agents increase activation and cytolytic activity of CD8+ T cells”。
他们的发现可能会增强免疫疗法,即一种目前对少数癌症患者有效的癌症治疗新模式。一些患者对免疫疗法反应良好,肿瘤体积急剧缩小,但是另一些患者仅有部分反应或根本没有反应。世界各地的临床医生和科学家正在努力了解为什么免疫疗法只对部分患者有帮助。
De Carvalho博士说,“我们未来的目标是利用这一策略与其他免疫疗法相结合,增强抗肿瘤免疫力。我们想象着未来的临床试验:我们从患者身上收集T细胞,在实验室里进行表观遗传学治疗。这可能扩大杀癌细胞(cancer killing cell,即杀死癌细胞的细胞)的军队,有效地构建出一支‘超级士兵军队’。然后,这些细胞可以重新注入患者体内,从而潜在地增强它们对肿瘤的内在免疫反应。”De Carvalho博士的实验室首先观察到,在用表观遗传学疗法治疗的小鼠肿瘤中,T细胞浸润增加。当他们移除这些T细胞时,这种疗法不再起作用,这表明这些T细胞对这种疗法的成功起到了促进作用。
这些研究人员对这一发现很感兴趣,便着手在实验室中将这种表观遗传DNA修饰疗法直接应用于T细胞。他们从健康的人类供体以及黑色素瘤、乳腺癌、卵巢癌和结直肠癌患者身上分离出T细胞。他们的结果证明,这种表观遗传学疗法增强了这些T细胞的杀癌能力。
doi:10.1093/nar/gkaa1050
近日,一项刊登在国际杂志Nucleic Acids Research上的研究报告中,来自东京工业大学等机构的科学家们通过研究开发了一种新型数学模型,利用该模型或能帮助定量评估特定表观遗传学改变对基因转录率的影响;研究者表示,基于这种方法,我们就能成功在体外制造重组的含有染色质的组蛋白修饰。文章中,研究人员提出了一种准确的定量方法来理解组蛋白位点特异性的改变如何影响染色质的可接近性和基因表达的水平。
单一蛋白质的产生是一个漫长而又复杂的过程。即使从DNA模板生产其蓝图(所谓的编码转录本)也会涉及多个步骤和参与者;DNA通常会被发现整齐地包裹在称之为组蛋白的蛋白质上形成一个核小体,这是一种称之为染色质的紧密浓缩结构的基本亚单位,其浓缩程度取决于有多少DNA可用于转录过程。这些组蛋白的改变(比如乙酰化修饰)会影响染色质对基因表达的可及性,这些表观遗传学在调节基因表达的过程中扮演着关键角色。截止到目前为止,研究人员并不清楚如何量化这些表观遗传学效应,以及位点特异性的组蛋白修饰如何影响基因的表达。
为了回答这一系列问题,这项研究中,研究人员开发了一种动力学模型,基于高度定量的实验结果来量化表观遗传改变对转录率的贡献。研究者Takinoue解释道,每个组蛋白的每个修饰状态对染色质转录的顺序步骤的贡献并没有被量化,因为我们很难用感兴趣的表观遗传学修饰来精确重建染色质的模板,并对从中得到的RNA转录进行量化分析。利用遗传密码扩展和细胞游离蛋白合成技术,我们合成了含有位点特异性乙酰化修饰的组蛋白H4,并重组了一个四乙酰化核小体。
【7】PLoS Med:女性孕期的饮食和生活方式或与后代机体DNA的表观遗传学修饰改变直接相关
doi:10.1371/journal.pmed.1003229
近日,一项刊登在国际杂志PLoS Medicine上的研究报告中,来自南安普敦大学等机构的科学家们通过研究发现,肥胖的孕妇或能通过改善饮食和更多的体育锻炼来帮助降低其后代所面临的健康风险;相关研究调查了高糖对妊娠糖尿病女性的影响以及对婴儿机体DNA的改变。
如今妊娠糖尿病在全球女性中越来越普遍,而且人群的肥胖率也在不断增加,这或许会增加女性孕期和分娩并发症的风险,还会增加后代在晚年时患代谢性疾病的风险。有研究表明,高水平的葡萄糖会诱发妊娠糖尿病女性子宫内发育中胎儿机体的表观遗传学改变,从而导致后代在出现严重的健康结局。
这项研究中,研究人员对来自英国孕期饮食和活动试验计划(UPBEAT)中超过550名肥胖孕妇和儿童进行研究,该试验旨在改善英国肥胖孕妇的饮食和体育锻炼情况,相比对照组(孕期生活方式并未发生任何改变)而言,那些通过改变饮食来降低血糖指数、减少脂肪摄入并增加体育锻炼的孕妇机体的体重增加更少,且新陈代谢也更为健康。研究人员比较了妊娠糖尿病孕妇和未患糖尿病的孕妇所生的后代机体中DNA甲基化的水平和模式差异,随后深入分析来观察是否孕期饮食和体育锻炼的干预能改变妊娠糖尿病女性所生后代机体的DNA甲基化修饰。
图片来源:Shutterstock
doi:10.1073/pnas.1912074117
近日,一项刊登在国际杂志Proceedings of the National Academy of Sciences上的研究报告中,来自欧洲分子生物学实验室的科学家们通过研究揭示了表观遗传学修饰背后的分子机制,DNA制造RNA进而制造蛋白质是分子生物学中的一项基本原理,基因表达的过程会以多种方式被严格调控,DNA自身会携带一种可逆转的化学修饰过程,即甲基化修饰,其能影响基因的表达。
这项研究中,研究人员首次揭示了DNA甲基化如何通过诱导沉默复合体的组装来指导细胞抑制部分基因组的表达;DNA甲基化是当细胞分裂时能够遗传的唯一一种表观遗传学修饰过程,这就意味着,一旦特殊的DNA序列被甲基化修饰,其就会在有机体的整个生命阶段存在,甲基化就好比是DNA上的一种标记,其能以一种依赖于亲本来源的方式促进某些基因失活,此外,DNA的甲基化还能作为一种细胞防御机制,其能防止寄生虫的DNA片段在基因组中移动并威胁其完整性,这种修饰就能指导细胞抑制这些所谓的转座子的功能。
尽管进行了很多年的研究,但目前研究人员并不清楚DNA甲基化抑制基因表达背后的精确分子机制,这项研究中,研究人员发现,蛋白质TRIM28或许是抑制甲基化基因所需要的,同时其也是此前研究人员并未发现与DNA甲基化有关联的一种沉默因子,然而,TRIM28并不会直接与DNA相互作用,这就意味着,其它蛋白质或许参与到了上述过程中去。
【9】Nat Commun:DNA的表观遗传学修饰竟会促进乳腺癌对激素疗法产生耐受性
doi:10.1038/s41467-019-14098-x
对激素疗法产生耐受性的乳腺癌细胞中的DNA常常会发生表观遗传学的改变,激素疗法是一种治疗ER+乳腺癌的有效疗法,而ER+乳腺癌在所有诊断的乳腺癌患者中占到了70%的比例;逆转这些表观遗传学改变或许有望帮助降低乳腺癌患者的复发率。
近日,一项刊登在国际杂志Nature Communications上的研究报告中,来自悉尼加文医学研究所等机构的科学家们通过研究发现,对激素疗法耐受的ER+乳腺癌细胞中DNA的3-D结构或许发生了“重新布线”(rewired),其能够改变基因的激活和失活。研究者Clark教授表示,这项研究中我们首次揭示了一种关键的3-D DNA相互作用,其与乳腺癌是否对激素疗法敏感有关,阐明其中的过程或能帮助揭示ER+癌症躲避激素疗法的分子机制,并有望帮助开发新型乳腺癌疗法。
雌激素或许会无意中促进癌症的进展,当雌激素“停靠”到细胞中时就会诱发ER+乳腺癌生长,阻断雌激素的激素疗法能够成功阻断癌症生长并减少复发率,然而随着时间延续,很多乳腺癌仍然会对该疗法产生耐药性。疗法耐受是癌症患者面临的一个主要的健康问题,其会导致三分之一接受激素疗法的ER+乳腺癌患者在15年内出现疾病复发。
【10】Science:我国科学家揭示人类早期胚胎发育中的组蛋白修饰重编程
doi:10.1126/science.aaw5118
在真核生物中,组蛋白与带负电荷的双螺旋DNA组装成核小体。因氨基酸成分和分子量不同,组蛋白主要分成5类:H1,H2A,H2B,H3和H4。除H1外,其他4种组蛋白均分别以二聚体形式相结合,形成核小体核心。DNA便缠绕在核小体的核心上。而H1则与核小体间的DNA结合。组蛋白修饰(histone modification)是指组蛋白在相关酶作用下发生甲基化、乙酰化、磷酸化、腺苷酸化、泛素化、ADP核糖基化等修饰的过程。
组蛋白上发生甲基化的位点是赖氨酸和精氨酸。赖氨酸能够分别发生一、二、三甲基化,精氨酸只能发生一、二甲基化。在组蛋白H3上,共有5个赖氨酸位点可以发生甲基化修饰。一般来说,组蛋白H3K4的甲基化主要聚集在活跃转录的启动子区域。组蛋白H3K9的甲基化与基因的转录抑制及异染色质有关。H3K27甲基化可导致相关基因的沉默,并且与X染色体失活相关。H3K36的甲基化与基因转录激活相关。
组蛋白修饰调节基因表达和发育。在一项新的研究中,为了解决在人类早期发育中组蛋白修饰如何发生重编程,中国清华大学生命科学学院的颉伟(Wei Xie)课题组、郑州大学第一附属医院的孙莹璞(Ying-Pu Sun)课题组和徐家伟(Jiawei Xu)课题组研究了人卵母细胞和早期胚胎中的关键组蛋白标记。相关研究结果发表在Science期刊上,论文标题为“Resetting histone modifications during human parental-to-zygotic transition”。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。