重磅!DNA甲基化引起的脂代谢障碍加速衰老
来源:生物谷原创 2022-06-20 17:22
该研究揭示了导致衰老的表观遗传-代谢轴,并说明了基于人工智能的方法在结构功能研究中的力量。
衰老是一个不可避免的生命过程,其特征是对疾病的易感性增加,分子保真度下降,组织和器官功能进行性下降。表观遗传改变通过整合环境信号来调节基因表达和下游细胞过程,在衰老过程中发挥关键作用。
衰老和DNA甲基化水平之间的完整关系直到最近才被清楚地描述出来,数百个与生物年龄相关的DNA甲基化水平的CpG位点被精确定位。表观遗传改变和代谢功能障碍是衰老的两个标志。然而,它们相互作用如何调节衰老的机制,特别是在哺乳动物中,在很大程度上仍然不清楚。

图片来源: https://doi.org/10.1038/s41392-022-00964-6
近日,来自中国科学院的研究者们在Signal Transduction and Targeted Therapy杂志上发表了题为“Lipid metabolism dysfunction induced by age-dependent DNA methylation accelerates aging”的文章,该研究揭示了导致衰老的表观遗传-代谢轴,并说明了基于人工智能的方法在结构功能研究中的力量。
在本研究中,研究者展示了ELOVL脂肪酸延伸酶2(ELOVL2),这是一个表观遗传学改变与年龄预测高度相关的基因,通过调节脂质代谢而促进衰老。研究者应用人工智能来预测ELOVL2的蛋白质结构及其与底物的相互作用。
ELOVL2功能受损通过增加内质网应激和线粒体功能障碍扰乱脂质合成,导致细胞和生理水平的关键衰老表型。此外,线粒体活性的恢复可以挽救由ELOVL2缺乏引起的人视网膜色素上皮(RPE)细胞的年龄相关性黄斑变性(AMD)表型;这表明人类和小鼠的保守机制。
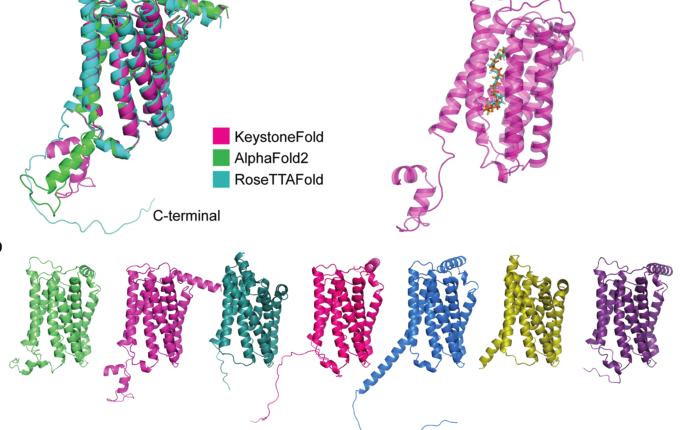
ELOVL的预测结构
图片来源: https://doi.org/10.1038/s41392-022-00964-6
在本研究中,研究者揭示了一个有助于衰老的表观遗传-代谢轴,并说明了基于人工智能的方法在结构功能研究中的力量。表观遗传变化改变了衰老过程中的新陈代谢,并提供了更好的理解潜在的表观遗传和代谢衰老过程的分子机制。
代谢功能障碍是年龄相关表观遗传学改变的效应者。同时,代谢功能障碍也可能是导致表观遗传变化的中介因素。代谢如何调控与年龄相关的表观遗传学改变的机制仍需进一步研究。
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


