Cell重磅:余建华团队发现并解析ILC2细胞的抗癌机制,可对抗各种肿瘤,改变细胞治疗格局
来源:生物世界 2024-01-17 10:05
研究证明了人类Ⅱ型固有淋巴细胞(ILC2)的特性,并确认这一固有免疫细胞亚群是具有广泛抗肿瘤活性的溶细胞性免疫效应细胞家族的一员,并可能为癌症的过继细胞疗法增添新手段。
希望之城国家医学中心余建华教授在 Cell 期刊发表了题为:Therapeutic application of human type 2 innate lymphoid cells via induction of granzyme B-mediated tumor cell death 的研究论文。
该研究发现人类Ⅱ型固有淋巴细胞(ILC2)是具有广泛抗肿瘤活性的溶细胞性免疫效应细胞家族的一员,通过分泌颗粒酶B(GZMB)诱导肿瘤的细胞焦亡和/或细胞凋亡,从而溶解各种肿瘤。该研究还开发了人类ILC2细胞的快速扩增平台,并在小鼠模型上验证了扩增的ILC2细胞对白血病和实体瘤积极的治疗效果。


余建华教授
余建华于2003年博士毕业于普渡大学,并在俄亥俄州立大学从事博士后研究并任职直至终身正教授,此后加入希望之城国家医学中心。余建华教授专注于新型细胞免疫疗法和溶瘤病毒疗法相关的基础和转化研究,还创立类一家名为CytoImmune Therapeutics的同种异体NK细胞疗法公司,该公司已有一款NK细胞疗法(CYTO-102)进入临床试验。
Ⅱ型固有淋巴细胞(ILC2),以GATA3的表达和Th2细胞相关细胞因子(包括IL-4、IL-5、IL-9和IL-13以及AREG)的产生为特征,它们在细胞因子IL-25、IL-33和胸腺基质淋巴细胞生成素(TSLP)的刺激下产生。
在小鼠中,已确定了两个主要的ILC2亚群:IL-33诱导的稳态天然ILC2和IL-25诱导的炎性ILC2。在人类中,ILC2被描述为CD127+ CRTH2+ c-Kit+/-细胞,表达IL-33受体ST2和IL-25受体IL-17RB亚基。在功能上,ILC2参与调节炎症,并作为固有和适应性2型免疫之间的关键桥梁。
但有争议的是,在不同的小鼠肿瘤模型中,ILC2既促进又抑制抗肿瘤免疫。一方面,小鼠ILC2可以通过产生2型细胞因子促进髓源性抑制细胞(MDSC)的扩增和活性,从而抑制抗肿瘤免疫。另一方面,它们还可以通过IL-5依赖的方式招募和激活嗜酸性粒细胞,抑制小鼠NK细胞介导的抗肿瘤转移免疫反应。而最近的一些研究显示,小鼠ILC2可以通过发挥抗肿瘤作用来减少胰腺癌、肺癌和结直肠癌模型中的转移扩散。
虽然这些关于ILC2在不同肿瘤类型中作用的对比数据可能反映了ILC2异质性和/或不同肿瘤微环境(TME)的差异,但这也提示了我们更好地理解这种独特的细胞类型的必要性。此外,大多数ILC2研究都集中在小鼠身上,对人类ILC2的研究有限。
因此,该研究尝试进一步描述正常和疾病环境中的人类ILC2,以弥补我们目前对于ILC2的认知。
具体来说,该研究发现,人类ILC2会分泌颗粒酶B(GZMB),并通过诱导细胞焦亡和/或细胞凋亡直接溶解肿瘤细胞,这由DNAM-1−CD112/CD155相互作用调控,使负调控因子FOXO1失活。随着时间的推移,急性髓系白血病(AML)细表面的CD155高表达损害了DNAM-1和GZMB的表达,从而允许肿瘤细胞的免疫逃逸。
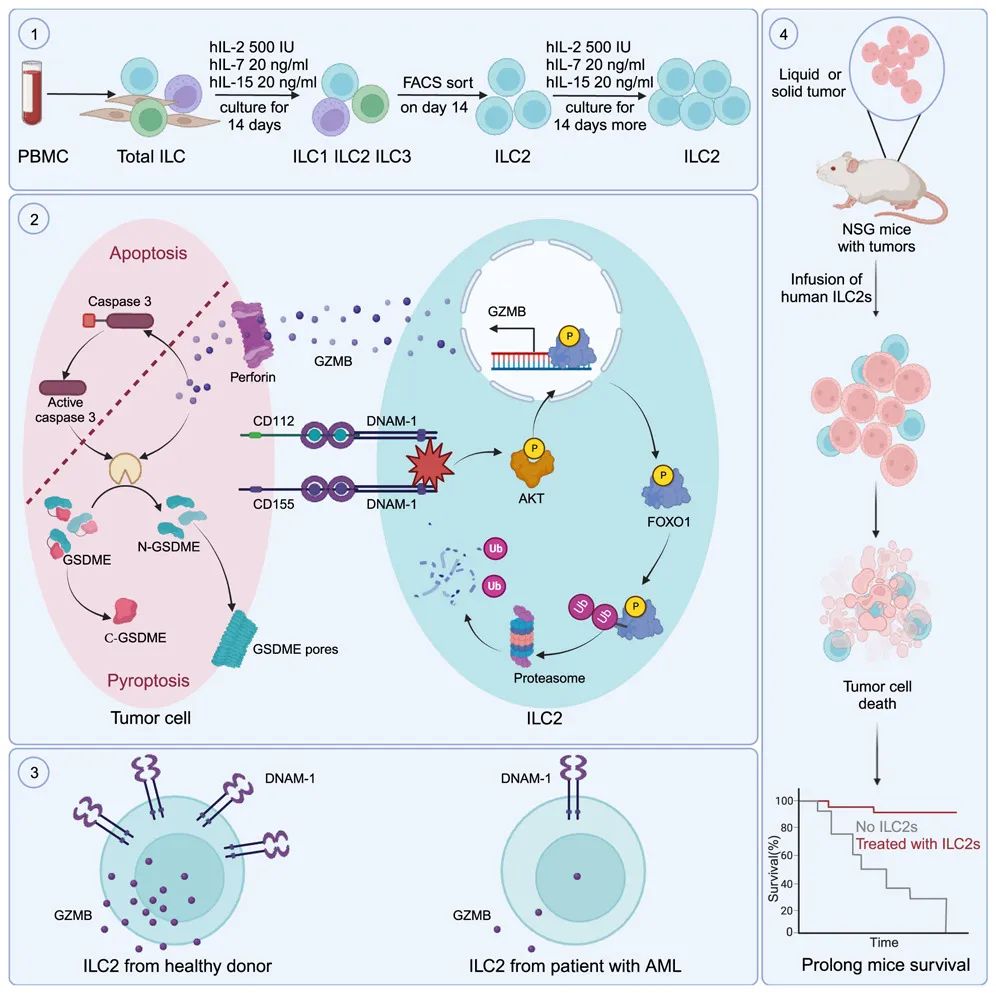
更重要的是,研究团队开发了一个可靠的平台,可以在4周内将人类ILC2扩增至2000倍,在白血病和多种实体瘤模型中,注射外源性扩增的人类ILC2,在体内表现出显著的抗肿瘤作用。
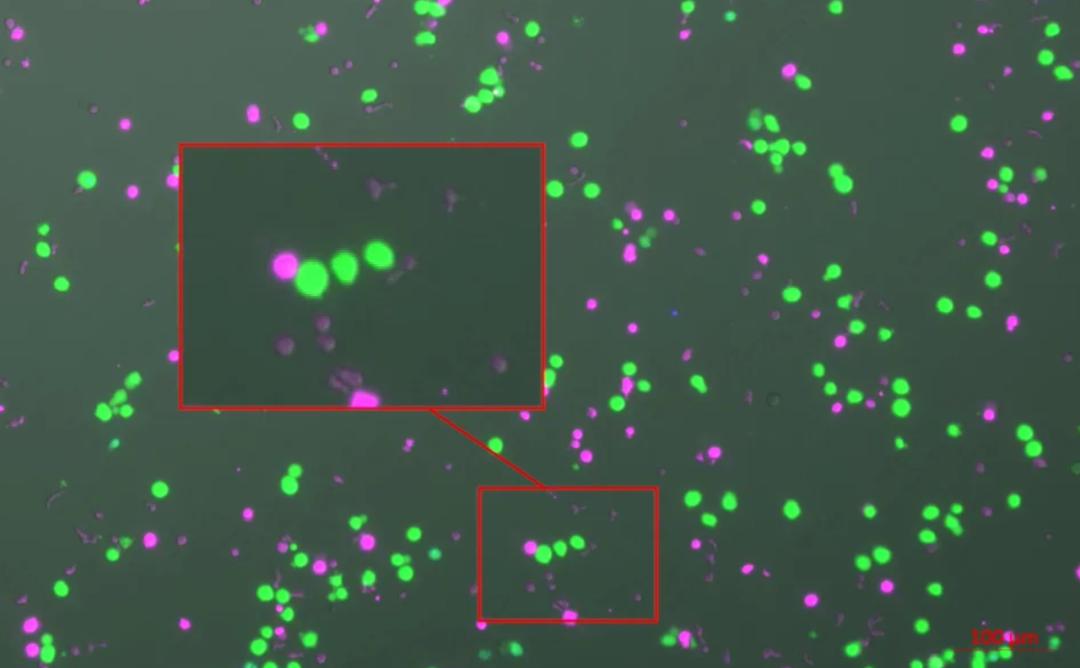
ILC2 细胞(洋红色)根除急性髓性白血病细胞(绿色)。ILC2细胞还可以对抗其实体瘤(包括胰腺癌、肺癌和胶质瘤细胞)
总的来说,该研究证明了人类Ⅱ型固有淋巴细胞(ILC2)的特性,并确认这一固有免疫细胞亚群是具有广泛抗肿瘤活性的溶细胞性免疫效应细胞家族的一员,并可能为癌症的过继细胞疗法增添新手段。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


