Nature子刊: 靶向LIFR−NF-κB−LCN2轴控制肝肿瘤发生和铁死亡
来源:本站原创 2022-01-22 18:47
对铁死亡的认识不断增长,提示了铁死亡在癌症中的作用和治疗潜力,但尚未转化为有效的治疗方法。
对铁死亡的认识不断增长,提示了铁死亡在癌症中的作用和治疗潜力,但尚未转化为有效的治疗方法。肝癌,主要是肝细胞癌(HCC),具有很高的致命性,治疗选择有限。LIFR在肝细胞癌中经常下调。在这里,通过研究肝细胞特异性和可诱导的Lifr基因敲除小鼠,作者发现LIFR的缺失促进了肝脏肿瘤的发生,并赋予了对药物诱导的铁下垂的抵抗力。
图片来源: https://doi.org/10.1038/s41467-021-27452-9
多项研究表明索拉非尼具有铁死亡诱导作用。另一方面,Conrad和他的同事最近报道(基于体外细胞培养实验),sorafenib在一组癌细胞系中不会引发铁细胞凋亡,尽管SLC7A11大量表达,经典的系统xc抑制剂只能在肿瘤细胞系中诱导铁细胞死亡。
癌细胞对索拉非尼诱导的铁死亡不敏感的另一个可能原因是,LIFR在多种肿瘤类型中表达下调,包括肝癌、膀胱癌、乳腺癌、结肠癌、肾癌、肺癌、直肠癌和甲状腺癌。因此,未来的工作应该确定LIFR的下调或丢失是否在多种癌症对索拉非尼诱导的铁死亡的耐药性中起到因果作用。
值得注意的是,肝癌患者来源的异种移植瘤通常具有低水平的LIFR和高水平的Lcn2;当携带这些肿瘤的小鼠接受索拉非尼联合Lcn2中和抗体治疗时,比单独治疗索拉非尼获得了更好的治疗反应。值得注意的是,联合治疗促进了肿瘤组织中的脂质过氧化和铁死亡。
另一方面,LIFR水平高、Lcn2水平低的PDX肿瘤对Lcn2中和抗体无反应,对索拉非尼单药治疗高度敏感。提示LIFR高表达和Lcn2低表达可用于预测索拉非尼的疗效,LIFR低表达和Lcn2高表达可用于筛选可能受益于索拉非尼和Lcn2中和抗体联合治疗的肝癌患者。
此外,考虑到放疗和免疫治疗通过抑制SLC7A11而触发脂质氧化和铁下垂,作者预计LCN2中和抗体可能有可能使肿瘤对放射和免疫治疗敏感,这一点值得进一步研究。值得注意的是,虽然Lcn2基因缺失的小鼠对细菌感染和铁超载毒性更为敏感,但这些小鼠的发育和生长正常,因此在生理条件下,全身中和Lcn2不会对正常组织造成实质性的毒性。
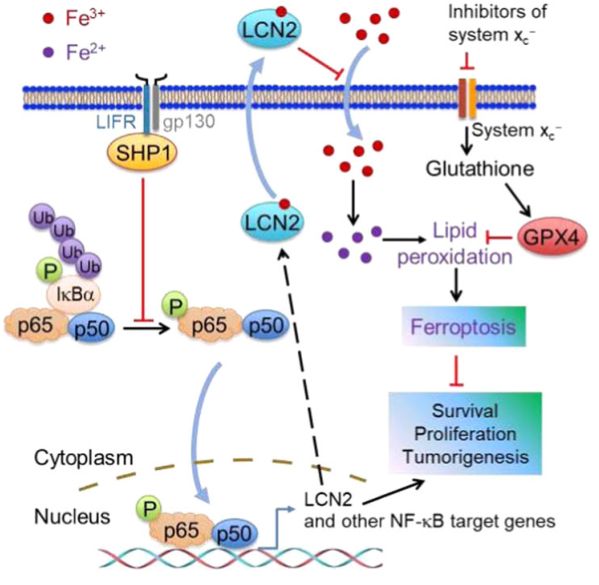
LIFR−NF-κB−LCN2轴在肝脏肿瘤发生和铁死亡中的作用模型
图片来源: https://doi.org/10.1038/s41467-021-27452-9
早期的工作表明,肿瘤抑制基因,包括apc、gstp1和cdh1,在肝癌中通常甲基化。随后对肝癌的研究发现了额外的高甲基化基因。这些基因中有一些被认为是肝肿瘤抑制因子,但在活体肝细胞癌中没有功能特征;其中一个基因是LIFR,编码白血病抑制因子受体。完全基因敲除小鼠在出生后24小时内死亡,并表现出神经元、骨骼、代谢和胎盘缺陷。
尽管组织特异性LIFR在小鼠子宫上皮中的消融会导致胚胎着床失败,但LIFR在包括肝脏在内的其他成人器官中的功能仍不清楚。在这项工作中,作者证明了LIFR的缺失促进了肝脏肿瘤的发生,并通过NF-κB介导的铁隔离细胞因子LCN2的上调来增强对药物诱导的铁死亡的抵抗力。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



