慢性自发性荨麻疹(CSU)新药!Dupixent(达必妥®)3期临床:显著减少瘙痒&荨麻疹!
来源:本站原创 2022-03-01 15:19
Dupixent已在中国获批上市,用于≥6岁人群治疗中度至重度特应性皮炎(AD)。
慢性自发性荨麻疹(CSU,图片来源:rappler.com)
2022年02月28日讯 /生物谷BIOON/ --赛诺菲(Sanofi)与合作伙伴再生元(Regeneron)近日在2022年美国过敏、哮喘和免疫学学会(AAAAI)年会上公布了抗炎药Dupixent(中文商品名:达必妥,通用名:度普利尤单抗,dupilumab)治疗中度至重度慢性自发性荨麻疹(CSU)3期随机双盲安慰剂对照LIBERTY-CUPID临床项目(NCT04180488)关键临床研究Study A的详细阳性结果。
数据显示,在先前没有接受过生物疗法治疗(biologic-naive,生物疗法初治)的中重度CSU患者中,治疗24周,与标准护理疗法抗组胺药(antihistamine)单独治疗相比,Dupixent+抗组胺药联合治疗方案显著减少了瘙痒和荨麻疹,将瘙痒和荨麻疹活动评分降低了近一倍。
CSU是一种慢性炎症性皮肤病,其特征是皮肤突然出现荨麻疹和/或皮肤深层肿胀。尽管有标准的护理治疗,CSU患者通常会出现持续瘙痒或烧灼感等症状,这些症状会使人虚弱,并严重影响生活质量。肿胀通常发生在脸、手和脚上,也会影响喉咙和上呼吸道。CSU通常使用抗组胺药治疗,但在可用治疗方案有限的患者中,高达50%的患者的病情仍然无法控制。
CSU是一种复杂的慢性疾病。此次会议上公布的这些数据,强化了靶向阻断IL-4和IL-13治疗CSU的潜力。这2种细胞因子是2型炎症的关键驱动因素。
德国柏林查理大学医学院教授Marcus Maurer表示:“尽管使用了标准的抗组胺药,但许多CSU患者仍在与荨麻疹和皮下肿胀相关的极度瘙痒、灼烧和疼痛中挣扎,这会严重扰乱他们的日常生活。这些令人鼓舞的结果表明,在单靠抗组胺药无法实现疾病控制的患者中,添加Dupixent治疗的患者,体征和症状得到改善,疾病得到更好的控制。”

LIBERTY-CUPID是一项3期随机双盲安慰剂对照临床项目。Study A研究在138例年龄≥6岁的中重度CSU患者中开展,这些患者尽管使用了非镇静性H1抗组胺药物但仍有症状、且之前没有使用过omalizumab(奥玛利珠单抗)治疗。研究中,患者被随机分配进入2个治疗组:(1)Dupixent治疗组接受Dupixent(注射液,皮下注射)+非镇静性H1抗组胺药(片剂,口服),治疗24周;(2)安慰剂组接受匹配的安慰剂(注射液,皮下注射)+非镇静性H1抗组胺药(片剂,口服),治疗24周。研究的主要终点是:治疗24周后瘙痒相对基线的变化(采用每周瘙痒严重程度评分[ISS7]测量)、瘙痒与荨麻疹相对基线的变化(采用每周荨麻疹活动评分[UAS7]测量)。
2021年7月公布的顶线结果显示,Study A研究在治疗24周时达到了主要终点和全部关键次要终点。2022年度AAAAI年会上公布的数据显示:与接受安慰剂和标准护理疗法抗组胺药物的患者组相比,Dupixent+抗组胺药物联合治疗组瘙痒和荨麻疹活动减少近一倍,持续改善直至第24周。具体数据如下:
——治疗24周,根据0-21分瘙痒严重程度量表测量结果(Dupixent组瘙痒严重程度降低10.24分,安慰剂组瘙痒严重程度降低6.01分,p<0.001),Dupixent组瘙痒严重程度降低63%、安慰剂组瘙痒严重程度降低35%,这是美国的主要终点(欧盟的次要终点)。
——治疗24周,根据0-42分荨麻疹活动量表测量结果(Dupixent组降低20.53分,安慰剂组降低12.00分,p<0.001),Dupixen组荨麻疹活动(瘙痒和荨麻疹)严重程度降低65%,安慰剂组减少37%,这是欧盟的主要终点(美国的次要终点)。
——Dupixent的安全性结果与该药已批准的皮肤病适应症中的已知安全性概况相似。在24周治疗期间,Dupixent组和安慰剂组不良事件总体发生率相似(Dupixent组50%,安慰剂组59%)。最常见的不良事件是注射部位反应(Dupixent组11%,安慰剂组13%)。
LIBERTY-CUPID项目Study B研究在接受标准护理治疗但仍有症状、并且对omalizumab(奥玛利珠单抗)不耐受或应答不足的中度至重度CSU成人和青少年患者中开展。根据2022年2月开展的一项预先指定的中期分析,该研究因被判定无效而将停止。虽然观察到瘙痒和荨麻疹的减少有积极的数值趋势,但中期分析结果显示主要终点没有统计学意义。目前,Dupixent在CSU中的潜在应用正处于临床开发中,其安全性和有效性尚未得到任何监管机构的全面评估。
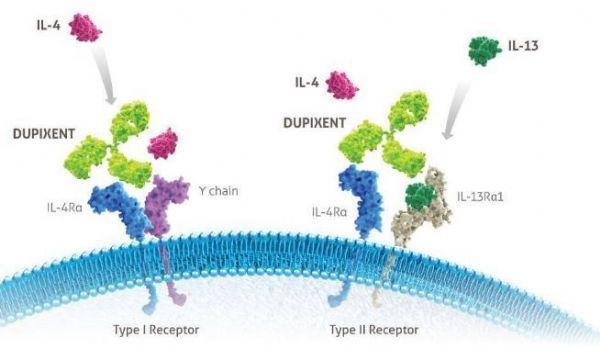
Dupixent作用机制(图片来源:dupixenthcp.com)
Dupixent靶向2型炎症的关键驱动因素,该药是一种全人源化单克隆抗体,特异性抑制2种关键蛋白IL-4和IL-13的过度激活信号。IL-4/IL-13是2种炎症因子,据认为是过敏性疾病和其他2型炎症疾病中内在炎症的关键驱动因素,包括特应性皮炎、哮喘、嗜酸细胞性食管炎、草过敏、花生过敏等。
Dupixent于2017年3月底上市,目前已获批治疗3种由2型炎症导致的疾病:中度至重度特应性皮炎(≥6岁患者)、中度至重度哮喘(≥6岁患者)、伴鼻息肉的慢性鼻-鼻窦炎(CRSwNP,成人患者)。
在中国,2020年6月,Dupixent(达必妥)获得国家药品监督管理局(NMPA)批准,用于治疗成人中重度特应性皮炎(AD)。达必妥是全球首个也是唯一获批治疗成人中重度特应性皮炎的靶向生物制剂,填补了国内临床未被满足的需求,能快速、显著、持续地改善特应性皮炎患者的皮损程度和瘙痒症状。得益于药监改革的推动,达必妥提前两年在中国获批,为中国患者提供了全新的治疗选择。
目前,赛诺菲和再生元也正在开展一项广泛的临床项目,评估Dupixent治疗由过敏和其他2型炎症引起的疾病,包括:慢性阻塞性肺病(3期)、儿童特应性皮炎(6个月至5岁,3期)、嗜酸性食管炎(3期)、大疱性类天疱疮(3期) 、结节性痒疹(3期)、慢性自发性荨麻疹(3期)、慢性诱导性荨麻疹(3期)、无鼻息肉的慢性鼻窦炎(3期)、过敏性真菌性鼻窦炎(3期)、过敏性支气管肺曲霉菌病(3期)、花生过敏(2期)。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


