Nature子刊:于杰/盖景鹏团队揭示粘多糖症相关溶酶体乙酰转移酶HGSNAT的跨膜催化机制
来源:生物世界 2024-05-21 09:40
本研究揭示了HGSNAT介导的一种全新的溶酶体跨膜区乙酰化的催化机制,完全不同于传统的乙酰转移酶,为开发更有效的治疗MPS IIIC疾病的治疗策略提供了结构见解。
中科院上海有机化学研究所生物与化学交叉研究中心于杰课题组联合上海科技大学盖景鹏课题组以及加拿大蒙特利尔大学Alexey V. Pshezhetsky课题组在 Nature Structural & Molecular Biology 期刊发表了题为:Structure and mechanism of lysosome transmembrane acetylation by HGSNAT 的研究论文。
该研究解析了HGSNAT 无底物结合apo状态、与乙酰辅酶A(Ac-CoA)结合以及与乙酰化产物结合的冷冻电镜结构,分辨率高达2.59 Å,揭示了HGSNAT介导的一种全新的溶酶体跨膜区乙酰化的催化机制,完全不同于传统的乙酰转移酶,为开发更有效的治疗MPS IIIC疾病的治疗策略提供了结构见解。
在这项研究中,研究团队首先解析了以二聚化的形式存在的HGSNAT,整体形状类似于大写字母“M”,是一种全新的折叠结构(图1)。HGSNAT的跨膜螺旋形成亲水性的跨膜通道。位于胞质侧的Ac-CoA进入跨膜通道并引起通道扩张。通道中的活化位点组氨酸和天冬酰胺催化乙酰基从Ac-CoA转移到位于溶酶体侧的HS的葡萄糖胺基,完成乙酰基从细胞质一侧转移到溶酶体侧。反应后,游离CoA被释放到细胞质中,乙酰化HS扩散到溶酶体腔内,进一步被降解(图2)。
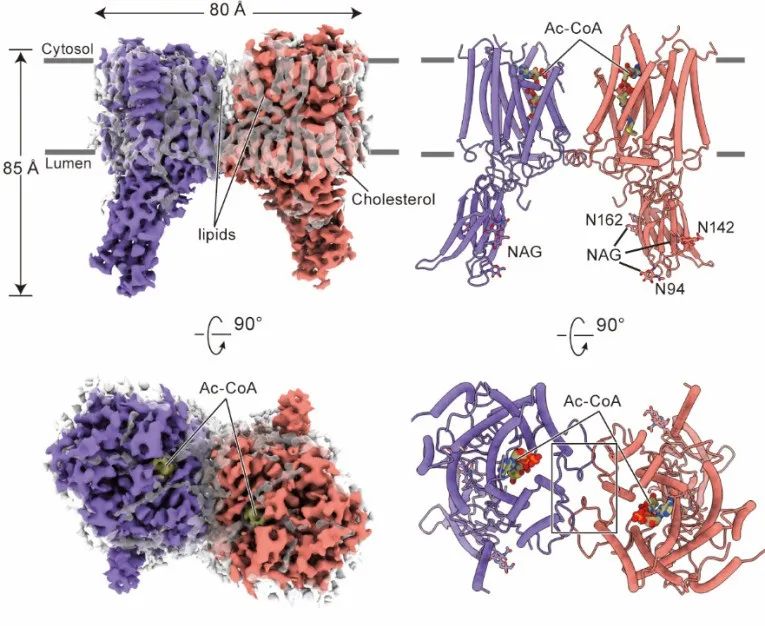
图1 HGSNAT的整体结构
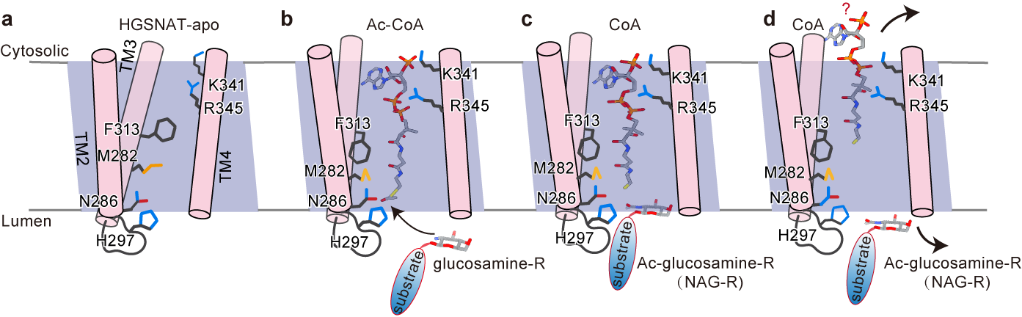
图2 HGSNAT的跨膜催化模型
中国科学院上海有机化学研究所生物与化学交叉研究中心博士研究生徐睿声、上海科技大学硕士研究生宁莹洁为论文共同第一作者。于杰研究员、盖景鹏教授与Alexey V. Pshezhetsky教授为论文共同通讯作者。中国科学院有机所交叉中心朱正江研究员以及其他作者也做出了重要贡献。该工作得到了上海临港实验室和上海浦江计划的资助。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


