iScience:利用诱导性多能干细胞构建研究肥厚型心肌病的体外模型
来源:生物谷原创 2024-07-07 10:42
基因突变发生在基因组中编码力学、挤压蛋白的部分,即肌节(sarcomeres)。如果运动蛋白出了问题,为什么电流会受到影响?
用动物来研究心脏病并不总能很好地转化为人类的健康结果,而且可用于研究的人类心脏细胞在人体外也无法正常发挥作用。
圣路易斯华盛顿大学麦凯威工程学院生物医学工程助理教授Nathaniel Huebsch说,“你无法让它们存活,更无法让它们在人体外工作足够长的时间来研究这些过程。”Huebsch 正在研究一种携带突变的细胞,所携带的突变会导致肥厚型心肌病(hypertrophic cardiomyopathy, HCM),这种疾病会在几乎没有预警的情况下引发心力衰竭。

在一项新的研究中,Huebsch及其同事们通过诱使干细胞表现得像成熟的心脏细胞,使得诱导性多能干细胞(iPSC)衍生的心肌细胞表现得像携带导致HCM突变的成熟心脏细胞,从而解决了这一难题。相关研究结果近期发表在iScience期刊上,论文标题为“Substrate mechanics unveil early structural and functional pathology in iPSC micro-tissue models of hypertrophic cardiomyopathy”。
为了让干细胞像成熟的心脏细胞一样发挥作用,这些作者在“机械压力”的训练营中对这些细胞进行了训练。本质上,他们试图复制心脏细胞作为运动肌肉的一部分所经历的运动和阻力。如果他们将他们的干细胞附着在坚硬的界面上,它们就必须“工作”才能拉动该界面。心脏细胞的工作也可能是导致HCM的突变如何导致这种疾病的关键。
圣路易斯华盛顿大学麦凯威工程学院生物医学工程学教授Jonathan Silva说,电心律失常经常影响HCM患者,但导致HCM的突变并不在编码电活动的基因附近。
基因突变发生在基因组中编码力学、挤压蛋白的部分,即肌节(sarcomeres)。如果运动蛋白出了问题,为什么电流会受到影响?Silva说,“这就像你的水管出了问题,灯却灭了一样。”通过这项新的研究,Silva和Huebsch如今对这种情况的潜在原因有了更好的了解。
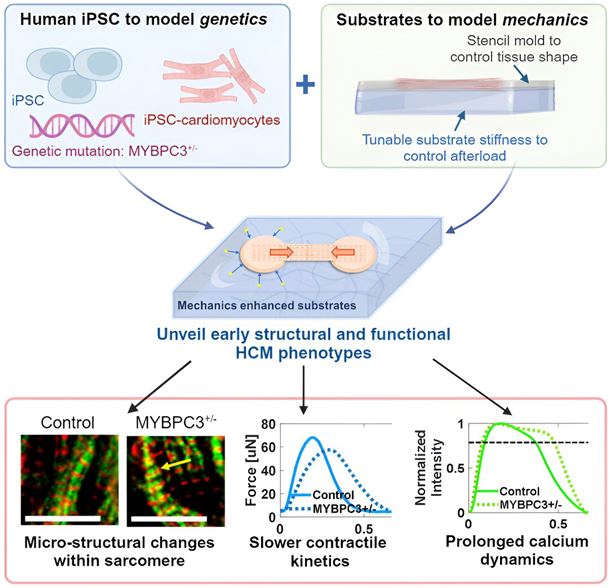
图片来自iScience, 2024, doi:10.1016/j.isci.2024.109954
Huebsch说,这种肌球蛋白结合蛋白C(MYBPC3+/-)突变会导致肌丝结构发生非常微妙的变化,而肌丝是细胞中将钙转化为力的部分。在 HCM 中,这种机械应力突变似乎影响了钙离子进入细胞的方式,以至于细胞容易发生心律失常。
Silva说,这项新研究推动了这一领域的发展,因为对心脏的机械和电功能之间的联系还没有很好的研究,这项研究显示了机械蛋白的遗传变异如何导致电问题。
Silva希望利用计算工具找到哪些特定的钙通道受到了破坏,对药物和机械压力进行修补,并建立不同的模型来预测患者的预后。(生物谷Bioon.com)
参考资料:
Jingxuan Guo et al. Substrate mechanics unveil early structural and functional pathology in iPSC micro-tissue models of hypertrophic cardiomyopathy. iScience, 2024, doi:10.1016/j.isci.2024.109954.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


