Nat Commun:揭示肥胖诱导的机体炎症和代谢功能异常背后的特殊细胞机制
来源:生物谷原创 2024-05-11 14:09
这项研究中,研究人员通过进行动物实验、单核RNA测序研究和活体成像研究,仔细分析了在炎性巨噬细胞中特异性存在的特殊蛋白—TM4SF19。
脂肪组织(AT,Adipose tissue)能以一种复杂的过程适应营养过剩,在这一过程中,特殊的免疫细胞会移除并利用新的脂肪细胞来待提供功能异常和处于压力状态下的脂肪细胞;在被招募到脂肪组织中的免疫细胞中,脂质相关巨噬细胞(LAMs,lipid-associated macrophages)已经成为肥胖和涉及脂质压力和炎症的疾病中的关键参与者。
近日,一篇发表在国际杂志Nature Communications上题为“TM4SF19-mediated control of lysosomal activity in macrophages contributes to obesity-induced inflammation and metabolic dysfunction”的研究报告中,来自韩国首尔大学等机构的科学家们通过研究成功揭示了与肥胖相关的组织中炎症发生及代谢功能障碍背后的分子机制。
据世界卫生组织数据显示,截至2022年,全球大约有16%的人群处于肥胖状态,这种流行病是世界范围内升级最为迅速的一种疾病,也是引起诸如糖尿病、高血压和动脉粥样硬化等多种人类代谢性疾病发生的主要原因。营养物质的过度消耗会促进多种类型巨噬细胞浸润到脂质组织中,其中,某些巨噬细胞在清除死亡细胞和维持组织平衡过程中扮演着重要角色,而另一些巨噬细胞则会引发炎性反应;在肥胖人群中,这些炎性巨噬细胞群的数量会迅速增加,从而就会加速与炎症和代谢功能相关的问题发生。
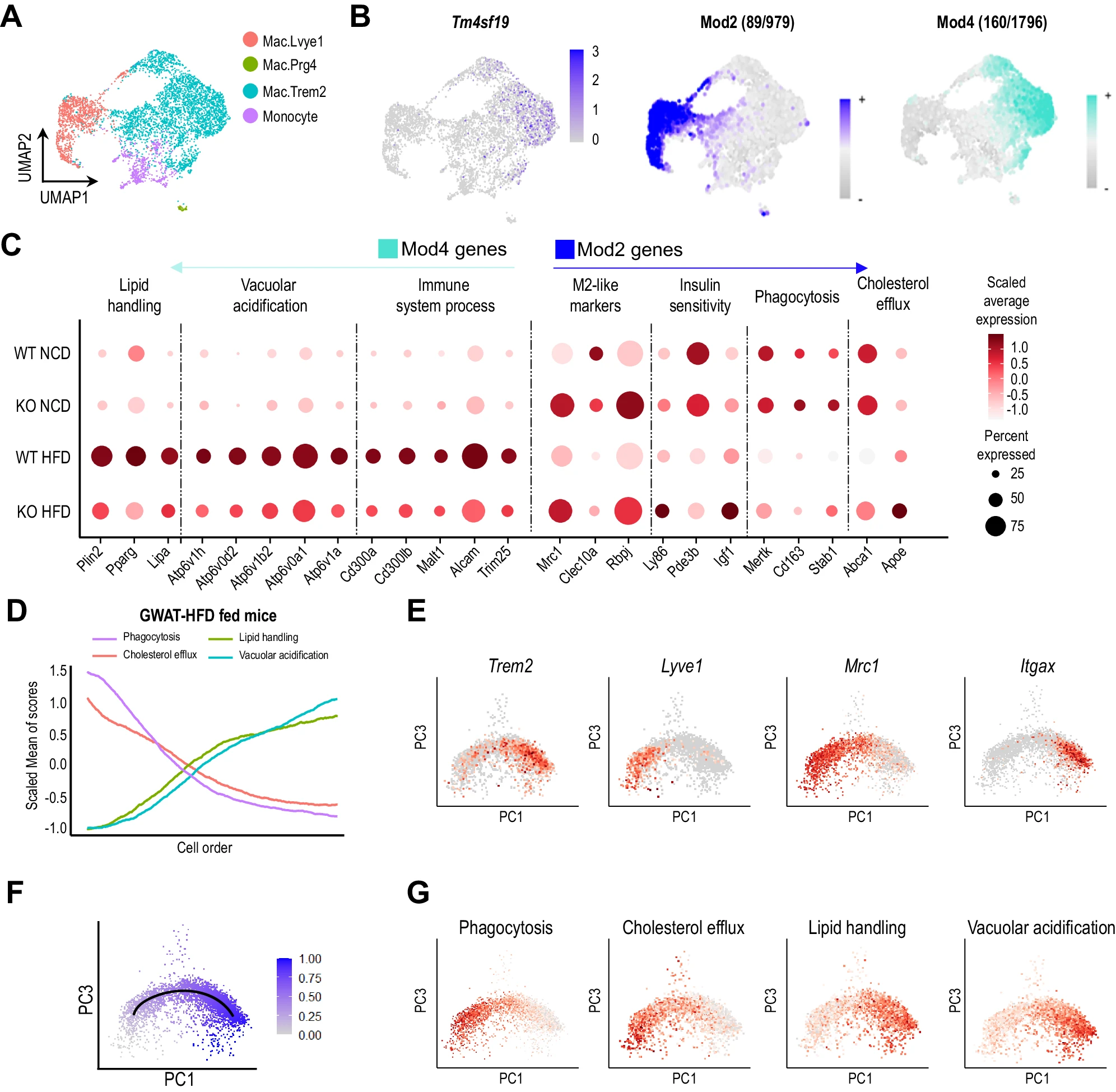
揭示肥胖诱导的机体炎症和代谢功能异常背后的特殊细胞机制
图片来源:Nature Communications (2024). DOI:10.1038/s41467-024-47108-8
这项研究中,研究人员通过进行动物实验、单核RNA测序研究和活体成像研究,仔细分析了在炎性巨噬细胞中特异性存在的特殊蛋白—TM4SF19。研究结果表明,被高脂肪饮食喂养的动物脂肪组织中TM4SF19的水平会显著增加,而值得注意的是,研究人员发现,这种蛋白或能抑制溶酶体中存在的泵(即V-ATP酶,V-ATPase),溶酶体中含有多种水解酶,其在溶酶体中pH调节中扮演着重要角色,因此,这或许就会阻碍巨噬细胞清除消耗脂肪组织的吞噬过程。
研究者指出,相反,缺失TM4SF19的巨噬细胞则能在清除死亡脂肪细胞方面表现出显著增强的效力,这不仅能阻止高脂肪饮食所诱导的体重增加,而且还能通过遏制组织炎症和胰岛素抵抗来改善机体的代谢功能异常。这项研究的意义在于,研究人员发现,存在于炎性巨噬细胞中的TM4SF1或许在肥胖患者中能帮助减缓炎症表现并增强患者机体的代谢功能。
最后,研究者表示,他们的最终目标就是揭示指导TM4SF19蛋白调节溶酶体活性背后的分子机制,相关研究结果有望帮助开发治疗人类肥胖和相关代谢性疾病的新型疗法。(生物谷Bioon.com)
参考文献:
Choi, C., Jeong, Y.L., Park, KM. et al. TM4SF19-mediated control of lysosomal activity in macrophages contributes to obesity-induced inflammation and metabolic dysfunction. Nat Commun 15, 2779 (2024). doi:10.1038/s41467-024-47108-8
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


