NPJ:同济大学医学院李思光/靳令经团队,破解运动缓解帕金森病之谜!
来源:奇点糕 2023-02-28 15:13
李思光教授和靳令经教授团队证实了鸢尾素可减轻帕金森病小鼠模型的神经元损伤,并揭示了背后的分子机制,表明鸢尾素是预防或治疗帕金森病的潜在药物。
在中老年群体中,帕金森病是一种常见的神经退行性疾病。
据统计,我国65岁以上人群帕金森病患病率为1.7%,预计到2030年我国帕金森病患病人数将达到500万,几乎占到全球帕金森病患者人数的一半[1]。
遗憾的是,时至今日,无论是药物还是手术,都只能改善患者的症状,不能阻止病情的发展,更无法治愈帕金森病。因此,寻找新的治疗手段,仍是科学家和临床医生研究的重点。
近日,由同济大学医学院李思光/靳令经领衔的研究团队,在自然合作期刊npj parkinson's disease上发表了一项重要研究成果[2],揭示了运动能改善帕金森病症状的潜在原因。
他们首先让23名帕金森病患者做了为期12周的定期康复锻炼,发现定期康复锻炼可以增加这些患者的血清鸢尾素水平,而且血清鸢尾素水平的增加与患者平衡功能的改善呈正相关。
随后在帕金森病小鼠模型上的研究表明,鸢尾素可以通过防止线粒体损伤的方式,发挥保护神经的作用。研究人员认为,外周给予鸢尾素是治疗帕金森病的一种潜在疗法。

论文首页截图
“生命在于运动”是我们的口头禅,然而要说清楚运动为何有益于生命健康却非易事。
康复与运动疗法是指南推荐的帕金森病疗法之一。很多帕金森病患者都存在的步态障碍、姿势平衡障碍、语言和/或吞咽障碍等轴性症状,虽然药物治疗疗效甚微,但是康复和运动疗法可以帮助患者缓解这些症状[1]。
这是为什么呢?李思光教授和靳令经教授团队,将注意力放在了鸢尾素上。
鸢尾素问世的时间并不长,它是由哈佛医学院Bruce M. Spiegelman团队在2012年发现的文[3]。当时Spiegelman就认为,这种运动后由肌肉产生的物质,可能对人类代谢疾病和其他通过运动能得到改善的疾病具有治疗作用[3]。
不出Spiegelman所料,七年之后的2019年,巴西里约热内卢联邦大学和美国哥伦比亚大学的研究人员发现,运动时肌肉释放的鸢尾素,确实能拯救因阿尔茨海默病造成的突触可塑性和记忆能力损伤[4]。
这意味着,运动后产生的鸢尾素有可能也是改善帕金森病症状的关键。
为了了解运动疗法对帕金森并患者血清鸢尾素水平的影响,李思光教授和靳令经教授团队招募了23名帕金森病患者,让他们开展了为期12周的定期康复锻炼,然后不对比锻炼前后血清中鸢尾素浓度的变化。
他们首先注意到,康复锻炼确实可以改善帕金森病患者的运动功能和平衡能力。而且检测结果也没让他们失望,帕金森病患者康复锻炼之后的血清鸢尾素水平(2.11±0.53μg/mL)明显高于锻炼之前(1.89±0.62μg/mL)。
更重要的是,血清鸢尾素水平的增加与判断患者平衡功能的Berg平衡量表(BBS)评分呈正相关(R=0.49,p=0.018)。
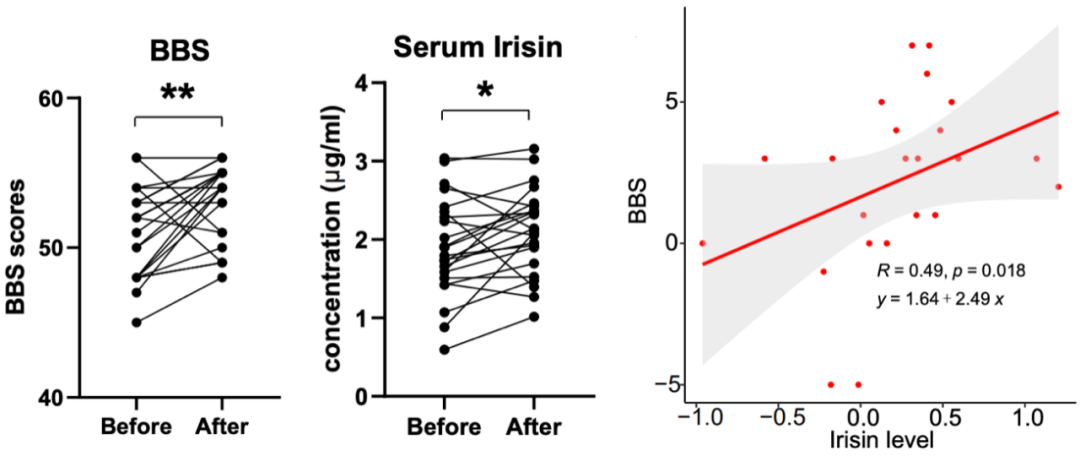
运动前后患者的BBS和血清鸢尾素的变化,以及二者之间的相关性
研究人员给帕金森病小鼠模型注射鸢尾素之后,能改善小鼠的运动功能和多巴胺能神经退行性病变。人体研究和小鼠模型的初步研究表明,运动产生的鸢尾素在改善帕金森病患者的症状方面,确实发挥了重要的作用。
接下来要解答的问题是,鸢尾素究竟通过什么样的方式改善了帕金森病患者的症状。
在查阅文献资料之后,李思光教授和靳令经教授团队发现,大量的研究均表明线粒体功能障碍是帕金森病的核心[5-9]。
因此,接下来的工作就是在帕金森病小鼠模型中探索鸢尾素对线粒体的影响。
通过大量实验反复验证,他们发现注射到小鼠血液中的鸢尾素没有进入神经细胞里面,而是通过与细胞表面的受体结合,激活靶细胞的PI3K-Akt通路和MAPK通路,进而发挥了缓解细胞凋亡和氧化应激、抑制线粒体分裂、促进线粒体呼吸和生物生成的神经保护作用。
总的来说,李思光教授和靳令经教授团队证实了鸢尾素可减轻帕金森病小鼠模型的神经元损伤,并揭示了背后的分子机制,表明鸢尾素是预防或治疗帕金森病的潜在药物。
另外,这个研究揭示了适度运动有助于改善疾病症状的潜在机制,加深了帕金森病患者对康复与运动疗法的认知,或许会提高患者对康复与运动疗法的依从性。
参考文献:
[1].中华医学会神经病学分会帕金森病及运动障碍学组, 中国医师协会神经内科医师分会帕金森病及运动障碍学组. 中国帕金森病治疗指南(第四版) [J] . 中华神经科杂志, 2020, 53(12) : 973-986. DOI: 10.3760/cma.j.cn113694-20200331-00233.
[2].Zhang X, Xu S, Hu Y, et al. Irisin exhibits neuroprotection by preventing mitochondrial damage in Parkinson's disease. NPJ Parkinsons Dis. 2023;9(1):13. Published 2023 Jan 31. doi:10.1038/s41531-023-00453-9
[3].Boström P, Wu J, Jedrychowski MP, et al. A PGC1-α-dependent myokine that drives brown-fat-like development of white fat and thermogenesis. Nature. 2012;481(7382):463-468. Published 2012 Jan 11. doi:10.1038/nature10777
[4].Lourenco MV, Frozza RL, de Freitas GB, et al. Exercise-linked FNDC5/irisin rescues synaptic plasticity and memory defects in Alzheimer's models. Nat Med. 2019;25(1):165-175. doi:10.1038/s41591-018-0275-4
[5].Langston JW, Ballard PA Jr. Parkinson's disease in a chemist working with 1-methyl-4-phenyl-1,2,5,6-tetrahydropyridine. N Engl J Med. 1983;309(5):310. doi:10.1056/nejm198308043090511
[6].Alessi DR, Sammler E. LRRK2 kinase in Parkinson's disease. Science. 2018;360(6384):36-37. doi:10.1126/science.aar5683
[7].Bonifati V, Rizzu P, van Baren MJ, et al. Mutations in the DJ-1 gene associated with autosomal recessive early-onset parkinsonism. Science. 2003;299(5604):256-259. doi:10.1126/science.1077209
[8].González-Rodríguez P, Zampese E, Stout KA, et al. Disruption of mitochondrial complex I induces progressive parkinsonism. Nature. 2021;599(7886):650-656. doi:10.1038/s41586-021-04059-0
[9].Malpartida AB, Williamson M, Narendra DP, Wade-Martins R, Ryan BJ. Mitochondrial Dysfunction and Mitophagy in Parkinson's Disease: From Mechanism to Therapy. Trends Biochem Sci. 2021;46(4):329-343. doi:10.1016/j.tibs.2020.11.007
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


